Terheléses kardiológiai vizsgálómódszerek ischaemiás szívbetegségben
• Kardiológiai Szakmai Kollégium •
Írták: Balogh Ildikó, Forster Tamás, Jánosi András (munkacsoport-vezető), Szilvási István
A cardiopulmonalis rendszer alapvető élettani funkciója a különböző szervrendszerek megfelelő vérellátásának biztosítása mind nyugalmi körülmények között, mind terhelés alatt. Terhelés hatására a szervezetben egy komplex adaptációs láncreakció indul meg, amelynek legfontosabb eredménye, hogy a perctérfogat akár hatszorosára is megnövekedhet, valamint megváltozik a szervek perfúziójának aránya annak függvényében, hogy melyek azok a szervrendszerek, amelyek működése az adott pillanatban a legnagyobb mértékű növekedést mutatja a nyugalmi állapothoz képest. Az adaptációs reakció mértékét a terhelés nagysága, formája, az egyén életkora, neme és edzettségi állapota határozza meg.
A cardiopulmonalis rendszer motorja a szív, vérellátásának növekedése párhuzamosan halad az általa végzett munkával. Egészséges egyénnél a coronariakeringés rezervkapacitása négy-ötszörös. Könnyen belátható, hogy a keringési rendszer működési zavarai kezdetben csak terhelésre manifesztálódnak. Ebből következik, hogy a keringési rendszer vizsgálatának integráns része a terheléses vizsgálatok elvégzése. Lényeges szempont, hogy a keringési rendszer különböző megbetegedései (ischaemiás szívbetegségek, strukturális szívhibák, szívizombetegségek stb.) azonos mértékű funkciókárosodást eredményezhetnek, vagyis különböző etiológiájú, eltérő morfológiai eltérések a funkcionális kapacitás azonos mértékű károsodását idézhetik elő.
A következőkben az ischaemiás szívbetegségek szempontjából áttekintjük a legfontosabb terheléses kardiológiai vizsgálómódszerek indikációjának, végrehajtásának és értékelésének fontosabb kérdéseit. Az EKG-vizsgálatot 100 éve alkalmazzuk a diagnosztikában, azért, mert a szív elektromos folyamatairól rajzolt görbe esetenként jelzi, jelezheti a kóros működést. A szív ultrahangvizsgálata láthatóvá tette a szív különböző részeinek mozgását, az áramlási viszonyokat. Elégtelen vérellátás esetén a szívizom funkciója megváltozhat, és ennek diagnosztikus jelentősége van. A koszorúér-keringés funkcionális eredménye a perfúzió, amelynek vizsgálata a myocardiumszcintigráfia segítségével lehetséges, és az elégtelen perfúzió a koszorúér-keringés károsodására utalhat. Súlyos perfúziós zavar esetén is lehet élő, de jelentős funkcionális károsodást mutató szívizom, amelynek kimutatása farmakológiai terheléssel kombinált izotóp- és echokardiográfiás módszerrel, továbbá pozitronemissziós tomográffal lehetséges. Így állt össze ezen összefoglaló tartalma, amely igyekszik képet alkotni a terheléses kardiológiai vizsgálatok szerepéről az ischaemiás szívbetegség felismerésében, a funkcionális kapacitás és a prognózis megítélésében.
A terheléses ekg-vizsgálat
A terheléses EKG-vizsgálat során folyamatosan növekvő dinamikus terhelés alkalmazása mellett figyelemmel kísérjük az alapvető hemodinamikai paraméterek (szívfrekvencia, vérnyomás) és az EKG változását (ingerképzési és -vezetési zavarok, valamint ST-depresszió és -eleváció), továbbá a beteg panaszait annak megítélésére, hogy a terhelés során jelentkezik-e olyan tünet vagy panasz, amely a keringési rendszer kóros működésére utal.
Személyi feltételek
A terheléses EKG indikációjának felállítása orvosi feladat, az a team végezze, amelyik kompetens a beteg további vizsgálatának és kezelésének, komplex kardiológiai megítélésének kérdésében. A terheléses vizsgálat ellenjavallatait az 1. táblázat tartalmazza. A vizsgálat orvosi felügyelethez kötött, a felügyeletet ellátó orvosnak tisztában kell lennie a vizsgálat indikációjának, kontraindikációjának, kiértékelésének, kivitelezésének és az esetleges szövődmények ellátásának elméleti és gyakorlati kérdéseivel. A gyakorlat megszerzéséhez minimálisan 100 vizsgálatban való tevékeny részvétel szükséges (7), amelynek során a leletezés gyakorlott vizsgáló ellenőrzése mellett történik. A vizsgálatot a kellő jártasság megszerzése után nem kardiológus is végezheti.
1. táblázat A terheléses vizsgálat ellenjavallatai | | Abszolút ellenjavallatok: - Heveny szívizominfarktus (2 napon belül).
- Instabil angina pectoris (ha gyógyszeres kezeléssel nem stabilizálható).
- Tüneteket és/vagy hemodinamikai zavarokat okozó ingerképzési, -vezetési zavar.
- Tünetekkel és szignifikáns gradienssel járó aortastenosis.
- Hemodinamikailag instabil szívelégtelenség.
- Akut pulmonalis embolia.
- Myocarditis, akut pericarditis.
- Aortadissectio.
|
| Relatív ellenjavallatok: - Ismert főtörzsszűkület.
- Közepesen súlyos billentyűbetegség.
- Elektroliteltérés.
- Súlyos hipertónia (szisztolés vérnyomás ≥200; diasztolés ≥110 Hgmm.
- Tachyarrhythmia, bradyarrhythmia.
- Hipertrófiás obstruktív cardiomyopathia (jelentős gradienssel).
- Magas fokú AV-blokk.
- Akut lázas betegség.
- Korlátozott szellemi teljesítőképesség, ami a vizsgálat szabályos végrehajtását akadályozza.
|
Tárgyi feltételek
A vizsgálatot jól szellőztethető, lehetőleg légkondicionált vizsgálóban kell végezni, ahol az esetleges szövődmények ellátásának objektív feltételei adottak. A kerékpár vagy járószőnyeg mellett leülésre, lefekvésre szolgáló hely kialakítása célszerű. A terheléses vizsgálóba betegszállító ülőkocsi vagy ágy betolása szükséges lehet.
A terheléses vizsgálatot elektromos fékezésű kerékpáron vagy elektromos meghajtású járószőnyegen végezzük. A vizsgálat során folyamatos EKG-monitorozás szükséges (legalább 3 elvezetés), minden terhelési fokozatnál vérnyomás- és szívfrekvencia-mérés, illetve 12 elvezetéses EKG-papírregisztrátum készítése kötelező. Az EKG ST-analízist végző programja nem helyettesíti az értékelhető papírregisztrátum készítését és annak vizuális elemzését.
A terhelési laboratóriumban a resuscitatióhoz szükséges eszközöknek (defibrillátor, Ambu ballon, tubus stb.) - működőképes állapotban - rendelkezésre kell állniuk, csakúgy, mint a leggyakrabban használt gyógyszereknek. Az újraélesztésnél alkalmazott eszközök állapotát havonta, az ergométer (kerékpár vagy járószőnyeg) karbantartását évente el kell végezni és erről írásos dokumentumot szükséges készíteni (műszer-karbantartási nyilvántartás). A terheléses vizsgálat alatt előforduló súlyos szövődmények (szívinfarktus, kamrafibrilláció, halál) gyakorisága elérheti akár az 1/2500 vizsgálatot is (1). Az indikációk és kontraindikációk gondos mérlegelésével ez a szám csökkenthető.
A USA-ból származó adatok szerint (2) 1996-ban a leggyakrabban elvégzett terheléses kardiológiai vizsgálómódszer a terheléses EKG volt. Ha a terheléses EKG költségét 1-nek vesszük, akkor a terheléses echokardiográfia kétszeres, a perfúziós izotópvizsgálat 5-szörös, a szívkatéteres vizsgálat 20-szoros költséggel jár (ezért az első választandó módszer ischaemiás szívbetegség kimutatásában - ha kivitelezhető - a terheléses EKG).
A terheléses vizsgálat megszakításának indikációi
Amennyiben a vizsgálatnak nincs abszolút vagy relatív megszakítási indikációja (2. táblázat), akkor befejezése sok esetben a maximális szívfrekvencia (220-életkor), illetve ennek bizonyos százalékának elérésén alapul (a szubmaximális frekvenciának a maximális szívfrekvencia 85%-át tekintik, ennek elérésekor szubmaximális terhelésről beszélünk). Tekintettel arra, hogy a szívfrekvencia változása sok esetben nem arányos a terhelés nagyságával (pl. hiperkinetikus egyének esetén), a terhelés nagyságának lemérésére a szívfrekvencia nem ideális. Tünetlimitált terhelés során a terhelés nagyságának mérésére a Borg-beosztást is alkalmazzák, amelyben a vizsgált egyén határozza meg a terhelés erősségét egy 6-tól 20-ig terjedő skálán. Összefoglalóan a terheléses vizsgálatot mindaddig célszerű folytatni, ameddig nem észlelünk megszakítási indikációt, igyekezvén elérni az egyén által teljesíthető legnagyobb terhelést.
2. táblázat A terheléses vizsgálat megszakításának indikációi | | Abszolút megszakítási indikációk: - A szisztolés vérnyomás ≥10 Hgmm-nél nagyobb csökkenése növekvő terhelés mellett, ha a myocardium ischaemiának egyéb jelei is vannak.
- Közepes vagy annál erősebb angina pectoris.
- Központi idegrendszeri tünetek (ataxia, szédülés, fenyegető syncope).
- Hipoperfúzió jelei (jelentős sápadtság, cianózis).
- Tartós kamrai tachycardia (≥30 s).
- ≥1 mm-es ST-eleváció olyan elvezetésben, ahol nincs patológiás Q-hullám.
- A folyamatos monitorozás (EKG, vérnyomás) feltételei megszűnnek.
- A beteg kérése (az egyén nem kívánja a vizsgálatot folytatni).
|
| Relatív megszakítási indikációk: - A szisztolés vérnyomás ≥10 Hgmm-nél nagyobb csökkenése növekvő terhelés mellett.
- Jelentős ST-depresszió kialakulása (>2 mm horizontális vagy lefelé irányuló „downsloping”) vagy a QRS-tengely hirtelen kialakuló, jelentős megváltozása.
- Ingerképzési zavarok: multifokális ventricularis extrasystolia, 3 tagú kamrai futam, supraventricularis tachycardia, AV-blokk, bradyarrhythmia.
- Kifáradás, fulladás, asztmás jellegű légzés, lábfájdalom, claudicatiós jellegű panasz.
- Bal Tawara-szár-blokk vagy intraventricularis vezetési zavar kialakulása.
- Fokozódó mellkasi fájdalom.
- Kóros tenzióválasz (szisztolés RR >250 Hgmm, diasztolés RR 115 Hgmm).
|
A terheléses vizsgálat elvégzésének indikációi
A terheléses vizsgálat elvégzésének számos indoka lehet, de a vizsgálat hasznosságának tudományosan alátámasztott indikációi ennél szűkebbek. A vizsgálat elvégzése tünetmentes egyéneken, általános szűrővizsgálat részeként még egyéb rizikófaktorok jelenléte esetén sem javasolható. Alapvetően 4 szempont miatt célszerű elvégezni a terheléses vizsgálatot: a koszorúér-betegség (ISZB) diagnózisa szempontjából (akiknél a betegség még nincs igazolva); ismert koszorúérbetegek prognózisának megállapítására; a myocardium ischaemia kimutatása céljából, amikor ismert koszorúérbetegeknél az adekvát terápiát (gyógyszeres kezelés versus revascularisatio) kívánjuk meghatározni, annak alapján, hogy van-e provokálható ischaemia vagy nincs; illetve a funkcionális kapacitás meghatározása céljából, pl. rehabilitáció során. A terheléses vizsgálat elvégzésének indikációit a 3. táblázat tartalmazza.
3. táblázat A terheléses vizsgálat indikációi | - Az ISZB diagnózisának felállítására olyan egyéneknél, akiknél a betegség fennállásának valószínűsége közepes,* és nincs olyan EKG-eltérés, amely vizsgálat értékelését nem teszi lehetővé.**
- Vasospasticus angina (Prinzmetal angina pectoris) esetén.
- Ismert koszorúérbetegek funkcionális kapacitásának meghatározása.
- Olyan koszorúérbetegek esetén, akiknél állapotváltozás észlelhető.
- Posztinfarktusos betegek esetén a prognózis megítélése, a mozgásterápia meghatározása és a gyógyszeres terápia eredményességének megállapítása céljából; az infarktust követő 7. napon szubmaximális, a 14-21. nap között tünethatárolt terheléses vizsgálat történik.
- A myocardium ischaemia kimutatása revascularisatiós beavatkozás előtt.
- Revascularisatiós beavatkozás után a közvetlen eredmény lemérésére (1-6 hónap), illetve a gondozás részeként (évente).
- Revascularisatiós beavatkozás utáni ismételt panaszok jelentkezése esetén.
- Munkaképesség, szívtranszplantáció eldöntésére a funkcionális kapacitás meghatározása.
- A frekvencia (rate) reszponzív pacemaker megfelelő beállítása céljából.
- A terheléssel összefüggő ingerképzési zavarok vizsgálata.
* Az ISZB valószínűsége a terheléses vizsgálat elott a nem, az életkor és a panaszok jellege alapján állapítható meg (5. táblázat). ** WPW-szindróma, pacemakerritmus, BTSZB, 1 mm-t meghaladó nyugalmi ST-depresszió. |
Speciális esetekben szükség lehet a terhelés során elvégzendő ergospirometriás vizsgálatra. A maximális oxigénfogyasztás direkt mérése a funkcionális kapacitás legpontosabb meghatározási módja, segít annak eldöntésében, hogy a funkcionális kapacitás beszűkülésének elsősorban kardiális vagy pulmonalis oka van. Az ergospirometriás vizsgálat indikációit mutatja a 4. táblázat.
4. táblázat A terheléses ergospirometriás vizsgálat indikációi | - Szívelégtelenség miatt megfelelően kezelt betegek funkcionális kapacitásának meghatározása, akiknél szívtranszplantáció indikációjának kérdése merül fel
- A beszűkült funkcionális kapacitás okának pontosabb vizsgálata, a korlátozott fizikai teljesítőképesség kardiális vagy pulmonalis okának megállapítása
|
A terheléses vizsgálat kivitelezésének módja
A terheléses vizsgálatok végrehajtásának személyi és tárgyi feltételeivel kapcsolatban már röviden összefoglaltuk a legfontosabb szempontokat. A terhelési protokollok megválasztása a vizsgáló döntésén alapul. Az egyes protokollok részletes leírása a megfelelő kézikönyvekben megtalálható. A leggyakrabban használatos kerékpár-ergometriás terhelési protokoll a következő:
- 10 wattos bemelegítés 1 percig, majd a terhelés folyamatos emelése;
- 25 wattonként;
- minden terhelési fokozaton a vizsgálandó személy 2 percig kerékpározik;
- a terhelés megszakításakor a beteg 10 Watt terhelés mellett 5-7 percig kerékpározik (levezetés).
A treadmill protokollok közül a leggyakoribb a Bruce által bevezetett terhelési mód, amely ugyancsak folyamatos terhelést alkalmaz, minden terhelési lépcső 3 percig tart, a járószőnyeg sebességét és meredekségét minden terhelési lépcső esetén változtatjuk. A Bruce terhelési protokoll egyes terhelési fokozataihoz tartozó sebességet, a lejtő meredekségét, a testsúlykilogrammra jutó oxigénfogyasztást, illetve a teljesítményt MET-ben a következőkben mutatjuk be.
| Fokozat | Sebesség
(mile/óra) | A lejtő meredeksége
(%) | Oxigénfogyasztás
ml/tskg/perc | MET | | 1 | 1,7 | 10 | 18 | 6 |
| 2 | 2,5 | 10 | 25 | 7,5 |
| 3 | 3,4 | 14 | 32 | 10 |
| 4 | 4,2 | 16 | 44 | 13 |
| 5 | 5,0 | 18 | 57 | 16 |
| 6 | 5,5 | 20 | 68 | 20 |
tskg = testsúlykilogramm
Betegkiválasztás
A terheléses EKG-vizsgálat teljesítményét nagymértékben befolyásolja a vizsgált populáció. A klinikai alkalmazhatóság szempontjából az optimális betegcsoportot azok alkotják, akiknél a vizsgálat elvégzése előtt (preteszt valószínűség) az ISZB fennállásának valószínűsége közepes. A preteszt valószínűség meghatározását a klinikai adatok alapján az 5. táblázatban tüntettük fel (2).
Diagnosztikus teljesítmény
A terheléses vizsgálat diagnosztikus értéke az érzékenységgel és fajlagossággal jellemezhető. Érzékenység („sensitivity”): azon páciensek százalékos aránya, akiknél a terheléses vizsgálat pozitív eredményű, és a koronarográfia is szignifikáns* ISZB-t igazol. Fajlagosság („specificity”): azon paciensek aránya, akiknél a terheléses vizsgálat negatív, és a koronarográfia sem igazol szignifikáns ISZB-t. Nagyszámú tanulmány (147) és 24 047 beteg adatainak metaanalízissel végzett értékelése során (3) a terheléses vizsgálat érzékenysége 68%, fajlagossága 77%, prediktív értéke 73% volt. A terheléses vizsgálat negatív eredménye nem zárja ki a coronariabetegség fennállását.
* A szignifikáns ISZB meghatározásának definíciója változik az irodalomban: egyesek 50%-os, mások 70%-os lumenszukületet tekintenek szignifikánsnak. Irodalmi metaanalízisek azt mutatják, hogy ezen eltérő kritériumrendszer nem befolyásolja a terheléses vizsgálat érzékenységét.
Prognosztikus jelentőség
A terheléses vizsgálat elvégzésének egyik fontos indikációja a prognózis megítélése. Az értékelhető és negatív terheléses EKG-vizsgálat (a provokálható ischaemiának sem klinikai, sem EKG-jele nincs) jó prognózist jelent. A terheléses paraméterek alapján prediktálható prognózis megítélésére a Duke treadmill score alkalmas. A score kiszámításának módszere az 1. ábrán látható. Az egyszerűbb megítélés során csak az elért MET-et vesszük figyelembe. A 7 MET teljesítményt elérő vagy azt meghaladó betegek prognózisa jó, amennyiben a terheléses vizsgálat negatív (6). Alacsony terhelhetőség rossz prognózisra utalhat.
5. táblázat A koszorúér-betegség „preteszt valószínűsége”* az életkor, a nem és a panaszok jellege alapján
Életkor (év) | Nem | Típusos angina pectoris** | Atípusos angina pectoris** | Extracardialis mellkasi fájdalom** | Tünetmentes | | 30-39 | Férfi
Nő | Közepes
Alacsony | Közepes
Nagyon alacsony | Alacsony
Nagyon alacsony | Nagyon alacsony
Nagyon alacsony |
| 40-49 | Férfi
Nő | Magas
Közepes | Közepes
Alacsony | Közepes
Nagyon alacsony | Alacsony
Nagyon alacsony |
| 50-59 | Férfi
Nő | Magas
Közepes | Közepes
Közepes | Közepes
Alacsony | Alacsony
Nagyon alacsony |
| 60-69 | Férfi
Nő | Magas
Magas | Közepes
Közepes | Közepes
Közepes | Alacsony
Alacsony |
* A valószínűségek meghatározása: >90% magas; 90-10% közepes; <10% alacsony; <5% nagyon alacsony.
** Típusos angina pectoris jellemzői (mind a három jelen van): (1) substernalis fájdalom és/vagy diszkomfort; (2) a panaszt terhelés vagy emocionális stressz váltja ki; (3) nyugalomban vagy nitroglicerin hatására a panasz megszűnik. Atípusos angina pectoris: a fenti három jellemzőből 2 jelen van. Extracardialis mellkasi panasz: a karakterisztikus panaszok közül egy vagy egy sincs jelen.

A terhelési paraméterek alapján kiszámítható prognózis. A terhelés alatt észlelt maximális ST-depresszió értékét az első vonalon jelöljük, majd a terhelés alatt észlelt anginát a harmadik vonalon bejelölve és a két pontot egyenessel összekötve a 2. vonalon kapunk egy pontot. Ha a kapott pontot és a teljesítmény MET-értékét összekötő vonalat meghúzzuk, akkor a 4. vonalon a prognózis leolvasható (5).
A terheléses vizsgálat eredményét befolyásoló gyógyszerek
A terheléses EKG eredményét több gyógyszer befolyásolja (digitálisz, antiischaemiás, antiaritmiás szerek), ezért a diagnosztikus indikáció alapján végzett vizsgálatoknál célszerű e gyógyszerek alkalmazása nélkül végezni a vizsgálatot. Amennyiben e gyógyszerek szedése mellett jelentkezik a beteg a vizsgálatra, nem feltétlenül szükséges ezen készítmények elhagyása, ami némi kockázattal jár (béta-receptor blokkoló), ill. rendkívül időigényes annak kivárása, hogy a gyógyszerhatással egyáltalán ne kelljen számolni (digitálisz esetén 1-2 hét). Negatív eredményű, gyógyszerhatásban végzett diagnosztikus célú vizsgálatot gyógyszerhatás nélkül meg kell ismételni. A béta-receptor blokkolóval kapcsolatos tanulmány nem igazolta, hogy a kezelés megváltoztatta a vizsgálat diagnosztikus teljesítményét (4). Ismert koszorúérbeteg gondozása során a gyógyszerek elhagyása felesleges és veszélyes, ezért nem javasolt.
A terheléses EKG értékelése
A terheléses EKG-vizsgálat során értékelhető változók felsorolása a 6. táblázatban található.
ST-depresszió
Az EKG-felvétel értékelése szempontjából a legfontosabb a V5-elvezetés. Az inferior (II., III., aVF) elvezetésekben jelentkező ST-eltérés sok esetben álpozitív eltérést mutat.
A QRS befejeződése után (J pont) 60-80 msec-mal értékeljük az ST-szakaszt, amely akkor kóros, ha legalább 1 mm-es ST-depresszió észlelhető, és az ST-szakasz lefutása horizontális vagy lefelé irányul („downsloping”).
Az ST-depresszió helye (inferior, anterior stb.) és a myocardium ischaemia lokalizációja között (szemben a szívinfarktussal) nincs összefüggés, ezért a terheléses EKG eredménye alapján a koszorúér-betegség lokalizációjára vonatkozó mindenfajta következtetés megalapozatlan.
6. táblázat A terheléses EKG-vizsgálat kapcsán figyelemmel kísért változók
EKG-változók
Maximális ST-depresszió
Maximális ST-eleváció
ST-depresszió iránya (horizontális, felfelé, lefelé irányuló)
ST-depressziót mutató elvezetések száma
ST-depresszió megszűnésének ideje
ST/szívfrekvencia index
Terhelésre jelentkező kamrai aritmia
ST-depresszió fellépésének ideje
Hemodinamikai változók
Maximális szívfrekvencia
Maximális szisztolés vérnyomás
Maximális kettős szorzat (szívfrekvencia x szisztolés vérnyomás)
Terhelési idő
Terhelésre bekövetkező tenzióesés
Chronotrop elégtelenség
Mellkasi fájdalom
Terhelés provokálta angina pectoris
Terhelés megszakítását indokoló angina pectoris
Angina pectoris fellépésének ideje
ST-eleváció
Patológiás Q-hullám nélkül jelentkező ST-eleváció igen ritka, és transmuralis ischaemiát jelent. Ha az adott elvezetésben patológiás Q-hullám is látható, akkor az ST-eleváció kialakulása inkább falmozgási zavart jelez.
R-hullám-változás
Az esetek többségében az R-hullám amplitúdója a terhelés során növekszik, de ezzel ellenkező irányú változásnak sincs diagnosztikus jelentősége.
ST/szívfrekvencia index korrekciója
Az ST-depresszió fellépésekor észlelt szívfrekvencia és az ebből származtatott különböző paraméterek (ST/szívfrekvencia index slope) nem javítják a vizsgálat diagnosztikus teljesítményét.
Komputer által végzett ST-szakasz-analízis
Az ST-szakasz számítógép által történő értékelése nem helyettesíti a megfelelő minőségű EKG-felvétel készítését és a rendkívül gondos vizuális értékelést. A terheléses EKG zajszűrése, átlagolása sok álpozitív eredményhez vezet. Jelenleg nincs kellő mértékben validált, széles körű felhasználásra ajánlható EKG-elemző algoritmus.
A terheléses EKG eredményét összefoglaló lelet
A terheléses EKG-vizsgálat eredményének összefoglalásakor leletbe kell foglalni mindazokat a fontosabb változásokat, amelyek részletes felsorolása a 6. táblázatban megtalálható. A leletben mindenképpen szerepelnie kell az alkalmazott protokollnak, a terhelés idején alkalmazott gyógyszereknek, az elért teljesítménynek MET-ben kifejezve (6. táblázat), az ST-szakasz változására vonatkozó pontos megállapításnak (típus, nagyság, lokalizáció), a terhelés alatt jelentkező panasz megjelölésének, a pulzus és a vérnyomás kiindulási értékének, ingerképzési vagy -vezetési zavaroknak, valamint a terhelés befejezésekor mért paramétereknek.
7. táblázat A kerékpár-ergometriás terhelés Watt-értékeihez tartózó MET*-ek és a beteg állapotát jellemző funkcionális stádiumok
(70 kg-os betegre számítva)
| Watt | MET | NYHA** | | 25 | 2 | III. |
| 5 | 4 | (3,5-4 MET) |
| 75 | 5 | II. |
| 100 | 6 | (5-7 MET) |
| 125 | 7,5 | |
| 150 | 8,5 | I |
| 175 | 10 | (≥8 MET) |
| 200 | 11 | |
* MET = metabolikus ekvivalens (1 MET = 3,5 ml O2/tskg/perc)
** NYHA = New York Heart Association által kialakított funkcionális stádiumok
Kerékpár-ergometriás vizsgálat során elért Watt átszámítása MET-re:

Terheléses echokardiográfia
A vizsgálat lényege, formái
A terheléses echokardiográfia során a kétdimenziós echokardiográfiát mint képalkotó módszert alkalmazzuk az ischaemia következtében létrejött falmozgászavarok kimutatására és az életképesség megítélésére (10, 11). Különösen indokolt esetben rossz echóablak mellett transthoracalis (TT) nézet helyett a transoesophagealis vizsgálat (TEE) elvégzése lehet szükséges. Az ischaemia provokálására különböző módszereket alkalmazhatunk, mint például fizikai terhelést vagy gyógyszeres terhelési formát. A gyógyszeres terheléseknél a dipyridamolt vagy a dobutamint használhatjuk.
Személyi feltételek
A terheléses echokardiográfia végzéséhez a vizsgálatot végző, ilyen irányban speciálisan képzett kardiológus és szakasszisztens együttműködése szükséges. Az orvos irányítja a vizsgálat lebonyolítását, miközben az echokardiográfiás felvételeket készíti. Az asszisztens adja a terhelést provokáló gyógyszert, készíti az EKG-t és méri a beteg vérnyomását. A vizsgálatot végző személyeknek jártasnak kell lennie a várható szövődmények elhárításában, illetve a cardiopulmonalis resuscitatio kivitelezésében (12).
Tárgyi feltételek
Terheléses echokardiográfiát mindenképpen célszerű nagy felbontóképességű echokardiográffal végezni a jobb várható eredmény, a falmozgászavarok pontosabb megítélése érdekében. A gyógyszeradagoláshoz infúziós pumpa használata javasolt, hogy a terhelést biztosító gyógyszereket minél pontosabban és biztonságosabban lehessen adagolni. Az EKG-eltérés regisztrálásához legalább 3, inkább több (6-12) csatornás EKG-t kell használni. A vérnyomásváltozásokat rendszeresen regisztrálni kell. Az esetleges szövődmények elhárítására defibrillátor és a resuscitatiós készenléti tálca is feltétlenül szükséges (12). A falmozgászavarok pontosabb megítélése érdekében osztott képernyőjű echokardiográf szükséges. Digitális rögzítőegység használata is javasolt, bár ez nem elengedhetetlenül szükséges, de a folyamatos videorögzítésre feltétlenül szükség van (1. táblázat).
1. táblázat A terheléses echokardiográfiás laboratórium felszerelése
| Minimális | Optimális | Nagy felbontóképességű,
osztott képernyőjű echokardiográf | + | + |
| EKG-készülék (minimum 3 csatornás) | + | - |
| 12 csatornás EKG-készülék | - | + |
| Nagy képernyős EKG-monitor | - | + |
| Vérnyomásmérő | + | - |
| Automata vérnyomásmérő | - | + |
| Infúziós pumpa | + | + |
| Defibrillátor | + | + |
| Resuscitatiós készenléti tálca | + | + |
| Digitális képrögzítő egység | - | + |
A vizsgálat indikációi
Terheléses echokardiográfiát abban az esetben célszerű végezni, ha az előzetes terheléses EKG eredménye nem diagnosztikus értékű (11). Ismert coronariabetegség jelentőségének megállapítása is fontos indikációs terület (pl. az 50%-os átmérőszűkület okoz-e ischaemiát). A módszer alkalmas terápiás beavatkozások eredményességének lemérésére is. A terheléses echokardiográfia prognosztikai értéke kiterjed az akut myocardium infarktus utáni rizikó felmérése mellett a nem szívsebészeti beavatkozásra kerülő betegek perioperatív kardiális rizikójának becslésére is (8, 13, 16). Lényeges, új indikációs terület a myocardium életképességének echokardiográfiás megítélése is (12) (2. táblázat).
2. táblázat A gyógyszeres terheléses echokardiográfiás vizsgálatok indikációi
Myocardialis infarktus után a 7-14 napon végezhetünk terheléses echokardiográfiát a korai terhelés helyettesítésére. A „távoli ischaemia” kimutatása itt is invazív kezelés indikációját képezi. Az életképesség megítélése elsősorban azon betegeknél indokolt, akiknek a nyugalmi ejekciós frakciója alacsony. Az életképes szegmentumok meghatározása alapján megbecsülhetjük a műtét utáni ejekciós frakció javulása mértékét. Nem szívműtétre (elsősorban nagyér-műtétre) kerülő betegeknél akkor indokolt gyógyszeres terhelés végzése, ha a klinikai adatok alapján a várható cardiovascularis kockázat fokozott.
A vizsgálat kontraindikációi
A terheléses echokardiográfiás vizsgálatok kontraindikációi igen hasonlóak a többi terheléses vizsgálat kontraindikációihoz (3. táblázat).
3. táblázat A terheléses vizsgálatok kontraindikációi
Abszolút kontraindikációk:
- myocardialis infarktus akut szaka;
- instabil angina pectoris;
- ismert „életveszélyes” coronariaanatómia (pl. bal közös főtörzs szűkülete);
- tünetekkel járó súlyos aortastenosis;
- hemodinamikailag instabil szívelégtelenség;
- akut myocarditis, pericarditis, endocarditis;
- súlyos hipertónia (>200/120 Hgmm nyugalomban);
- lázas állapot, akut infekció alatt;
- súlyos ingerképzési vagy ingervezetési zavar;
- súlyos társbetegség;
- a beteg beleegyezésének a hiánya.
Relatív kontraindikációk:
- hipertrófiás cardiomyopathia súlyos kifolyási obstrukcióval;
- bradyarrhythmia;
- a beteg kooperációjának hiánya.
A vizsgálat kivitelezésének módja
A terheléses echokardiográfia kivitelezésének számos lehetősége van, ezek közül csak azokat ismertetjük itt, melyeknek hazai körülmények között is megvan a realitása.
A terheléses echokardiográfia megszakítási indikációi közel azonosak, mint más terheléses vizsgálatok esetén, kiegészítve azzal, hogy új falmozgászavar megjelenése vagy a meglévő falmozgászavar romlása a vizsgálat egyértelmű pozitivitását jelenti, és megszakítását is indokolja. A falmozgászavarok kiértékelése során a bal kamra szegmentális felosztása pontosítja az ischaemia súlyosságának és kiterjedésének megítélését. Erre a 16 szegmentumos beosztás a legelfogadottabb (1. ábra).
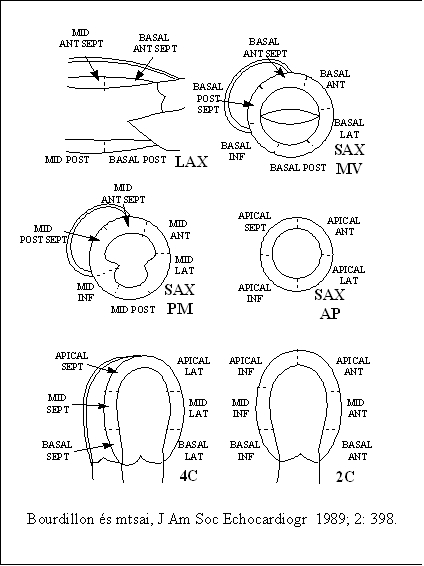
1. ábra 16-szegment modell sematikus rajza.
A fenti ajánlást az American Society of Echocardiography tette.
- LAX = parasternalis hossztengelyi felvétel;
- SAX MV = parasternalis rövidtengelyi felvétel a mitralis billentyű szintjében;
- SAX PM = rövidtengelyi felvétel a papillaris izmok szintjében;
- SAX AP = rövidtengelyi felvétel a szívcsúcshoz közel;
- 4C = csúcsi négyüregi felvétel;
- 2C = csúcsi kétüregi felvétel;
- sept = septalis;
- ant = anterior;
- lat = laterális;
- inf = inferior szegmentum
Fizikai terhelés
A legegyszerűbben alkalmazható terhelési forma a közvetlen előtte - azonnal utána végzett echokardiográfiás regisztrálási mód. A terhelést végezhetjük kerékpáron vagy futószőnyegen, mielőtt a terheléshez fognánk, rögzíteni kell a nyugalmi felvételt. A terhelés csúcsán a beteg ismét haladéktalanul az echokardiográfiás vizsgálóágyra fekszik, majd az echokardiogramot minden felvételi síkból rögzítjük (1, 5, 7). A módszer nehézsége abból adódik, hogy relatíve igen kevés idő áll rendelkezésre a felvételek elkészítésére az ischaemia megszűnte előtt (a négy felvételi irányból egy percen belül kell jó minőségű echófelvételt készíteni). Fizikai terhelés esetén a digitális képrögzítő használata elkerülhetetlen. Ezért inkább a gyógyszeres terhelési formát részesítjük előnyben.
Dipyridamolterhelés
A dipyridamolterhelés előtt, mint minden terheléses vizsgálatnál, a terhelés eredményét befolyásoló gyógyszereket indokolt kihagyni. A nitráttartalmú vegyületeket, kalciumcsatorna-blokkolókat a vizsgálat előtt 24 órával, míg a béta-blokkoló hatású szerek adását 48 órával előbb érdemes felfüggeszteni. Dipyridamolterhelés esetén figyelni kell arra is, hogy a vizsgálat előtti napon a beteg ne fogyasszon nagyobb mennyiségben kávét, teát vagy csokoládét (ezek teofillinszerű anyagot tartalmaznak, mely a dipyridamol hatását antagonizálják). A dipyridamolterhelést is, mint minden terheléses vizsgálatot, éhgyomorral kell végezni.
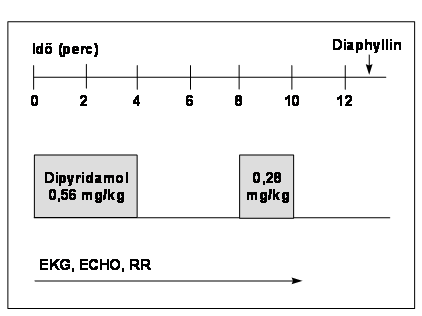
A dipyridamol az adenozin anyagcseréjébe avatkozik bele, gátolja annak lebomlását, ezáltal az adenozin felszaporodik és erős vasodilatatiót hoz létre. A dipyridamol hatásmaximuma ezért kb. 2-2,5 perccel a szer beadása után jelentkezik. A terhelés során először 0,56 mg/kg dipyridamolt adunk 4 perc alatt, majd 4 percig várunk a maximális hatásra. Ezt követően - ha megszakítási indikáció nem áll fenn - 2 perc alatt 0,28 mg/kg dipyridamollal folytatjuk a terhelést (2, 3). A maximális hatás kifejlődése után, amelyhez az esetek többségében minor mellékhatás is társul, antidotum (teofillinszármazék) adásával felfüggesztjük a dipyridamolhatást. A dipyridamolterhelés protokollját a 2. ábra mutatja. A méréseket (EKG, echó, vérnyomás - az ábrán RR) 2 percenként végezzük.
2. ábra A dipyridamolterhelés protokollja
4. táblázat A dipyridamolterhelés szövődményei:
- fejfájás;
- fulladás;
- bradycardia;
- AV-blokk;
- bronchospasmus;
- elhúzódó ischaemia;
- myocardialis infarktus;
- kardiális halálozás.
A szövődmények nem gyakoriak, leginkább az AV-blokkra és a bronchospasmusra hívnánk fel a figyelmet, mert ezen állapotok a vizsgálat elvégzésének kontraindikációját is képezik.
Dobutaminterhelés
Dobutaminterhelésre történő előkészítéskor szintén figyelni kell a gyógyszerek kihagyására, elsősorban a béta-blokkolókra, mert ezek a terhelés eredményét meghamisíthatják.
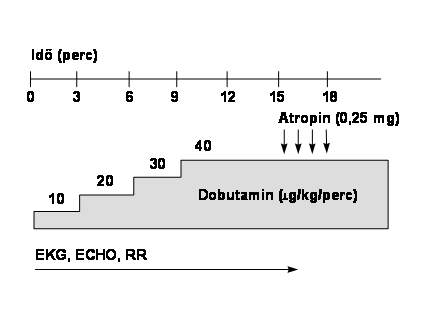
A dobutamin egy szintetikus katecholamin, mely fokozza a myocardium kontraktilitását, emeli a pulzusszámot és kismértékben a vérnyomást is. Szokásos esetben a terhelést 10 mg/kg/perc dózissal kezdjük, majd 3 percenként 10 mg/kg/perc dózissal emeljük egészen 40 mg/kg/perc dózisig. Amennyiben ezt követően kielégítő frekvenciaemelkedést nem tudunk elérni, akkor percenként 0,25 mg Atropin adásával egészítjük ki a terhelést (lásd 3. ábra). A terhelés végén vagy szövődmény jelentkezésekor antidotumot (vénás béta-blokkolót) adunk. Dobutaminterheléses vizsgálat során a vérnyomást minden fázis végén meg kell mérni, míg az EKG-t és az echocardiogramot folyamatosan monitorozzuk, és szintén 3 percenként regisztráljuk (6, 9, 14).
A fenti protokolltól csak abban az esetben térünk el, ha a myocardium életképességének megítélése a cél, amit alacsony dózisoknál lehet a legjobban értékelni. Ilyenkor a kezdő dózist 5 mg/kg/percben állapítjuk meg. Pusztán az életképesség vizsgálata céljából elegendő a 20 mg/kg/perc dózis elérése.
3. ábra A dobutaminterhelés protokollja
5. táblázat A dobutaminterhelés szövődményei:
- myocardialis infarktus;
- kamrafibrilláció;
- kamrai tachycardia;
- kamrai ES-ek fokozódása;
- supraventricularis ES-ek;
- pitvarfibrilláció;
- hipertenzív reakció;
- szimptómás hipotónia;
- hipotónia-bradycardia reakció;
- remegés, tremor.
Gyakori szövődmény a különböző típusú kamrai ritmuszavar és esetenként hipertónia. Ezek előfordulása nyugalmi állapotban a vizsgálat kontraindikációját is képezik.
A vizsgálat helye az ISZB kivizsgálásában
Ischaemiás szívbetegség gyanúja vagy mellkasi fájdalommal jelentkező beteg kivizsgálása során, amennyiben lehetőség van rá, mindig a terheléses EKG legyen az első választandó diagnosztikai módszer. A terheléses echokardiográfia az első választás, ha a terheléses EKG elvégzése valamilyen okból kivitelezhetetlen (15). Ha a terheléses EKG eredménye nem diagnosztikus, a kivizsgálást terheléses echokardiográfiával indokolt folytatni. Ischaemiás szívbetegség alacsony előzetes klinikai valószínűsége esetén - a relatíve sok álpozitív eredményt adó - terheléses perfúziós szcintigráfia lehetőleg kerülendő. Amennyiben az ISZB feltételezett diagnózisa klinikailag megalapozott, de azt sem a terheléses EKG, sem a terheléses echokardiográfia egyértelműen sem kizárni, sem igazolni nem tudta, akkor a terheléses perfúziós szcintigráfiával lehet az ISZB kivizsgálását folytatni.
Terheléses izotópvizsgálatok
A vizsgálat lényege
I.1 Terheléses myocardialis szcintigráfia (stressz MSC), MPI
A terheléses myocardialis szcintigráfia lényege, hogy a vizsgálat során az ergometriás vagy farmakológiai terheléssel elért vérátáramlás-fokozódás maximális szintjén intravénásan radiofarmakont adunk be, mely a vérátáramlástól, perfúziótól függő mértékben jut a myocardium sejtjeibe (uptake), ahol beépül (retenció). A radiofarmakon gamma- vagy röntgensugárzó fotont emittál, mely sugárzás gamma-kamerával leképezhető, a szívizom regionális vérellátásáról jó minőségű kép nyerhető. A jó vérellátású, intenzíven ábrázolódó bal kamrához képest a csökkent perfúziójú régió - a perfúzió csökkenésével arányosan - csökkenő intenzitással jelenik meg. Felvételeinken a koszorúér 50%-ot elérő flow-redukciója esetén már intenzitáscsökkenést, a nekrózis perfúziómentes területén pedig teljes kiesést látunk (fotonmentes terület). A terheléses vizsgálatot követően meghatározott időintervallum után nyugalmi állapotban is felvétel készül, melyeken a regionális perfúziókülönbség megállapítható. Így vizsgálhatóvá válik az ischaemia súlyossága, irreverzibilitás esetén a nekrózis esetleges jelenléte.
Gamma-kamera segítségével planáris (szummációs) többirányú felvétel vagy tomográfiás eljárással ún. SPECT- (single photon emission computer tomography) felvétel készül, melyeken a koszorúér-anatómia ismeretében a bal kamra perfúziója régiónként kvalitatívan és kvantitatívan is elemezhető, a perfúziós eltéréseket az érellátási területekhez rendelve. A planáris felvételhez képest a SPECT-felvételen kisebb eltérés is pontosabban lokalizálható, a szív a közelében elhelyezkedő és a planáris felvételen egybevetülő szervektől jobban elkülöníthető.
A terheléses myocardialis szcintigráfia során alkalmazott radiofarmakonok a Tl-201-klorid és a Tc-99m-hez kötött isonitril vagy tetrofosmin. Alkalmazásuknak fiziológiai alapja: a talliumflow-tól függően jut a myocardium sejtjeihez, káliumanalóg lévén döntően a Na+-K+-ATP-ase segítségével, tehát aktív transzporttal kerül a sejtmembránon át a szívizomsejtekbe, ahol a citoplazmában kötődik. Az uptake mechanizmus tehát metabolikus aktivitást feltételez. A kötődés azonban nem stabil, a tallium a sejtekből az intravascularis és intracelluláris koncentráció különbsége függvényében kimosódik (wash-out). A rossz vérellátású területeken a kimosódás lassult a jó vérellátású területhez képest. Igen jelentős flow-redukciónál az intracelluláris Tl-koncentráció a vérben lévő Tl-koncentrációnál alacsonyabb lehet, ekkor kimosódás helyett bemosódás (wash-in) alakulhat ki. A stresszvizsgálatot követő kb. 4 óra alatt mindezen folyamat (redisztribúció) lejátszódik, a vérellátás nyugalmi állapota „visszarendeződik”. A terheléses myocardialis szcintigráfia „terheléses” felvételén tehát a különbözően megnövekedett perfúziótól függő uptake mechanizmus terhelés alatti regionális különbségét, kb. 4 órával később készült „redisztribúciós” felvételen a kimosódás és esetleg bemosódás regionális különbségét detektáljuk. Az isonitril és tetrofosmin szintén a flow-tól függően jut a sejtekhez, ahol azonban passzív transzporttal kötődik a mitokondriumhoz. Kimosódása gyakorlatilag nincs, tehát a vizsgálat terheléses és nyugalmi fázisa csak két, egymástól független időpontban beadott radiofarmakon-dózissal kivitelezhető.
I.2 Az életképesség-vizsgálat lényege
A nyugalomban csökkent perfúziójú (hibernált) szívizomzat elkülönítése az irreverzíbilisen károsodott (nekrotizált) szívizomzattól az életképesség-vizsgálat lényege. Az életképesség megállapítására legérzékenyebb a PET-vizsgálat. A klinikai gyakorlatban elegendő lehet a SPECT-vizsgálat és a kis dózisú dobutaminterheléses echokardiográfia is. Az életképesség SPECT-vizsgálata során alkalmazott Tl-201-klorid és Tc-isonitril ún. perfúziós radiofarmakonok (perfúzió függvényében jutnak a szívizomsejtekhez), a felvételük azonban a sejtek metabolikus aktivitásához kötött. A tallium az ép sejtmembránon át a Na+-K+-ATP-ase energiaigényes folyamatával épül be a sejtekbe, az isonitril mitokondriumokhoz kötődéséhez a sejtmembrán integritása, a sejtmembránon áthaladáshoz energia szükséges. A nekrózis területén a sejtmembrán roncsolódik, a sejt metabolikus tevékenysége megszűnik, így a tallium, ill. az isonitril myocardiumhoz kötődése nem következhet be, a nekrózis perfúziókiesésként detektálható.
I.3 Akut myocardialis infarktus kimutatása
Az ún. „infarct avid” anyagokkal* (Tc-99m-pirofoszfát, In-111-antimiozin) a szívizomelhalás megállapítható. A Tc-pirofoszfát (Tc-PYP) a mitokondriumban kicsapódó kalciumhoz kötődik, az In-111-antimiozin, azaz miozinellenes antitest az elhalt sejtek miozinjához specifikusan kötődik (immunszcintigráfia). A Tc-PYP-pel az infarktus kialakulása után 12 órával, az In-111-antimiozinnal 1 nap után detektálható az infarktus.
* Olyan izotóp, amely a nekrotikus területhez kötődik.
I.4 A kamrafunkció vizsgálata
A radionuklid-ventrikulográfia (RNV) során tartósan a vérpályában maradó radiofarmakon segítéségével (Tc-99m-mel jelölt vörösvértestek) a bal- és jobbkamra-funkció vizsgálatára nyílik lehetőség, amikor a balkamra-volumen szisztolé-diasztolé alatti változását mérjük a volumenváltozást hűen tükröző aktivitásváltozás mérésével. A vizsgálat nyugalomban és gyógyszeres vagy ergometriás terhelés hatásában is egyaránt elvégezhető. A nyugalmi balkamra-funkció megítélésére első módszerként az echokardiográfia javasolt.
I.4.1 A first pass radionuklid-angiográfiával a radioaktív bolusz centrális keringésen való első áthaladását vizsgáljuk, néhány szívciklus alatt a balkamra-volumenváltozás átlagából számítjuk a kamrafunkciós paramétereket. A vizsgálat nyugalomban és terheléskor egyaránt elvégezhető.
I.4.2 MUGA (gated RNV = EKG-val kapuzott ekvilibriumállapotban végzett RNV)
Az adatgyűjtést az EKG R-hulláma szinkronizálja (EKG gated aquesition). Az R-R intervallumot 16 vagy 32 részre (képre) bontva, egy-egy képbe több száz szívciklus adatait gyűjtjük össze, így a képekben elegendő az információ ahhoz, hogy a kamrafunkció-változást filmszerűen nézhessük, számítógépes feldolgozás segítségével a kamrafunkciós paramétereket, falmozgászavarokat megbízhatóan elemezhessük. Nyugalmi és terheléses vizsgálat egyaránt végezhető (a terhelés lehet fizikai vagy gyógyszeres).
II. Személyi feltételek
A nukleáris medicina szakmai kollégiumának állásfoglalása alapján a nukleáris kardiológiai vizsgálatok megfelelő minőségű kivitelezése, értékelése, az eredmények interpretálása nukleáris medicina szakvizsgával rendelkező orvos feladata. Az izotóplaboratórium további feltételeit illetően utalunk a PET-vizsgálatnál leírtakra (lásd később).
III. Tárgyi feltételek
A perfúziós szcintigráfiás vizsgálat felvételeinek elkészítéséhez alapműszer a SPECT-kamera, mellyel planáris és rétegvizsgálat is készíthető.
A rétegvizsgálatnál elérhető legkisebb feloldóképesség 0,9 cm. A vizsgálat elvégezhető egy vagy többfejes (2-3) SPECT-kamerával. A kétfejes készülék a SPECT-vizsgálathoz szükséges 180 fokos fordulatot szimultán kétirányú leképzéssel, az egyfejes készülékhez képest feleannyi idő alatt teszi meg, így a beteg számára kedvezőbb, rövidebb vizsgálati idő érhető el. A kétfejes, nagy látómezejű (39x53 cm) detektorral rendelkező kamerák változtatható szögállásúak, így a szív vizsgálatához derékszögbe fordíthatók. Az ún. dedikált szívkamera két kisebb látómezejű (22x35 cm) detektora fix derékszög állású. Az adatgyűjtés, kiértékelés és végül archiválás a gamma-kamerához kapcsolt számítógéprendszer segítéségével történik, emiatt a számítógép tárolókapacitása iránti követelmény min. 30 GB. A balkamra-funkció megítéléséhez gamma-kamera is elegendő.
IV. A vizsgálat indikációja
IV.1.1 Myocardium ischaemia kimutatása izotópmódszerekkel (1)
| Indikáció | Módszer | | Diagnózis anginás panasz esetén | Terheléses MSC
Terheléses RNV |
Az ischaemia súlyosságának
lokalizációjának megítélése | Terheléses MSC
Terheléses RNV |
| „Culprit” laesio | Terheléses MSC
Terheléses RNV |
| Risk stratificatio | Terheléses MSCTerheléses RNV |
| Balkamra-funkció meghatározása | RNV (nyugalmi vagy terheléses) |
Revascularisatio utáni
ischaemia kimutatása | Terheléses MSC
Terheléses RNV |
A nukleáris vizsgálatok közül a terheléses RNV alkalmas a myocardium ischaemia igazolására, de a klinikai gyakorlatban lényegesen ritkábban (SPECT hiányában) használjuk. A terheléses myocardialis szcintigráfia alkalmas a regionális flow megítélésére, azaz a perfúziókülönbség detektálására terheléses körülmények között és nyugalomban egyaránt. A vizsgálat segítségével tehát regionális eltéréseket detektálunk, ennek alapján véleményezzük az ischaemia fennállását.
IV.1.2 Kontraindikáció
Az ergometriás, ill. farmakológiai terheléses izotópvizsgálat kontraindikációi megtalálhatók a terheléses EKG, ill. a terheléses echokardiográfia megfelelő fejezeteiben. A sugárterhelés miatt - hasonlóan a konvencionális radiológiai vizsgálatokhoz - a vizsgálat terheseknél, ill. szoptató anyáknál nem végezhető. A sugárterhelés nagysága szervenként és radiofarmakononként eltérő (2), pl. a talliumvizsgálatnál 4,2-24 mGy között változik (teljes test 4,2, szívizomzat 10, vese 24 mGy).
IV.2 Életképesség-vizsgálat
Indikált a vizsgálat elvégzése csökkent balkamra-funkció esetén a revascularisatiós műtét lehetőségének és szükségességének megítélésére. Ha életképes szívizomzat nem mutatható ki, a műtét után alig várható a kamrafunkció változása.
IV.3 Akut myocardialis infarktus kimutatása
A vizsgálat elvégzése csak akkor indokolt, ha a diagnózis megállapítása a klinikum, az EKG-, enzimvizsgálatok eredménye alapján nem lehetséges.
IV.4 Kamrafunkció megítélése
A globális és regionális kamrafunkció (nyugalmi és terheléses) megítélésére akkor indikált az izotópvizsgálat, ha egyéb módszer nem diagnosztikus értékű.
V. A vizsgálatok kivitelezése
V.1 Terheléses myocardialis szcintigráfia kivitelezése
V.1.1 A beteg előkészítése
A dipyridamolterhelés előtt koffein-, teofillintartalmú szerek fogyasztása ellenjavallt. Az optimális leképzéshez éhomi állapot szükséges. (A szív közeli hasi régió magas radiofarmakon-felvétele a myocardialis perfúzió értékelését zavarja, éhgyomri állapottal azonban a hasi szervek vérellátása csökkenthető.)
V.1.2 Terhelés kivitelezése
A terheléses szövődmények elhárítására szolgáló gyógyszerek, valamint a radiofarmakon beadására a terheléses vizsgálatok valamennyi formája előtt a cubitalis vénát kanüláljuk.
Ergometriás terhelésnél a szubmaximális frekvenciaérték elérésekor vagy panasz kialakulásakor a radiofarmakont a vénába juttatjuk, ezután még 1-2 percig a terhelést alacsonyabb szinten folytatjuk fiziológiás sóoldat lassú intravénás adása mellett (a radiofarmakon jó bemosódása érdekében).
Dipyridamolterhelés: összmennyisége 0,56 mg/kg vagy 0,84 mg/kg (high dose), 4 percen keresztül egyenletesen adagolva. A maximális hyperaemia további 2-4 perc múlva alakul ki, ekkor adjuk be a radiofarmakont. Ez alatt a 2-4 perc alatt, valamint a radiofarmakon beadása után is fiziológiás sóoldat adása szükséges.
Dobutaminterhelés: standard protokoll nem ismert. Az általunk alkalmazott protokoll szerint 3 percenként növekvő dózisban 5-10-20-30-40 μg/kg/perc dobutamint adagolunk a szubmaximális frekvencia eléréséig. Ha a célfrekvenciát nem értük el, 0,25 mg/perc Atropin adásával folytatjuk (max. 4 percig).
Adenozinterhelés: 140 μg/kg/perc, 3-4 percig. A radiofarmakont a 3. vagy 4. percben adjuk be, fiziológiás sóoldattal bemosva.
V.1.3 Leképezés
V.1.3.1 Felvételi protokollok
A talliummal végzett terheléses vizsgálatnál csak a stressz-rest sorrend lehetséges (redisztribúció). Tc-isonitril vagy -tetrofosminnál 1 vagy 2 napos stressz-rest vagy rest-stressz sorrendű protokoll egyaránt alkalmazható.
Stresszfelvétel
Talliumnál a beadás után 10 percen belül, Tc-tetrofosminnál optimálisan 60, Tc-isonitrilnél 90 perc elteltével kezdjük a leképezést. A beteg a kamera alatt hanyatt fekvő helyzetben helyezkedik el.
Redisztribúciós vagy nyugalmi felvétel
A stresszfelvételt követően a talliummal történő vizsgálatnál 4 óra múlva ún. redisztribúciós felvétel készül a stesszvizsgálattal megegyező módon. A Tc-tetrofosmin-, Tc-isonitril-vizsgálatnál a nyugalmi vizsgálathoz újabb radiofarmakon-mennyiség beadása szükséges, melyre kb. 3-4 óra múlva kerülhet sor, a terhelésnél alkalmazott aktivitásmennyiség mintegy 3-szorosát fecskendezzük be intravénásan.
V.1.3.2 Adatgyűjtés
• Planáris felvételnél anterior, LAO 45°, LAO 70° felvételi irányból ún. szummációs felvétel készítésével a bal kamra valamennyi régiójának „megörökítése” szükséges (az adatgyűjtés max. ideje kb. 30 perc).
• SPECT-vizsgálat: a kamerát (vagy a két-három fejes változatnál kamerákat) a mellkashoz legközelebbi pozícióba állítjuk. A kamera RAO 45°-tól indul, majd folyamatosan vagy 6°-onként megállva hosszan adatot gyűjt. Az adatgyűjtés ideje max. 30 perc.
V.1.3.3 Adatfeldolgozás
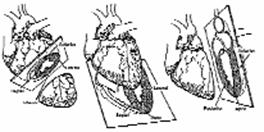
• Planáris felvétel: valamennyi modern SPECT-készülék szoftverprogramjában megtalálható a kvantitatív értékelés lehetősége circumferentialis profilanalízissel (lásd ábra). A circumferentialis analízis során a bal kamra LAO 45°-os vetületi képét a középpontból kiinduló sugarakkal egyenlő, általában 6°-os, 60 részre osztjuk, és valamennyi rész beütésszámát meghatározzuk. A beütésszámértékeket grafikonon egymás mellé helyezzük. A grafikon 100%-os értékének a maximális beütésszámot tartjuk. Így a bal kamra regionális aktivitásfelvétele, azaz perfúzióeloszlása egy profilgörbén kerül ábrázolásra. Az aktivitás-profilgörbén látható eltéréseket normál, önkéntes egyének profilgörbéihez hasonlítjuk, az eltéréseket ehhez mérjük.
• SPECT-felvétel: A szívből (szervezetből) emittált sugárzás sok irányból gyűjtött mérési adataiból számítógépes program segítéségével a szív térbeli képének 3 síkú rétegfelvételi képe nyerhető (a 3 sík: transzverzális, koronális, sagittalis). A SPECT-felvételek pontosabb elemzését teszi lehetővé a bull´s-eye analízis, vagy polar map kép.
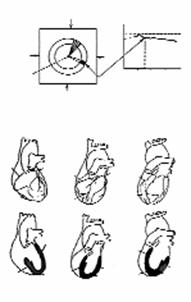
E képen középen a szívcsúcs helyezkedik el, melyet koncentrikus körökként vesz körül a bázis felé haladó, ún. koronális síkú, folyamatosan egymást követő gyűrűk sora. A bull´s-eye, vagy polar map kép középpontjában tehát a szív csúcsa, a legkülső gyűrűjében pedig a szív bázisa helyezkedik el, így az egész szívet kiterítve 2D képben látjuk magunk előtt.
V.2 Életképesség-vizsgálat
A beteg előkészítése: éhgyomri állapot szükséges. Bármely - később leírt - vizsgálati protokoll szerint készüljön is a vizsgálat, a cél: a szív adott keringési viszonyok közti optimális vérellátásának leképezése, ezért szükséges az egyébként is alkalmazott valamennyi antiischaemiás gyógyszer bevétele.
V.2.1 Protokollok:
- Stresszredisztribúciós-reinjekciós vizsgálat: a stresszredisztribúciós felvételt követően a stresszvizsgálathoz alkalmazott talliummennyiség kb. felének beadásával ismételt SPECT-vizsgálat készül.
- Restredisztribúciós vizsgálat: a betegnek nyugalmi állapotban 100-120 MBq talliumot adunk intravénásan, majd kb. 15 perc múlva adatgyűjtést (SPECT-felvétel) kezdünk. 4 órával később készül a redisztribúciós felvétel.
- Stressz-rest vizsgálat: Tc-isonitrillel (megegyezik a terheléses vizsgálatnál leírt protokollal).
V.2.2 Adatgyűjtés, feldolgozás
Az életképesség-vizsgálat során minden esetben SPECT-vizsgálatot végzünk.
V.3 Akut infarktus kimutatása infarct avid radiofarmakonokkal
A gyakorlatban az olcsóbb és könnyebben hozzáférhető Tc-PYP-pel történnek a vizsgálatok. Az In-111-antimiozin igen drága, a hozzáférés is rendkívül nehézkes - a radiofarmakon szállítási időpontjához kötött a felhasználás, hetente kb. 1 alkalommal.
A Tc-PYP-vizsgálat során a radiofarmakon 400-600 MBq mennyiségének beadása után 3-4 óra várakozással többirányú planáris felvétel készül, anterior, LAO 45°, LAO 70° felvételi irányban. A pontosabb lokalizálás, kisebb eltérés detektálása érdekében célszerű SPECT-felvételt is készíteni.
V.4 Radionuklid-ventrikulográfia (RNV)
V.4.1 First pass módszer: A radioaktív bolusz beadásakor a kamera-számítógéprendszer segítségével adatfelvétel kezdődik. A vizsgálat igen rövid időtartamú (max. 1 perc), így a beteg testhelyzete a vizsgálat alatt álló vagy fekvő egyaránt lehet.
A felvételi irányt a vizsgálat célja határozza meg, kamrafunkció mérésére egy irány elegendő, erre optimális a LAO 45°. Falmozgászavar elemzéséhez több felvételi irány elkészítése szükséges: anterior LAO 45°, LAO 70°. Minden vizsgálathoz (felvételi irányhoz) külön injekció, új radioaktív bolusz beadása szükséges.
Adatgyűjtés: másodpercenként legkevesebb 20 képet (frame-et) kell felvenni, 20-30 másodpercig. Átlagban 8-10 szívciklus adatai használhatók fel a kiértékeléshez. Az adatfeldolgozás során a számítógépes képen megjelenő bal kamra fölé ROI-t (region of interest) helyezünk, e területen belül az egy szívciklus alatti aktivitásváltozást fejezi ki az időaktivitás-görbe. Néhány szívciklus összesített, ún. reprezentatív szívciklusának időaktivitás-görbéje megbízhatóan jellemzi a kamrafunkciót.
A vizsgálat nyugalmi állapotban és terhelés hatásában egyaránt készülhet.
V.4.2 MUGA
A vizsgálathoz olyan radiofarmakon szükséges, mely tartósan, akár több órán keresztül is a vérpályában marad. E szempontnak legjobban a Tc-vel jelölt vörösvértest felel meg. A vörösvértestek Tc-vel jelölése in vitro v. in vivo módon történik. A gyakorlatban az egyszerűbben kivitelezhető in vivo módszert alkalmazzuk. Az aktivitásmennyiség 500-700 MBq.
A radiofarmakon intravénásan vérpályába juttatása után 10 perccel, azaz az ekvilibriumállapot elérésekor kezdődik az adatgyűjtés. A vizsgálat céljától függően egy- v. többirányú felvételt készítünk, valamennyi felvételi irány optimális minőségű elkészítéséhez kb. 10-15 perces adatgyűjtés szükséges. Kamrafunkció-meghatározáskor csupán egyirányú - az ún. optimális septalis irányú - felvétel (LAO 30-50°, ahol a bal és jobb kamra a legjobban elkülönül egymástól) elkészítése szükséges. Falmozgászavar elemzéséhez több felvételi irányban készül a vizsgálat, az optimális septalis ferde, anterior, LAO 70°. Az adatgyűjtés szinkronizálásához az EKG R-hulláma szolgál (lásd 1. rész).
A vizsgálat nyugalomban és terhelés hatásában egyaránt elvégezhető.
VI. A vizsgálat értékelésének szempontjai, érzékenység, fajlagosság
VI.1 Terheléses myocardialis szcintigráfia
A planáris és SPECT-felvételek kiértékelése kvalitatívan, szemikvantitatívan vagy kvantitatívan történhet (2).
A planáris vizsgálat háromirányú felvételén a kvalitatív kiértékelés során elemezzük:
- a bal kamra jellemző paramétereit (falvastagság, kamraüreg-tágasság, perfúzióeloszlás);
- a perfúziózavar helyét, kiterjedését, súlyosságát (egy vagy több ér ellátási területében észlelünk-e ischaemiát), reverzibilitását (teljes, részlegesen reverzíbilis, esetleg irreverzíbilis);
- a szív-tüdő aktivitás arányát (a tüdő aktivitása a stressz Tl-felvételen magasabb, ha a véna pulmonalis nyomása megemelkedett).
Szemikvantitatív analízisnél (pl. planáris felvétel circumferentialis profilanalízise, SPECT-vizsgálat bulls-eye analízise). A kvalitatív kiértékelésnél vizsgált fenti jellegzetességek a kvantitatív elemzéssel számszerűsíthetők, pl. a perfúziós eltérés súlyossága a jó perfúzió százalékában megadható, kiterjedése a teljes kamrafal területének százalékában megállapítható.
A kvalitatív elemzéshez képest a kvantitatív analízissel a planáris és SPECT-vizsgálatok szenzitivitása növelhető. ISZB diagnózisának megállapításában (3) a planárishoz képest a SPECT-vizsgálat szenzitivitása magasabb (85-93%), a specificitásban számottevő különbség nincs (78-77%).
A terheléses MSC felvételén rossz prognosztikai jel: a több ér ellátási területében talált súlyos perfúziós eltérés, a magas tüdőaktivitás, a bal kamra reverzíbilis (csak terhelés alatt) vagy irreverzíbilis tágulata.
Álnegativitást okozó tényezők
Technikai ok: nem megfelelő terhelési szint, rossz képminőség, terheléses talliumvizsgálatnál késői felvételkezdés, a myocardialis szcintigráfia nem korrekt interpretációja.
Coronariakeringési ok: kielégítő kollaterális, ún. overlap keringés (adott régiót két ér lát el, melyek egyikének keringészavara ischaemiát nem okoz), „ballanced” hipoperfúzió (háromér-betegségnél a körülírt perfúziózavar hiányozhat, a bal kamra reverzíbilis tágulata jelezheti az ISZB súlyosságát).
Álpozitív szcintigráfiás eredmény
Technikai ok: mamma és diafragma fokozott sugárgyengítése (fotonattenuáció), rossz felvételi technika (beteg elmozdulása).
Valódi ischaemia, epicardialis koszorúér-elváltozás nélkül: hipertrófiás cardiomyopathia, dilatatív cardiomyopathia, balkamra-hipertrófia (a flow-rezerv csökkent!), utóbbi esetekben a vizsgálat specificitása ≤50%, így diagnosztikus értéke csupán a negatív vizsgálatnak van! Az álpozitivitás csökkenthető attenuáció- (elnyelési) korrekcióval. Ez csupán a legmodernebb SPECT-készülékeknél elérhető lehetőség.
VI.2 A myocardium életképesség-vizsgálata
A leképezés módszerének javításával, azaz planáris helyett SPECT-vizsgálatok végzésével, a SPECT-vizsgálatok kvantitatív analízisével, valamint attenuációkorrekció alkalmazásával (mely lehetőség a PET-nél megvan) a vizsgálat megbízhatósága fokozható.
VI.3 Radionuklid-ventrikulográfia
Akut myocardialis infarktusban a jobb kamrai infarktus RNV-vel kimutatható: a jobb kamrai EF csökken, falmozgászavar állapítható meg.
VI.4 Akut infarktus kimutatása infarct avid radiofarmakonokkal
Viszonylag magas szenzitivitása és specificitása ellenére a vizsgálat elvégzése ritkán indokolt.
A pozitronemissziós tomográfia (pet) szerepe a kardiológiában
I. Bevezetés
A pozitronemissziós tomográfia - a PET - pozitronsugárzó radionuklidok detektálásán alapuló korszerű képalkotó eljárás. Kardiológiai jelentőségét az adja, hogy az életképes szívizomzat kimutatásának legmegbízhatóbb vizsgálóeljárása. Elméletileg a koszorúér-betegség következtében kialakuló myocardium ischaemia kimutatásának legpontosabb noninvazív módszere. A PET-technológia egyszerűsödése és elterjedése révén a költséghatékony kardiológiai PET-vizsgálatok számának növekedése hazánkban is várható.
II. A PET fizikai alapjai
A radionuklidból kilépő pozitron - mozgási energiájától függően 0,2-3 mm-en belül - találkozik egy elektronnal. Tömege az ún. megsemmisülési sugárzás következtében két - egy vonal mentén ellentétes irányba haladó -, egyenként 511 keV energiájú elektromágneses sugárzássá alakul. Ezek a fotonok arra alkalmas kristályban fényfelvillanást, szcintillációt okoznak. A PET ezek egyidejű, ún. koincidenciadetektálásával állítja elő a radionuklid-eloszlás rétegfelvételeit.
A PET-berendezések formái:
- Dedikált PET. Detektora több ezer, gyűrűszerűen elhelyezett apró kristályt tartalmaz. A vizsgálandó beteget úgy helyezik el, hogy a detektor mintegy 15-16 cm-es testrészletet „lát”, amelybe a teljes szív „belefér”.
- Koincidencia üzemmódú SPECT-berendezések. Ezeknek több - speciális - gamma-kamera detektora van, amelyek ugyancsak koincidenciadetektálás révén észlelik a pozitronsugárzó radionuklidot. Érzékenységük, időbeli és geometriai felbontóképességük elmarad a dedikált PET-étől, de a myocardium glükózfelvételének vizsgálatára ezek a berendezések is alkalmasak. (Egyetlen gamma-kamera is - speciális, nagy energiájú kollimátorral ellátva - képes detektálni az 511 keV-os fotonokat, de ez a berendezéstípus nem terjedt el.)
III. A PET-vizsgálatok tárgyi és személyi feltételei
- A PET-vizsgálatokat arra alkalmas és hatósági engedéllyel rendelkező, a beteg és a vizsgálószemélyzet megfelelő sugárvédelmét biztosító PET-vizsgáló laboratóriumban végezzük. A PET radionuklidjait ciklotronban állítják elő. Az N-13, O-15 használatához „on-site” ciklotronra van szükség. A C-11 használatához a ciklotron geográfiai közelsége (kilométereken belül) kell, az F-18 felhasználásához 3-4 órán belüli szállítási elérhetőség szükséges.
- Ha a PET-labor egy nukleáris medicina munkahely része, annak infrastruktúráját-személyzetét (adminisztráció, takarítás, betegváró, meleg laboratórium, izotópátvevő, -beadó, hulladéktároló, archiváló, betegvécé, a személyzet szociális helyiségei) használja. Ha önmagában működik, a felsorolt helyiségekre-személyzetre is szükség van.
- A PET-vizsgálatokat nukleáris medicina szakorvos végezheti. Minimálisan szükséges egy izotóp-szakasszisztens és egy operátor is.
- Szükséges felszerelés
- Alkalmas PET-berendezés (dedikált PET/koincidencia gamma-kamera).
- A PET minőségbiztosításához speciális fantomok.
- A radiofarmakon aktivitásmennyiségének méréséhez aktivitásmérő („dóziskalibrátor”).
- A radionuklidok gyors felezési ideje miatt speciális gyorstesztek a radiofarmakon minőségének ellenőrzésére.
- Az FDG-vizsgálatokhoz gyors vércukor-meghatározási lehetőség és gyors hatású inzulin.
- A levett vér aktivitásának mérésére alkalmas műszer.
- A kardiológiai terheléses vizsgálathoz (gyógyszeres terhelést alkalmazunk): dipyridamol (vagy a drága adenozin), dobutamin.
- A kardiológiai terheléses vizsgálathoz: a sürgősségi ellátásához (resuscitatio) szükséges gyógyszerek és eszközök.
IV. A PET-vizsgálatok általános módszertana
- A PET lehet dinamikus vagy statikus vizsgálat. A rutindiagnosztika számára megfelelő a jóval egyszerűbb statikus vizsgálat.
- A dinamikus vizsgálatok adatfelvételét a radiofarmakon beadásával egy időben inditjuk. Rövid (másodperces) adatgyűjtési idejű felvételek sorozatát állítjuk elő, majd ún. „region of interest” (ROI) technikával az érdeklődésre számot tartó területek (pl. a szív különböző szegmentumai) idő-aktivitásgörbéit állitjuk elő. Ezekből - vérvétellel egybekötve a vérbeli aktivitás mérésével vagy a szívüreg vértartalma időaktivitás-görbéjének felhasználásával - matematikai (2 vagy 3 kompartment) modellek révén különböző paramétereket (pl. metabolikus ráta) számolunk ki. A radiofarmakon-felvétel mértéke egyszerűbb, grafikus eljárással is vizsgálható.
- A statikus felvételek értékelése vagy kvalitatíve, vizuálisan, vagy szemikvantitatíve, a regionalis aktivitáseloszlás értékelésével történhet.
- Az 5-10 mm vastag rétegfelvételeket számítógépes adatfeldolgozással - rekonstrukciós eljárással - állítjuk elő. Ez lehet filterezett visszavetítés vagy iterativ eljárás. Mivel a szív és a test tengelyállása eltérő, a szívtengely reorientációját követően állítjuk elő a szív transzverzális, koronális és sagittalis irányú rétegfelvételeit. A radiofarmakon-eloszlás vizsgálható ún. polar map (bulls-eye) kijelzéssel. Ez praktikus a perfúzió és a metabolizmus összehasonlításában. Lehetőség van 3D ábrázolásra is.
- Az élő szövet sugárgyengítő hatásának kompenzálása céljából ún. attenuációkorrekciós eljárásra van szükség. Ehhez egy ún. transzmissziós scant készítünk. Külső sugárforrással pár perc alatt feltérképezzük az adott beteg vizsgált testtájékának - pl. a mellkasának - sugárgyengítő képességét. Ezt használjuk fel a beteg PET-vizsgálati felvételeinek korrigálására.
- A szívizom-perfúzió terheléses PET-vizsgálatát gyógyszeres terheléssel, dipyridamol, adenozin vagy dobutamin alkalmazásával végezzük.
A PET előnyei a nukleáris medicina másik rétegvizsgálati módszerével, a SPECT-tel szemben:
- A C-11, N-13, O-15 és a F-18 alkalmas az élő szervezet különböző építőköveinek, metabolitjainak radioizotópos jelzésére és így a fiziológiai és biokémiai folyamatok, az intermedier anyagcsere képi ábrázolására („slice of life”).
- Az anyagcsere kvantitatíve, mmol/g/perc dimenzióban vizsgálható.
- A detektálás a SPECT-nél sokkal érzékenyebb.
- A PET-felvételek térbeli felbontóképessége jobb, mint a SPECT-é.
V. A PET alkalmazása a kardiológiában
A PET alkalmas a szívizom-perfúzió, a szívizom-anyagcsere (glükóz, zsírsav, oxigénfelhasználás), a szívizom-hypoxia, a szív vegetatív beidegzésének vizsgálatára. A különböző vizsgálatokat különböző radiofarmakonokkal végezzük.
A klinikumban legfontosabb a szív glükózfelvételének vizsgálata a hibernált szívizomzat kimutatására.
Kisebb gyakorlati jelentőségű a szívizom-perfúzió PET-vizsgálata. A szív zsírsavanyagcseréjének, oxigénfelhasználásának, innervációjának és hypoxiájának PET-vizsgálata elsősorban a klinikai kutatás eszköze.
V.1 A szívizom-metabolizmus PET-vizsgálata
A szívizom-metabolizmus PET-vizsgálatai közül a szívizom glükózfelvételét vizsgáljuk F-18-2-fluoro-2-dezoxi-D-glükózzal (FDG). (Ma Magyarországon csupán ennek a PET-módszernek van gyakorlati jelentősége a kardiológiában.)
V.1.1 A módszer lényege
A súlyosan ischaemiás, hibernált szívizomzat a struktúrájának fenntartásához szükséges ATP-t - a főleg zsírsavakat égető normális szívizomzattól eltérően - elsősorban a glükóz anaerob glikolízise útján nyeri. A glükózfelhasználásra utaló FDG-felvétel kimutatható az egyéb módszerekkel életképtelennek tűnő, de nem elhalt (hibernált) szívizomzatban (4, 5).
Az FDG-felvétel és a perfúzió egybevetése. A kifejezetten csökkent perfúziójú terület lehet hegszövet vagy életképes, de veszélyeztetett szívizomzat. Hegszövetben nincs perfúzió, és FDG-felvételt sem látunk, ez a perfúziómetabolizmus „match”. Az életképes, de súlyosan hipoperfundált, hibernált szívizomzatban FDG-felvételt, életképességre utaló anyagcserét látunk, ez a perfúziómetabolizmus „mismatch”. A perfúzió vizsgálatát végezhetjük SPECT-tel is (Tl-201, Tc-99m-sestamibi vagy -tetrofosmin), de ha az FDG-vizsgálatot dedikált PET-tel végeztük (és lehetőségünk van rá), célszerűbb a perfúziót is PET-tel (N-13-NH3) vizsgálni, mert a két PET-módszer eredménye jobban összevethető.
Az FDG-PET az életképesség kimutatásának legpontosabb módszere (1, 4, 5).
V.1.2 Az FDG-PET-vizsgálat menete
A gyakorlati diagnosztikában nyugalmi statikus FDG-vizsgálatot végzünk. Meghatározzuk a beteg vércukorértékét. Ha normális, a szív glükózfelvételének fokozása céljából 50-100 gramm glükózt adunk per os (teában) vagy iv. (ritkábban használt protokollok: glükóz-inzulin-kálium infúzió, illetve glükóz és nikotinsav együttes adása). Diabéteszes betegnek - a vércukortól függő mennyiségű - gyors hatású inzulint adunk.
Az FDG-t ezután 45-60 perc múlva kapja a beteg.
370 MBq FDG-t adunk iv. Ha dinamikus vizsálatot végzünk, az adatfelvételt azonnal indítjuk. Statikus vizsgálat esetén 30-40 perc múlva 15-25 perces adatfelvételt végzünk. A transzmissziós scant az FDG beadása előtt vagy a vizsgálat után is elvégezhetjük.
Az FDG-PET-vizsgálat kiértékelése lehet kvalitatív, szemikvantitatív (polar map ábrázolás) és kvantitatív (dinamikus vizsgálat esetében).
V.1.3 Az FDG-PET klinikai haszna
A perfúziómetabolizmus „mismatch” jó előrejelzője a regionális falmozgás visszatérésének, vagyis annak, hogy a súlyos ischaemia megszüntetése után (revascularisatio) a szívizom adott részének működése javul, ill. normalizálódik (2, 3, 4). Nagyobb betegcsoporton vizsgálva 88%-os érzékenységű és 73%-os fajlagosságú módszernek bizonyult (1), azaz az FDG-felvétel nem feltétlenül jelenti a szövet életképességét.
V.1.4 A szívizom FDG-PET-vizsgálatának indikációja
A vizsgálat indikált azon betegeknél, akiknél felmerül, hogy a revascularisatio kiválthatja a szívtranszplantációt. Ha a rossz balkamra-funkciójú ischaemiás szívbetegben jelentős az életképes myocardium mennyisége (és vannak revascularizálható erek), akkor jó esély van arra, hogy a műtétet követően jelentős javulás következik be a balkamra-funkcióban. A PET-vizsgálat akkor indikált, ha az egyéb noninvazív módszerek nem adnak egyértelmű információt az életképesség kérdésében.
V.2 A szívizom-perfúzió PET-vizsgálata
Az egyetlen noninvazív kvantitatív módszer, amellyel a szívizom perfúziója kvantitatíve - ml/g/percben - meghatározható. Vizsgálatára olyan pozitronsugárzó radiofarmakonokat használunk, amelyek myocardialis felvétele a vérellátástól függ. Közülük az N-13-NH3 és az Rb-82 (generátorból) használatos. A módszernek nálunk jelenleg csak elméleti jelentősége van.
VI. A PET-vizsgálatok sugárterhelése
- Rb-82. 1110 MBq beadása esetén a teljes test effektív dózisegyenértéke 5,3 mSv. A kritikus szerv a vese, sugárterhelése 20 mGy (ICRP 53, 162. oldal).
- F-18-FDG. 370 MBq beadása esetén a teljes test effektív dózisegyenértéke 10 mSv. A kritikus szerv a húgyhólyag, sugárterhelése 63 mGy (ICRP 53, 76. oldal).
- N-13-NH4. 500 MBq beadása esetén a teljes test effektív dózisegyenértéke kb. 1 mSv.
VII. A vizsgálatok kontraindikáltak:
terhes nők és gyerekek esetében. Szoptató nők FDG-vizsgálata esetén tej nem adható 1 napig a csecsemőnek. A kontraindikáció csak elméleti, mert a klinikumban jelenleg e betegcsoportot nem vizsgálják.
Összefoglalás
A terheléses kardiológiai vizsgálatok alapvető jelentőségűek a klinikai gyakorlatban. Alkalmazásukra mindazon esetekben sor kerül, amikor a betegek panaszai ischaemiás szívbetegség gyanúját keltik, illetve akkor is, ha a betegség már igazolt, de a további teendők megítélése végett prognosztikai információkat szeretnénk nyerni. Fontos segítséget jelentenek az előzőekben ismertetett vizsgálatok a kezelés (beavatkozás) eredményességének lemérésében is.
A költséghatékonysági adatok egybehangzóan arra utalnak, hogy ischaemiás szívbetegség gyanúja esetén - a terheléses kardiológiai vizsgálatok közül - első lépésben a terheléses EKG-vizsgálatot végezzük el mindazon esetekben, ha a vizsgálandó személy képes a dinamikus terhelés elvégzésére és nincs olyan EKG-elváltozása, amely nem teszi lehetővé a várható EKG-változás értékelését. Sok esetben a terheléses EKG-vizsgálat negatív eredménye szükségtelenné teszi a továbblépést, máskor az alacsony terhelhetőség és az ischaemiát igazoló tünetek, elváltozások egyértelműen a koronarográfia indikációját jelentik. A terheléses EKG-vizsgálat számos esetben nem ad elégséges diagnosztikus információt, így pl. nem alkalmas az ischaemia lokalizációjának megállapítására.
A terheléses echokardiográfia mindazon esetekben választandó eljárás, amikor a terheléses EKG-vizsgálat el nem végezhető vagy valamilyen okból nem értékelhető. Amennyiben az ischaemiás szívbetegség preteszt valószínűsége magas és a terheléses EKG-vizsgálat negatív, a terheléses echokardiográfia elvégzése ugyancsak szóba jön. A terheléses - az esetek döntő többségében - farmakológiai intervenciót jelent. A vizsgálat érzékenysége és fajlagossága meghaladja a terheléses EKG-vizsgálat hasonló mutatóit, alkalmas a myocardium ischaemia lokalizációjának megállapítására. A vizsgálat végzéséhez és értékeléséhez korszerű ultrahangkészülék, megfelelő gyakorlattal bíró vizsgáló szükséges.
A terheléses izotópvizsgálatok indikációja megegyezik a terheléses echokardiográfiánál leírtakkal. A perfúzió vizsgálata történhet dinamikus terheléssel vagy farmakológiai módszerrel. A vizsgálat technikai feltételei bonyolultabbak, költségei nagyobbak minden előzőleg említett módszernél, ebből következően hozzáférhetősége korlátozott. Az érzékenység és a fajlagosság tekintetében a módszer teljesítménye megegyezik a terheléses echokardiográfia hasonló mutatóival, ugyancsak alkalmas az ischaemia lokalizációjának megállapítására. Mind a terheléses echokardiográfia, mind a terheléses izotópdiagnosztika alkalmas a myocardium életképességének vizsgálatára is.
A választandó „második” diagnosztikai módszer (terheléses echokardiográfia, ill. a terheléses izotópvizsgálat) függ a helyi lehetőségektől, ill. szokásoktól is.
A pozitronemissziós tomográfia (PET) a szívizom anyagcsere-folyamatainak vizsgálatára szolgáló eljárás. Alkalmas az ischaemiás, de életképes myocardium kimutatására. Azokban az estekben, amikor az életképesség megítélésének kérdésében más képalkotó módszer alkalmazásával nem érünk el eredményt, rendkívül hasznos kiegészítő információkat szolgáltat annak eldöntésére, hogy a revascularisatiós eljárás után várható-e érdemleges változás a balkamra-funkcióban. A vizsgálat eredménye jelentősen befolyásolhatja a revascularisatiós beavatkozás indikációját. A vizsgálat - a technikai feltételek bonyolultsága és a magas költség miatt - jelenleg csak jól körülírt indikációk esetén, várakozás után hozzáférhető.
Az akut coronariaszindróma bekövetkezésének valószínűségét egyik terheléses vizsgálómódszerrel sem tudjuk biztonsággal előre jelezni, illetve kizárni.
Irodalom
A terheléses ekg-vizsgálat (dr. Jánosi András)
- Stuart, R. J. Jr., Ellestad, M. H.: National survey of execise stress testing facilities. Chest. 1980;77:94-97.
- ACC/AHA Practice Guidelines for Exercise Testing. JACC. 1997;30:290-315.
- Gianrossi, R., Detrano, R., Mulvihill, D., Lehmann, K., Dubach, P., Colombo, A., McArthur, D., Froelicher, V.: Exercise induced ST depression in the diagnosis of coronary artery disease:a meta analysis. Circulation. 1989;80:87-98.
- Hertbert, W. G., Dubach, P., Lehmann, K. G., Froelicher, VF.: Effect of beta-blockade on the interpretation of the exercise ECG: ST level versus delta ST/HR index. Am Heart J. 1991;122:993-1000.
- Ramamurthy, G., Kerr, J. E., Harsha, D., Tavel, M. E.: The treadmill test-where to stop and what does it mean? Chest. 1999; 115:1166.
- Mark, D. B., Shaow, L., Harrel, F. E. Jr., Hlatky, M. A., Lee, K. L., Bengston, J. R. et al.: Prognmostic value of a treamill exercise score in outpatients with suspected coronary artery disease, N Eng J Med. 1991;325:849-853.
- ACC/AHA Clinical Competence Statement on Stress Testing. JACC. 2000;36:1441-53.
- Ashley, E. A., Myers, J., Froelicher, V.: Exercise testing in clinical medicine. Lancet. 2000;356:1592-97.
Terheléses echokardiográfia (dr. Forster Tamás)
- Feigenbaum, H.: Exercise echocardiography. J Am Soc Echocardiogr. 1988;1:161-166.
- Picano, E., Severi, S., Michelassi, C., Lattanzi, F., Masini, M., Orsini, E., Distante, A., LAbbate, A.: Prognostic importance of dipyridamole-echocardiography test in coronary artery disease. Circulation. 1989;80:450-457.
- Picano, E., Lattanzi, F.: Dipyridamole echokardiography. A new diagnostic window on coronary artery disease. Circulation. 1991;83 (Suppl.III):III-19-III-26.
- Ryan, T.: Dobutamine stress echocardiography. Cor Art Disease. 1991;2:552-558.
- Marwick, T. H., Namec, J. J., Pashkow, F. J., Stewart, W. J., Salcedo, E. E.: Accuracy and limitations of exercise echocardiography in a routine clinical setting. J Am Coll Cardiol. 1992;19:74-81.
- McNeill, A. J., Fioretti, P. M., El-Said, E. S. M., Salustri, A., Forster, T., Roelandt, J. R. T. C.: Enhanced sensitivity for detection of coronary artery disease by addition of atropine to dobutamine stress echocardiography. Am J Cardiol. 1992;70:41-46.
- Aldrich, H. R., Reichek, N.: Stress echocardiography. Curr Op Cardiol. 1993;8:978-987.
- Poldermans, D., Fioretti, P. M., Forster, T., Thomson, I. R., Boersma, E., El-Said, E. S. M., du Bois, N. A. J. J., Roelandt, J. R. T. C.: Dobutamine stress echocardiography for assessment of perioperative cardiac risk in patients undergoing major vascular surgery. Circulation. 1993;87:1506-1512.
- Bach, D. S., Muller, D. W. M., Gros, B. J., Armstrong, W. F.: False positive dobutamine stress echocardiograms: characterization of clinical, echocardiográfic and angiográfic findings. J Am Coll Cardiol. 1994;24:928-933.
- Cheitlin et al.: ACC/AHA guidelines for the clinical application of echocardiography. Circulation. 1997;95:1686-1744.
- Armstrong, V. F., Pelikka, P. A., Ryan, T., Crouse, L., Zoghbi, W. A.: Stress echocardiography: recommendations for performance and interpretation of stress echocardiography Stress Echocardiography Task Force of the Nomenclature and Standards Committee of the American Society of Echocardiography, J Am Soc Echocardiogr. 1998;11:97-104.
- Forster, T., Csanády, M.: Terheléses echocardiographia. Medicina, Budapest, 1998.
- Poldermans, D., Boersma, E., Bax, J. J. et al.: The effect of bisoprolol treatment on perioperative mortality and myocardial infarction in high-risk patients undergoing vascular surgery. Dutch Echocardiographic Cardiac Risk Evaluation Applying Stress Echocardiography Study Group. N Engl J Med. 1999;341:1789-1794.
- Marwick, T. H., Case, C., Sawada, S., et al.: Prediction of mortality using dobutamine echocardiography. J Am Coll Cardiol. 2001;37:754-760.
- Kim, C., Kwok, Y. S., Heagerty, P., Redberg, R.: Pharmacologic stress echocardiography for testing coronary artery disease diagnosis: A meta-analysis. Am Heart J. 2001;142:934-944.
- Romero, L., de Virgilio, C.: Preoperative cardiac risk assessment: An update approach. Arch Surg. 2001;136:1370-1376.
Terheléses izotópvizsgálatok (dr. Balogh Ildikó)
- AHA/ACC Task Force Report: Guideline for Clinical Use of Cardiac Radionuclid Imaging. Report of the American College of Cardiology/American Heart Association Task Force on Assessment of Diagnostic and Therapeutic Cardiovascular Procedures(Committee on Radionuclid Imaging) developed in Collaboration with the American Society of Nuclear Kardiology. JACC. 1995;25:521-47.
- Nuclear Medicine in Clinical Diagnosis and Treatment (ed: I. P. C. Murray, and P. J. Ell). Churchill-Livingstone, 1998.
- Nuclear Cardiac Imaging: Principles and Applications (ed: A. Iskandrian and MS Verani). F. A. Davis Company. 1996. Philadelphia, PA 19103.
A pozitronemissziós tomográfia (PET) szerepe a kardiológiában (dr. Szilvási István)
- Bax, J. J., Wijns, W., Cornel, J. H. et al.: Accuracy of currently available techniques for prediction of functional recovery after revascularization in patients with left ventricular dysfunction due to chronic coronary aretery disease: comparison of pooled data. JACC. 1997;30:1451-60.
- Di Carli, M. F., Asgarzadie, F., Schelbert, H. L. et al.: Quantitative relation between myocardial viability and improvement of heart failure symptoms after revascularization in patients with ischemic cardiomyopathy. Circulation. 1995;92:3436-44.
- Vom Dahl, J., Altehoefer, C., Sheehan, F. H. et al.: Recovery of regional left ventricular dysfunction after coronary revascularization. Impact of myocardial viability assessed by nuclear imaging and vessel patency at follow-up angiography. JACC. 1996;28:948-958.
- Schwaiger, M., Melin, J.: Cardiological applications of nuclear medicine. Lancet. 1999;354:661-666.
- Walsh, J. F., Gropler, R. J.: Positron emission tomography of the cardiovascular system. In: Nuclear medicine (Eds.: Henkin RE, Boles MA, Dillehay GL ea), Mosby, St. Louis. 1996:773-797.





