Állásfoglalás és ajánlás a rhinitis diagnosztikájához és kezeléséhez
• Fül-orr-gégészeti Szakmai Kollégium, Tüdőgyógyászati Szakmai Kollégium •
Definíció
A rhinitis az orrnyálkahártya gyulladása, amely klinikailag akkor állapítható meg, ha a tüsszögés, orrviszketés, orrfolyás, gátolt orrlégzés közül legalább két tünet napi rendszerességgel, fél-egy órán át megfigyelhető. Tágabb értelmezésben az átlag napi négynél több orrfúvás és/vagy tüsszögés rhinitisre utalhat.
Csoportosítás
Fertőzéses
- Virális
- Bakteriális
- Specifikus
- Egyéb
Allergiás
- Intermittáló (a tünetek időtartama rövidebb mint 4 hét, illetve 4 nap/hét)
- Szezonális allergiás rhinitis (SAR) - szénanátha, pollenosis
- Perzisztáló (a tünetek időtartama több mint 4 hét, illetve 4 nap/hét)
- Perennialis (nem szezonális, perzisztáló) allergiás rhinitis (PAR)
Egyéb etiológia
- Idiopathiás
- Nem allergiás rhinitis eozinofil szindrómával (NARES)
- Vazomotoros rhinitis
- Hormonális
- Foglalkozási (allergiás és nem allergiás)
- Környezeti
- Élelmiszer által kiváltott
- Gyógyszer által kiváltott
- Atrófiás
- Pszichogén
- Gastrooesophagealis reflux
A rhinitis típusai
Fertőzéses eredetű rhinitis
Az akut rhinitis általában banális vírusos betegség, mely spontán, illetve tüneti kezelés hatására gyorsan, legtöbbször 7-10 napon belül gyógyul. Profúz vizes orrfolyás, tüsszögés, gátolt orrlégzés a legjellegzetesebb tünetek. A lehetséges kórokozók: rhino-, adeno-, influenza- és parainfluenza-, ECHO-, RS-, Coxsackie- és reovírus. Leggyakoribb a rhinovirus által okozott fertőzés. Másodlagos bakteriális fertőzés esetén - legtöbbször 7 nap után - a tünetek elhúzódnak, az orrfolyás purulenssé válik. A krónikus rhinitist majdnem minden esetben baktériumok okozzák, illetve tartják fenn: Haemophilus influenzae, Streptococcus pneumoniae és pyogenes, Moraxella catarrhalis. Jellemző a tartósan gátolt orrlégzés, gennyes orrfolyás és szaglászavar. Bizonyos esetekben - szövődményként - orrmelléküreg-gyulladás (rhinosinusitis) társulhat hozzá, amely fejfájással és arctáji feszítő érzéssel járhat. Seromucosus vagy gennyes középfülgyulladás szintén társulhat az infekciós eredetű rhinitishez. A specifikus fertőzések közül a rhinoscleroma (Klebsiella rhinoscleromatis) viszonylag gyakrabban, többségük azonban Magyarországon már csak elvétve fordul elő (tbc, luesz, lepra, malleus, parazitás). A mikotikus eredetű rhinosinusitisek (leggyakrabban Aspergillus fumigatus) napjaink rinológiai gyakorlatában növekvő incidenciát mutatnak, ezért feltétlenül gondolni kell rá. Ezt a formát allergiás és/vagy eozinofil típusú gyulladás jellemzi, amelyet a nyákban előforduló gombaantigének váltanak ki. Az invazív forma magas lázzal jár, és általában immunkomprimált betegeknél fordul elő.
Allergiás rhinitis
Szezonális (intermittáló) allergiás rhinitis (pollenosis, szénanátha)
Az ismert vezető klinikai „triászt” - vizes orrfolyás, tüsszögés, orrdugulás - igen gyakran kísérik szemtünetek (rhinoconjunctivitis allergica) viszketés, könnyezés, periorbitalis ödéma formájában, valamint orr- és torokviszketés. Gyakori a szénanátha és a különböző súlyosságú asthma bronchiale (20%, Smith 1983) együttes előfordulása. Esetenként fáradtság, fejfájás, a koncentrálóképesség csökkenése egészíthetik ki a tüneteket. A panaszok súlyossági foka erősen változó az enyhétől a munkaképesség-csökkenésig.
A szezonális allergiás rhinitis kiváltó okai különböző virágporok (pollenek) és gombaspórák lehetnek. A nagy tömegben alacsony fajsúlyú polleneket termelő, szélporozta növények jelentős számú allergiás egyénnél váltanak ki tüneteket (Thommen-szabály). A szélporozta növények szfirikus pollenszemcséi kb. 15-20 μm nagyságúak. Ezek a pollenek száraz, szeles időben nagy mennyiségben jutnak el távolabbra is, és származási helyüktől igen messze is tömeges megbetegedést váltanak ki. A magyarországi éghajlati viszonyok között az allergiás szezon - kedvező időjárás esetén - már február-március táján elkezdődhet a kora tavasszal virágzó fák (mogyoró, nyír, éger, kőris) pollenjei révén. Hazánkban jelentősebb azonban az április végétől júliusig tartó fűszezon, amikor a füvek (komócsin- és perjefélék, csenkesz, ebír stb.) és az egyes gabonafajták (rozs, kukorica) már tartósabb és klinikailag súlyosabb tüneteket váltanak ki. A gyomok (ürömfélék, útifű, parlagfű, csalán stb.) augusztustól szeptember-októberig pollinálnak, és tartják fenn az allergiás szezont. Utóbbiak közül Magyarországon a parlagfű kiemelten súlyos problémát jelent, mivel - kisebb kivételektől eltekintve - az egész ország területe nagymértékben fertőzött. Nagy antigenitású, kis tömegű pollenjei milliárdszámra szabadulnak ki összetett, fűzérszerűen elhelyezkedő fészkes virágaiból, és így a szezonban az ország területének túlnyomó részén igen magas a parlagfűpollen-koncentráció a levegőben. Júliustól októberig a különböző gombaspórák (Alternaria, Cladosporium) légköri koncentrációja is általában elég magas ahhoz, hogy allergiás tüneteket váltson ki a megfelelő egyénben.
A légköri pollenkoncentráció jól mérhető az ún. pollencsapdák segítségével. A pollenszám folyamatos regisztrációja segíthet a betegeknek a pollenszezon indulásának előrejelzésében, és ezáltal a szükséges preventív gyógyszerek szezon előtti alkalmazásában. A pollenszám későbbi - szezon alatti - ismerete igen hasznos segítség mind a betegek, mind a kezelőorvos számára. Mint ismeretes, a légköri pollenkoncentráció és az egyes betegek tünetei/panaszai között nincs egyenes összefüggés, mivel utóbbiakat az időjárási viszonyok (szél, esős és napsütéses órák száma, felhőzet, hőmérséklet) jelentős mértékben befolyásolják.
A pollen- és az allergiás tüneti pontszámok egybevetése nagy segítséget jelenthet a gyógyszeres és/vagy tudományos kísérletek értékelésében. Hazánkban regionálisan és Budapesten is több pollencsapda működik.
Bizonyos élelmiszerek és pollenek között keresztreakciók fordulhatnak elő: parlagfűérzékeny betegeknél allergiás tüneteket provokálhat a dinnye és a banán, fekete üröm esetében a zeller és néhány fűszer, nyírfapollen-allergiásoknál pedig alma, cseresznye, mogyoró és őszibarack (Ortolani et al. 1988).
Perennialis vagy perzisztáló (nem szezonális) allergiás rhinitis
A tünetek hasonlóak, mint a szezonális formában, azzal a különbséggel, hogy általában a gátolt orrlégzés áll előtérben, és szemtünetekkel csak elvétve találkozhatunk. A náthás panaszok - az allergénexpozícióval párhuzamosan - gyakran intermittáló jellegűek, és kb. az esetek egyharmadában pollenosissal is kombinálódnak. A leggyakoribb allergének a háziporatkák (Dermatophagoides pteronyssinus és farinae - faeces), állati szőrök, hám- és testnedvek (macska, kutya, nyúl stb.) és a gombaspórák. Ritkábban élelmiszerek, csótány (faeces és nyál) és foglalkozási allergének is okozhatnak perennialis/perzisztáló tüneteket. Az atkák és a gombák (Aspergillus, Mucor, Penicillium) párás, meleg környezetben szaporodnak jobban, ezért ilyen környezetben számuk ugrásszerűen megnő. Az atka ürülékének beszáradt maradványai még hosszú ideig megmaradnak, és időről időre a levegőbe jutnak. A gombaspórák kedvelik az eldugott, nedves, rosszul szellőző helyiségeket, fürdőszobák nedves sarkait, radiátorok, hűtőszekrények, légkondicionálók, egyes élelmiszerek felületét.
Egyéb etiológia
Idiopathiás rhinitis
Tartósan gátolt orrlégzés, változó mértékű orrváladékozás (beleértve a posztnazális tapadós váladékcsorgást) jellemzi. Gyakori panasz a környezeti ingerekre adott fokozott válasz, de - szemtünetek nélküli - szénanáthát utánzó forma, illetve időskori profúz vizes orrfolyás (old man's drip) is előfordul. Ez a rhinitisforma ritkábban ugyan, de gyermek- és serdülőkorban is előfordul. E betegcsoport kezelése sokszor nehézségekbe ütközik, és gyakran találkozunk antibiotikumokkal és lokális vasoconstrictor tartalmú orrcseppekkel „tartósan félrekezelt”, pszichés és emocionális zavarokkal jelentkező beteggel.
Nem allergiás rhinitis eozinofil szindrómával (NARES)
Az idiopathiás rhinitis egyik változatára - az allergiatesztek negativitása mellett - az orrváladék kifejezett eozinofíliája jellemző (NARES - Non-allergic Rhinitis with Eosinophilia Syndrome; Jacobs 1987). Az eozinofil sejtes gyulladásban általában jellemző, hogy a szteroidok hatékonyan befolyásolják a tüneteket. Az orrtükri kép nem jellegzetes, az orrkagylók duzzadtak, a beteg gátolt orrlégzést és - gyakran - tapadós orrgarati váladékcsorgást panaszol.
Vazomotoros rhinitis
Multifaktoriális etiológiájú rhinitis, amelyben az orrnyálkahártya vegetatív beidegzésének zavarából erednek a tünetek. Gyakran hasonló panaszokat okoz, mint a szénanátha. Az orrtükri kép szintén nem jellegzetes, de nem ritka, hogy az alsó orrkagylók lividek, duzzadtak és nagyobb mennyiségű vizes orrváladék is látható. Számtalan külső és belső inger válthatja ki és tarthatja fenn a tüneteket.
Exogén extranasalis irritáció:
- füst, por, gőz, gáz;
- kemikáliák, szerves oldószerek, parfümök;
- légszennyező anyagok;
- formaldehid, ragasztóanyagok.
Exogén intranasalis irritáció:
- orrsövénytövis, -léc, -ferdülés;
- góc (sinusitis, adenoiditis);
- ganglionitis (Sluder-, Charlin-szindróma);
- axonreflex.
Endogén
- stressz, neurózis;
- hormonális változások (klimax, endokrin betegségek);
- anyagcsere-betegségek;
- gyógyszerek;
- paraszimpatikus diszfunkció;
- aszpirin intolerancia.
Hormonális rhinitis
Az ösztrogénhormonról régebben ismeretes (Mortimer 1937; Watson-Williams 1952), hogy befolyással van az egészséges orrnyálkahártyára. Az emberi élet bizonyos fiziológiás változásai kapcsán - pubertás, terhesség, szexuális izgalom (honey-moon rhinitis), menstruációs ciklus - változó mértékű rhinitises panaszok (gátolt orrlégzés, orrfolyás, tüsszögés) figyelhetők meg. Ugyancsak enyhébb tünetek észlelhetők néhány orális fogamzásgátlót alkalmazó (Ammar-Kohdja 1938; Schiff 1968) - egyébként egészséges - nőnél. Chalon (1971) a menstruációs ciklussal összefüggésbe hozható ciklikus citomorfológiai változásokat észlelt fiatal nők felső légúti csillószőrös hengerhámjában. Feltételezhetően a megemelkedett szérumösztrogénszinttel is összefüggésbe hozható a bizonyos terheseknél kialakuló súlyos rhinitis, illetve sinusitis (Mohun 1943; Sorri 1980). Csökkent ösztrogén-, illetve nemihormon-szint lehet a háttérben az „igazi” atrófiás rhinitisben (Blaisdell 1938), valamint - a hasonló tünetekkel járó - hypopituitarismusban, hypogonadismusban és menopauzában.
Foglalkozási rhinitis
Jellegzetesen allergiás vagy atípusos nem allergiás rhinitis formájában jelentkezhet. Előbbi elsősorban az állatokkal foglalkozók (pl. kutya, macska, patkány, nyúl, egér, tengerimalac, tehén), a mezőgazdaságban és a malomiparban (rozs, búza, gabona, liszt, atka, gombaspórák, állatok), textiliparban (pamut, gyapjú stb.), valamint a vegyiparban (enzimek, savanhidridek, izocianát, platinasók) dolgozók körében fordul elő. A szerves oldószerek, formaldehid, illetve több, a vegyiparban alkalmazott anyag jellegzetesen irritatív hatásmechanizmussal nem allergiás asztmát és rhinitist provokálhatnak.
Környezeti ártalmak által kiváltott rhinitis
Modern világunkban a légi és gépjárművekből származó kipufogógázok, a különböző gyárak és kőolaj-finomítók égéstermékei, a CFC (klór-fluorokarbon)-gázzal hajtott palackok, a cigarettafüst és egyéb lebegő szerves részecskék folyamatosan szennyezik a levegőt. A „régi” (redukáló) típusú szennyeződések (pl. kén-oxidok, füst, korom) elsősorban nem specifikus alsó légúti megbetegedésekkel hozhatók összefüggésbe, míg a „modern” (oxidáló típusú) városi légszennyező anyagok (pl. nitrogén-dioxid, ózon) felszaporodása az allergiás légúti betegségek incidenciájának növekedéséhez vezetett. Ez utóbbi magyarázatára több elmélet is született az elmúlt években: fokozott adhéziósmolekula-expresszió a felső légúti nyálkahártyában, az antigének antigenitásának fokozódása, valamint a felső légúti nyálkahártya-gyulladás okozta fokozott sensitisatio és permeabilitás. A tünetek mértéke függ a szennyeződés koncentrációjától, a behatás időtartamától, a szellőzés mértékétől és az orrüregben megtapadt részecskék számától. Az ózon, nitrogén-oxidok és a hideg levegő az orrnyálkahártya gyulladását okozzák (Bascom 1993). Davies (1997) munkacsoportja in vitro vizsgálatokkal megállapította, hogy N02, illetve ózon hatására fokozódik a felső légúti nyálkahártya epithelsejtjeiben a különféle proinflammatoricus mediátorok (citokinek, adhéziós molekulák) szintézise (14). Az is egyértelműen kiderült a fenti vizsgálatok során, hogy az allergiás egyén epithelsejtjeiből szignifikáns mértékben több citokin és kemokin szabadul fel (GM-CSF, IL-6 és 8, RANTES), valamint ugyanilyen mértékben fokozott az epithelsejtekben az ICAM-1 expressziója. A nagyon hideg levegőre érzékeny embereknél az orrnyálkahártya párásítási kapacitása csökkent, és a következményesen emelkedett ozmolaritás mastocytaaktivációt provokál (Togias 1993). Az ún. föld közeli ózon (03) lebegő szerves részecskék, nitrogén-oxidok és napfény kölcsönhatásaiból képződik. A por és a cigarettafüst tisztán irritatív hatásúak, előbbi nem befolyásolja sem a mucociliaris transzporttevékenységet (MCT), sem a nazális rezisztenciát (NR). S02 hatására az MCT csökken, az NR nő. A formaldehid irritáns, metaplasiát okozhat. Az intenzív napsütés kiváltotta reflexes tüsszögés és orrfolyás szintén irritatív, neurogén mechanizmussal magyarázható. A kísérletesen létrehozott extrém hőmérséklet-változások az NR emelkedésével járnak, a száraz levegő nem befolyásolja. Sick-building-szindróma részeként szintén találkozhatunk gátolt orrlégzéssel, esetleg rhinitises panaszokkal, amelynek hátterében többféle ok is valószínűsíthető: légkondicionáló, fénymásoló gép, szellőzetlen helyiség, ragasztott, porfogó padló és tapéta.
Élelmiszer által kiváltott rhinitis
Az élelmiszer-intoleranciában szenvedő betegeknek - a több szervet érintő panaszok mellett - rhinitises tünetei is lehetnek, azonban ezek csak elvétve jelentkeznek önállóan. Az élelmiszer-adalékokkal és konzerválószerekkel összefüggésben bőr- és emésztőszervi elváltozások esetenként megfigyelhetők, az izolált rhinitis ellenben ritka. Gyanú esetén a konvencionális allergiavizsgálatokat minden esetben kettős-vak, placebo-kontrollált élelmiszer-provokációs vizsgálatnak kell követnie az allergiás eredet, illetve az intolerancia megállapítására. Az inhalatív úton szenzitizált pollenallergiás betegnél - a keresztreakcióknak köszönhetően - bizonyos gyümölcsök, zöldségek és fűszerek az orális bevitelt követően száj- és garatelváltozásokat okozhatnak (pl. orális allergiaszindróma, Quincke-ödéma). Az élelmiszer-allergének országonként, illetve földrészenként nagy eltéréseket mutathatnak: az ismertebb allergének (hús, tej, tojás, csokoládé, dió, zöldség-, gyümölcsfélék) mellett pl. a Távol-Keleten a hal- és rákfajták jelentős allergénforrások. A forró, fűszeres ételek - nem allergiás mechanizmussal - direkt neurogén úton válthatnak ki rhinitises tüneteket.
Gyógyszer által kiváltott rhinitis
A lokális nazális vasoconstrictor tartalmú készítmények - α1-agonista sympathomimeticus aminok: efedrin, pszeudoefedrin, fenilefrin, illetve α2-agonista imidazolinszármazékok: oxi- és xilometazolin, nafazolin - kb. 7-10 napot meghaladó folyamatos alkalmazása során alakul ki a „rhinitis medicamentosa”. Jellemző tünetei a következők: „rebound” effektus, azaz a vasoconstrictor hatás megszűnte után észlelhető még kifejezettebb, tartós orrdugulás; nazális hiperreaktivitás; tolerancia, azaz a vasoconstrictor hatás mértékének és időtartamának csökkenése. A rebound orrdugulás független a dózistól, azaz az előírt adagtól mindkét irányba eltérve (napi egyszeri vagy az előírt adag 3-szorosa) is kialakul, és a vasoconstrictor elhagyását követően 2-3 nappal mérséklődik. A hiperreaktivitás dózisfüggő, és az alkalmazás felfüggesztését követően még több hétig (1-2 hónapig) kimutatható (Graf 1994). A tolerancia miatt hamar addikció (hozzászokás) lép fel, amelynek következtében sokszor extrém (többéves) időtartamú alkalmazás is megfigyelhető. Patofiziológiája részleteiben ismeretlen, szövettani képében kompenzatorikus vasodilatatio és interszticiális ödéma látható. A tünetek súlyossági foka összefüggésben állhat az alkalmazott készítmény kémiai szerkezetével (a szelektív α1-agonista aminok csak az ún. capacitance-erek constrictióját váltják ki, szöveti ischaemia nélkül) de hangsúlyozandó, hogy a rhinitis medicamentosa α1- és α2-receptor agonista vegyület abúzusa mellett egyaránt kialakul (Osguthorpe és Reed 1987). A vizes oldatokat konzerváló benzalkonium-klorid majdnem mindegyik készítményben megtalálható, ami egyértelműen súlyosbítja a kialakult klinikai képet. In vitro gátló hatást fejt ki a csillószőrök, illetve a granulocyták kemotaktikus és fagocitaaktivitására (Batts 1989). Az önmagában - benzalkonium-klorid nélkül - adagolt vasoconstrictor oldatok is létrehozzák a rhinitis medicamentosát.
A következő orális gyógyszerekkel kapcsolatosan írtak eddig le nazális tüneteket (elsősorban gátolt orrlégzés, száraz orrnyálkahártya): vérnyomáscsökkentők (reszerpin, guanethidin, phentolamin, metildopa, prazosin, béta-blokkolók, ACE-gátlók), acetilszalicilsav és egyéb nem szteroid gyulladáscsökkentők (NSAID-csoport), intraocularis béta-blokkolók, brómkriptin.
Atrófiás rhinitis
A primer atrófiás rhinitis mint ozaena ismeretes, és általában a Klebsiella ozaenae kimutatható az orrváladékból vagy az orrnyálkahártyából. A primer esetekben hormonális ok is keresendő: hypopituitarismus, hypogonadismus, menopauza, egyéb ösztrogénhormonszint-csökkenés. Krónikus infekció, trofikus zavarok, iatrogén sebészi ártalom, sérülés, irradiáció, egyéb nazális trauma kapcsán másodlagos atrófiás rhinitis (pl. rhinitis sicca anterior) fejlődhet ki, amely nemegyszer orrsövény-perforációhoz vezet. Jellemző a gátolt orrlégzés, pörkképződés, kisebb vérzések, ozaenában foetor.
Pszichogén rhinitis
Stresszel, neurózissal és egyéb emocionális behatással kapcsolatosan akut vagy tartós rhinitises tünetek jelentkezhetnek. Ezekkel kapcsolatban megfigyelhető, hogy az „orrbetegség” - leggyakrabban a gátolt orrlégzés - bizonyos pszichovegetatív alapprobléma vagy pszichiátriai betegség lokális megnyilvánulása. Orrműtéte(ke)n átesett betegeknél posztoperatív nazális szenzációk, fóbiák léphetnek fel, amelyek hátterében vélt vagy valós tünetek, kisebb mértékű iatrogén ártalmak állhatnak. Az sem ritka, hogy az idiopathiás rhinitisben szenvedő, sok orvost és rendelőt eredménytelenül látogató betegnél „másodlagosan” alakulnak ki a neurotikus jelek, melyekről később igen nehéz eldönteni, hogy elsődlegesek vagy másodlagosak. Előfordulhat, hogy diagnózis hiányában ebbe a csoportba kerülnek primer receptor hypo- vagy anesztéziás betegek, akiknél a csökkent vagy túlérzékeny nazális afferentatio (munkahelyi, környezeti ártalmak, dohányzás) tehető felelőssé a panaszok kialakulásáért.
A rhinitis fokozatai
A fokozatok meghatározásánál döntőek az életminőség mutatói, a tünetek erőssége, szervi megjelenése és időtartama. Előfordulhat, hogy a fokozatok közötti átmenet nem egyértelmű, és egy napon belül is változik.
I. Enyhe
Kevés, a beteg számára nem terhelő, általában napi egy-két óránál rövidebb ideig tartó, döntően korai fázisú, irritációs tünetek - viszketés, tüsszögés, orrfolyás - jellemzik. Betegségtudat kialakul ugyan, de sokszor kezelés nélkül is tolerálható. Az alvást és a napi aktivitásokat nem befolyásolja.
II. Közepes
Több, a beteg számára zavaró, általában naponta két óránál tovább tartó, döntően gátolt orrlégzéssel járó tünetek jellemzik. A napi tevékenységet és az alvást jelentősen zavarják, ezért kifejezett betegségtudat és életminőség-romlás alakul ki.
III. Súlyos
Folyamatosan fennálló, kínzó tünetek, amelyek több szervet is érintenek. Gyakori a bronchialis hiperreaktivitás miatt fellépő köhögés és átmeneti dyspnoe. A napi tevékenységet és az alvást lehetetlenné teszik, ezért komoly betegségtudat és életminőség-romlás alakul ki.
Az Európai Akadémia (EAACI) ajánlásában hasonló felosztást találhatunk, míg az ARIA dokumentumban a közepes-súlyos fokozatot összevonták.
Az orr és a melléküregek élettani szerepe
Orrüreg:
- a felső légutak proximalis része;
- szaglószerv.
Az orrüregek a vestibulum nasiból nyílnak, amelyeket többmagsoros, csillószőrös hengerhám borít. Az orrmelléküregekben hasonló a hám, amely a természetes szájadékokon keresztül összeköttetésben van az orrüregi nyálkahártyával. Az orrüregeken keresztül jut el a szükséges levegőmennyiség az alsó légutakba. Az orrnyálkahártya funkciói:
- a belégzett levegő felmelegítése;
- a belégzett levegő párásítása;
- a belégzett levegő szűrése és tisztítása.
A 4,5 μm-nél nagyobb részecskék 85%-a az orrból nem jut tovább. Ezzel szemben az 1 mikronnál kisebb szennyeződések kevesebb mint 5%-a akad csak fenn az orrnyálkahártyán.
Az orrváladék a nyálkahártya felszínén nyákfilmet alkot, amelynek felül vékonyabb, gél fázisú, alatta vastagabb, szól fázisú rétege van. A csillószőrök mozgása, illetve csapásai következtében a felületi, gél fázisú nyákszőnyeg lassan, a vestibulumtól az orrgarat felé halad. Megfigyelések szerint az alsó orrkagyló elülső pólusától 10-20 perc alatt jut el a nyákfilm a choanáig. Az orrgaratból a mesopharynx felé távozik a váladék, ahonnan a nyelőmozgások távolítják el. A melléküregekben a természetes ostiumtól legtávolabb eső ponttól az ostium irányába konvergálva halad a transzport, majd az ostiumon át az orrüregbe jut a nyák.
Az orrüreg nyálkahártyájának hátul-felül található része a regio olfactoria, amely a szaglás szerve. A szaglásra jellemző:
- az analitikus képtelenség;
- a definitív pontatlanság;
- a gyors fáradékonyság és regenerációs készség.
Orrmelléküregek
Az orrüreg a melléküregekkel együtt rezonátorüregként működik a beszéd-, ének- és az artikulálatlan hangok formálásában.
Az orrmelléküregek az orrüreggel összeköttetésben álló, nyálkahártyával bélelt, zárt, páros üregek (arc-, homloküreg, iköböl és a rostasejtek).
A rhinitis epidemiológiája
Az allergiás nátha prevalenciájáról pontos adatokhoz jutni nehéz. Sokszor nincs éles határ a „már betegség” és a „még nem betegség” között, az allergiás nátha tünetei egy betegnél is igen változó súlyosságúak, illetve a betegek csak egy része fordul orvoshoz. Az orvoshoz fordulókról nincs központi nyilvántartás, nem kötelezően bejelentendő betegség. Korábban nem volt nemzetközileg elfogadott standard módszer a prevalenciavizsgálatok végzésére, így az egyes tanulmányok adatait nehezen lehetett összehasonlítani. Az első nemzetközileg összehangolt vizsgálat az ISAAC (International Study of Asthma and Allergies in Childhood). Az ISAAC 1995-től 56 országban, 155 centrum részvételével egységes epidemiológiai felmérést, adatgyűjtést végez. Ehhez 2003-tól Magyarország is csatlakozott (Stachan 1997). A szezonális rhinitis allergica jár a legegyértelműbb tünetekkel, és a legkönnyebben diagnosztizálható, így a legtöbb prevalenciavizsgálat e betegség gyakoriságát határozta meg. Ennek megfelelően a szénanátha gyakorisága Európában 5-20% közötti (Balogh 2003; Bittera 1990, 2003; Fleming 1987; Weeke 1987; Wüthrich 1986, 1995). A perennialis allergiás és perennialis nem al1ergiás nátha prevalenciájáról csak kevés irodalmi adat áll rendelkezésre. Sibbald és Rink (1991) 1988-ban Londonban a 16-65 évesek (n=7702) között kérdőíves módszerrel és randomizált utánvizsgálattal a rhinitis prevalenciáját 24%-osnak találta: 3% szezonális, 13% perennialis és 8% kevert. Míg a szezonális rhinitises betegek közel 80%-ánál bizonyítható volt az allergiás eredet, addig a perennialis rhinitisesek felének negatív lett a bőrtesztje. Magyarországon Bittera és Gyurkovits (1990) 1987-ben 903, 6-14 éves gyermek között a rhinitis allergica valószínű prevalenciáját 8,1%-nak találta. 1997-ben, majd 2002-ben azonos körülmények között megismételték a vizsgálatot. Ekkor a gyermekkori rhinitis allergica prevalenciáját 14%, illetve 17%-nak találták (Bittera 2003).
Balogh és munkatársai adatai Budapesten 2002-ben, teljes populációra vetítve hasonló eredményt mutattak (Balogh 2003). Kadocsa (1994) 1993-ban kérdőívvel és utánvizsgálattal megállapította, hogy a rhinitis prevalenciája Szegeden az 5-75 évesek között 11%, aminek egyharmada nem allergiás perennialis nátha. Az atópiások nagy része szezonális allergiás náthában szenved (mezőgazdasági terület, sok parlagfű). Epidemiológiai vizsgálatok bizonyítják, hogy az allergiás rhinitis általában iskoláskorban vagy fiatal felnőttkorban kezdődik (ARIA 2001; Charpin 1988; Kadocsa 1994). Gyermekkorban a fiúknál, felnőttkorban pedig a nőknél gyakoribb (Crouer 1982). A betegség kialakulása, illetve korábbi életkorban való megjelenése szempontjából főként azok veszélyeztetettek, akiknek a családjában atópiás allergiás betegek vannak az első és másodfokú rokonok között (Mezei 1986, 1987).
A csecsemő- és kisdedkorban ekcémás és/vagy asztmás gyerekeknél fokozottan nagy a kockázat a 15-30 éves kor között megjelenő rhinitis allergica betegségre (Settipane 1994). Egyes vizsgálatok szerint a szénanátha gyakrabban fordul elő a tavaszi-nyári hónapokban születettek között (Sibbald 1991).
A szénanátha prevalenciáját magasabbnak találták a városban élőknél, mint a falusiaknál (Peddersen 1981), és a jobb szociális körülmények között élőknél, mint a szegényebbek között (Sibbald 1993). Számos, különböző országból származó tanulmány szerint az utóbbi 20 évben megduplázódott az allergiás nátha prevalenciája (Aberg 1995; Rimpela 1995; Weeke 1992; Bittera 2002), aminek a pontos oka nem ismert. Nem tudni továbbá azt sem, hogy ez ilyen irányban és ütemben fog-e tovább is haladni, vagy csak egy átmeneti jelenséggel állunk szemben. Epidemiológiai vizsgálatok szerint több tényező együtthatása tehető felelőssé e jelenségért. Ezek között kiemelkedő fontosságúak a környezeti tényezők, elsősorban a modern életvitellel - az úgynevezett „nyugati stílusú” életmóddal az utóbbi évtizedekben - együtt járó levegőszennyeződés és annak nagyfokú növekedése, illetve minőségi változása. Ehhez járul az embert körülvevő vegetáció megváltozása (pl. az Európában nem őshonos parlagfű európai elterjedése, a kemizálás, sok gyógyszer fogyasztása, a tápanyagokban előforduló sok mesterséges anyag, dohányzás). E tényezők károsító hatása részben tapasztalati tény, részben kísérletek bizonyítják légúti nyálkahártyát károsító hatásukat, immunrendszerre való káros befolyását stb. (Michel 1992; Weeke 1993). Az utóbbi időben a figyelem középpontjába leginkább az ún. „higiénéelmélet” került, amely szerint a túlságosan steril életkörülmény (közösségbe nem járó gyermek, védőoltások hiánya, kevés testvér) vezetne az allergiás megbetegedések emelkedő számban való kialakulásához (Strachan 2000).
Patomechanizmus
Fertőzéses eredetű rhinitis
A legtöbb rhinovirus és néhány Coxsackie-vírusfajta receptora az orrnyálkahártyában is megtalálható ICAM-1 (Intercellular Adhesion Molecule-1), amely az adhéziós molekulák immunglobulin-családjához tartozik. Vírusos náthában az orrnyálkahártya felszínén és az orrváladékban is megnövekszik a neutrofil granulocyták száma (21), ami tehát nem csak a bakteriális gyulladásra jellemző. Röseler (16) igazolta, hogy a természetes úton szerzett vírusos náthában szenvedő betegek orrmosó folyadékában az IL-1ß, IL-6 és IL-8 szintje megemelkedik. Az IL-1ß fokozza az ICAM-1 és E-Selectin, valamint a neutrofil kemotaktikus hatású IL-8 (régi nevén Neutrophil Activating Peptide, NAP-1) expresszióját. Vírusos náthában a nyálkahártya-neutrofília megjelenéséért a fokozott mennyiségű IL-1 és IL-8 a felelős, amely a vírusos gyulladás része, és nem jelent okvetlenül bakteriális felülfertőzést. Az IL-6 szinergista hatású az IL-1-gyel és a TNF-α-val. A fenti adatok a proinflammatoricus citokinek virális eredetű náthában való szerepét is alátámasztják.
A nyálkahártya ereiben vasodilatatio alakul ki, a kis nyákmirigyek nagy mennyiségű szekrétumot termelnek, és szövetközti ödéma lép fel. A rhinitisszel párhuzamosan legtöbbször conjunctivitis és pharyngitis is zajlik.
Bakteriális rhinitisben nagy mennyiségű neutrofil granulocyta és baktérium látható az orrkenetben. A gennyes gyulladásra általában jellemző laboratóriumi eltérések kimutathatók: gyorsult süllyedés, emelkedett fehérvérsejtszám, CRP és AST, balra tolt vérkép.
Allergiás rhinitis
Allergiás rhinitisben (AR) a mastocyták azonnali típusú, IgE-közvetített aktivációja során felszabaduló mediátorok hatására jellegzetes tünetek lépnek fel. Mind a természetes, mind a nazális allergénprovokációval kiváltott kísérletes formájában két fázis különíthető el: a korai fázis az allergénprovokáció után azonnal jelentkezik, és elsősorban tüsszögés, viszketés, vizes orrfolyás jellemzi, míg a késői fázis - mely általában több óra múlva lép fel, és még két nap után is észlelhető - meghatározó tünete a gátolt orrlégzés. A korai fázis részben a mastocyták és hízósejtek granulumaiban tárolt (hisztamin, triptáz stb.), részben a sejtmembránban előállított (bradikinin, prosztaglandinok [PGD2], leukotriének [LTC4, E4], vérlemezke-aktiváló faktor [PAF]) mediátorok hatására alakul ki. A sejtmembrán telítetlen zsírsavaiból (arachidonsav) szintetizált anyagai mellett az eozinofil sejtek sejtkárosító fehérjéi is fontos szerepet játszanak a késői (szöveti) fázis kialakításában.
Az igen bonyolult interakciók sorában az első lépés az antigén-prezentáció. A T-sejt-rendszer megfelelő receptorok segítségével ismeri fel az antigén-prezentáló sejt (APC) - rendszerint makrofág vagy Langerhans-sejt - által bekebelezett és az MHC (HLA) II. osztályú molekulájához kötött antigént. A makrofágok és az epithelsejtek az antigén-felismerés folyamatában termelt és
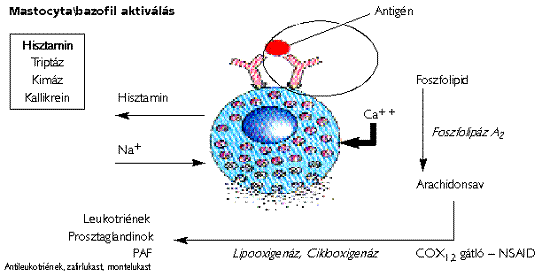 |
kiválasztott proinflammatoricus citokinek (interleukin v. citokin: IL) segítségével serkentik a Th1 és Th2 típusú sejtek differenciálódását és az adhéziós molekulák expresszióját. Az aktivált T-sejtek meghatározó és központi irányító szerepet töltenek be az allergiás gyulladás korai és késői fázisában. A helper T- (CD4+) sejtek irányításával aktiválódott B-sejtekből kialakult plazmasejtek termelik a nagy mennyiségű IgE-molekulákat az atópiás egyénnél, amelyek a korai fázis meghatározó sejtjeit, a mastocytákat szenzitizálják. Ugyancsak a T-sejt-rendszer szabályozza az eozinofil és bazofil sejtek aktivációját, érési folyamatát, szöveti migrációját és élettartamát, ezáltal az allergiás gyulladás késői fázisát. Az allergiás sensitisatiót követő első antigén-találkozáskor genetikailag meghatározott kóros mennyiségű IgE-szintézis indul be az atópiás egyénben. A termelést közvetlenül a citokinrendszer irányítja, az interferon-γ (INF-γ) gátolja, az IL-4 serkenti. Az interleukinek meghatározó fontosságú mediátor molekulák, melyek a gyulladásban részt vevő sejtek közötti „párbeszédet” irányítják és bonyolítják. A helper T-sejteket citokintermelésük alapján két csoportra lehet osztani: Th1 (IL-2, INF-γ) és Th2 típusúakra (IL-4,5,6,10,13). IL-3, GM-CSF (granulocyta-makrofág kolóniastimuláló faktor) és TNF-α mindkét sejttípusban megtalálható.
A T-sejteken kívül a citokinek legfontosabb forrásai a mastocyták, a makrofágok, az epithel- és endothelsejtek. Az ún. „proinflammatoricus” citokinek (IL-1, 8, TNF-α) - melyek az antigén-expozíciót követően szinte azonnal megjelennek - a Tho-sejtek, fibroblastok, endothel- és epithelsejtek aktiválásában vesznek részt. Az IL-1 és -4, valamint a TNF-α az adhéziós molekulák expresszióját fokozzák az endothel- és epithelsejteken (Bachert 1995). A sejtadhéziós molekulák (cell adhesion molecule, CAM) egy komplex molekuláris rendszert képeznek, amely - többek között - szerepet játszik az intercelluláris, a fehérvérsejt-epithelium adhézióban, a szöveti struktúra fenntartásában, a szelektív migrációban, azaz a sejtek egymáshoz kapcsolódásában.
Az epithel- és endothelsejtek már nem tekinthetők pusztán passzív szereplőknek az allergiás gyulladásban; felszínükön adhéziós molekulák expressziója figyelhető meg, és citokintermelésük is jelentős. Az adhéziós kaszkád eredményeképpen a submucosa kitágult ereiben a keringés a sejtek forgásával egy időben lelassul (rolling), és a granulocyták aktivációját követően azok szorosan az endothelsejtekhez tapadnak (adhézió).
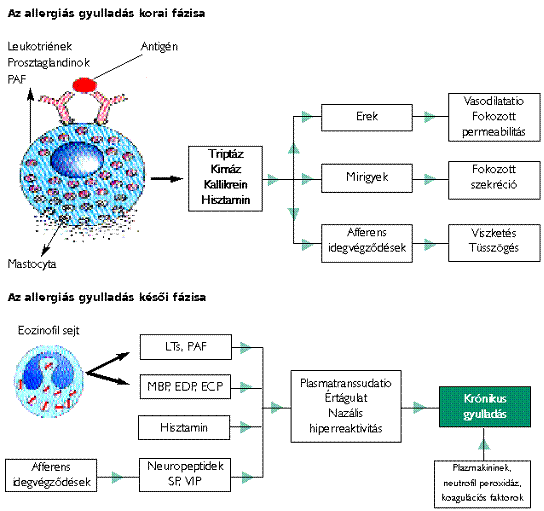 |
Az endothel résein keresztül a megtapadt sejtek átjutnak (migráció) az érfalon a submucosába, majd a mucosába. Az adhéziós rendszer, mediátorok és kemotaktikus faktorok hatására a különböző sejtek a gyulladás helyszínére vándorolnak (szöveti fázis), és belőlük további mediátorok, valamint toxikus anyagok szabadulnak fel. Az IL-3 a mastocyták, az IL-5 az eozinofil sejtek érését, aktivációját, migrációját és élettartam-növekedését befolyásolja és fokozza. Az eozinofil sejtek számos citotoxikus anyag (Major Basic Protein - MBP, Eosinophil Cationic Protein - ECP, Eosinophil Peroxidase, Eosinophil-Derived Neurotoxin) forrásai, melyek direkt sejtkárosító hatásukon keresztül az epithelium desquamatióját, a légutak hiperreaktivitását okozzák. Az ugyancsak e fázisra jellemző interszticiális ödéma és plasmaexsudatio a tartós gyulladás biztos és reprodukálható jelei. Jellemző a mastocyták redisztribúciója, az aktivált gyulladásos sejtek migrációja, a nazális hiperreaktivitás és az ún. priming (telítődés). A gyulladásos sejtek, mediátorok és az exsudatum jelenléte szövettani, valamint az orrmosó folyadék vizsgálatával igazolható. A legújabb tudományos eredmények szerint (Canonica 1997) tünetmentes allergiás rhinitises beteg felső légúti nyálkahártyájának epithelsejtjeiben is fokozott mértékű az adhéziós molekulák expressziója, ami azt sugallja, hogy ne „tüneteket”, hanem a „betegséget” kezeljük. Ez azt jelenti, hogy a folyamatos, preventív terápiát kell előnyben részesíteni a szükség szerinti (on demand) kezelési formával szemben.
Allergénprovokáció
Az allergén dózisától és az egyéni érzékenység fokától függő azonnali válasz - orrfolyás, tüsszögés, viszketés - váltható ki nazális provokációval. A bizonyos százalékban 6-12 óra múlva kifejlődő késői fázisban a gátolt orrlégzés és a specifikus hiperreaktivitás dominál. Az orrmosó folyadékban mindkét fázis során megnövekedett mediátortartalom (Naclerio 1985), valamint - főleg a késői fázisban - nagyobb eozinofil- és bazofilsejt-szám mutatható ki. A specifikus allergénprovokáció kiválóan alkalmas a patomechanizmus ismeretlen tényezőinek kísérletes elemzésére; pl. a mosófolyadék in situ hibridizációs vizsgálatával a meghatározó citokinek szerepe igazolható (Durham 1992), míg citológiai és szövettani eszközökkel a sejtes infiltráció vizsgálható. Aspecifikus provokáció során (pl. 2 mg/ml hisztamin) a nem specifikus nazális hiperreaktivitás (idiopathiás rhinitis) kimutatható, és objektív eszközökkel - pl. rinomanométer, akusztikus rinométer, rinosztereométer stb. - mérhető.
Nazális telítődés (priming)
Bizonyos mennyiségű - természetes, illetve provokációs - pollenterhelést követően az orrnyálkahártya „telítődik”, azaz a pozitív válasz kiváltásához szükséges pollenmennyiség jelentősen csökken (Connell 1969). A jelenség az első terhelést követő gyulladásos sejtinfiltrációnak tulajdonítható (Bentley 1992). Egy adott pollenszezonban telítődött orrnyálkahártya a későbbiekben nagyságrendekkel kisebb specifikus (allergén) vagy nem specifikus (pl. légköri szennyeződés, cigarettafüst) behatásokra kifejezett tünetekkel reagálhat.
Nem allergiás rhinitis
A nem allergiás típusú rhinitisről lényegesen kevesebb tudományos adat áll rendelkezésünkre. Sok esetben feltételezhető, illetve kimutatható a kiváltó ok, az idiopathiás formában azonban teljességgel ismeretlen. Bizonyos légköri ágensek és behatások irritatív jellegüknél fogva (pl. por, cigarettafüst), mások orrnyálkahártya-gyulladás kiváltásával (pl. nitrogén-oxidok, ózon, hideg levegő) tartanak fenn rhinitises panaszokat. A gyulladás jelenléte kimutatható és bizonyítható, ha az orrmosó folyadékban emelkedett az albumin- és neuromediátor-tartalom, valamint a gyulladásos sejtek (neutrofil és eozinofil granulocyta) száma. Idiopathiás formában az ún. axonreflex mechanizmus feltételezhető: az orrnyálkahártya receptorainak és afferens rostjainak mediátorok (mindenekelőtt hisztamin), lokális tényezők (pl. septum-spina), illetve krónikus környezeti ártalmak általi ingerlése axonreflex kiváltásával neuromediátorok (pl. Substance-P, SP; Vasoactive Intestinal Polypeptide, VIP) felszabadulásához vezethet. Ezen anyagok - elsősorban az SP - a mastocyták degranulációját provokálják, és maguk is erősen toxikusak (vasodilatatiót, transsudatiót, szekréciót, simaizom-kontrakciót váltanak ki). E mechanizmusok nem allergiás és allergiás rhinitisben egyaránt feltételezhetők. Az esetek nagy részében fennálló nazális hiperreaktivitás kvalitatív és kvantitatív módon is kimutatható, pl. aspecifikus nazális hisztaminprovokációs vizsgálattal.
A rhinitis diagnosztikája
Alapvizsgálatok
- Anamnézis
- Bőrpróba
- Fül-orr-gégészeti vizsgálat: rinoszkópia
Kiegészítő vizsgálatok
- Allergológiai vizsgálatok:
- szérum össz IgE, specifikus IgE;
- nazális provokációs vizsgálat.
- Orrváladék-vizsgálat:
- bakteriológia;
- citológia;
- IgE-vizsgálat;
- albumintartalom.
- Orrendoszkópia:
- merev endoszkóp;
- flexibilis endoszkóp.
- Képalkotó vizsgálatok:
- szummációs orrmelléküreg-felvételek;
- CT;
- MRI.
- Nazális légzésfunkciós vizsgálatok:
- nazális csúcsáramlásmérés;
- rinomanometria.
- Akusztikus rinometria
- Mucociliaris rendszer vizsgálatai
- Funkcionális:
- nazális mucociliaris clearance (NMC);
- ciliaris csapásszám (ciliary beat frequency = CBF);
- nyálka mennyiségi és minőségi vizsgálata.
- Morfológiai:
- fénymikroszkópos;
- elektronmikroszkópos vizsgálat (scanning, transzmissziós).
- Szövettani vizsgálat
- Szaglásvizsgálat:
- szagfelismerési próba;
- küszöbvizsgálat;
- adaptációs teszt.
- Egyéb vizsgálatok
Anamnézis
A rhinitis kivizsgálásában első és legfontosabb lépés a gondos anamnézisfelvétel. A betegre vonatkozó általános anamnézisfelvételen túl ki kell térni a tünetek megjelenésének gyakoriságára, szezonalitására, a korábbi életkorban előforduló allergiás betegségekre (ételallergia, atópiás dermatitis, asztma); a részletes családi, környezeti és foglalkozási körülményekre. A tünetek részletes elemzése szintén alapvető fontosságú.
Bőrpróba
A bőrpróbák a bőrbe juttatott allergén és a bőr hízósejtjein lévő specifikus IgE által kiváltott azonnali reakción alapulnak. Az IgE közvetítette allergiás betegségek diagnosztizálására két bőrpróbamódszert alkalmazhatunk: a prick-tesztet (SPT) vagy az intrakután tesztet. A prick-teszt során az alkar hajlító oldalán, a bőr felszínére juttatott vizsgálandó allergénen keresztül pontszerű hámsérülést ejtünk a bőr felszínes hámrétegén. Az intrakután teszt során az allergén vizes oldatát juttatjuk a hám felszínes rétegei közé. A prick-teszt egyszerű, megbízható, gyors, olcsó, lényegében fájdalom nélküli vizsgálat, specificitása nagy, az anafilaxiás reakció veszélye minimális, ezért a legáltalánosabban alkalmazott eljárás az IgE közvetítette betegségek megállapítására.
Az azonnali reakció során a karcolás körül csalángöb és bőrpír mutatkozik, amely az allergénre 15-20, a hisztaminra 10, a kodein-foszfátra 8-12 perc múlva látható. Ha a negatív kontrollként használt anyagra nincs reakció, akkor pozitív válaszként értékelhető, amennyiben a csalángöb legnagyobb átmérője meghaladja a 3 mm-t. A diagnózis alapját az anamnézissel korreláló pozitív bőrpróba adja.
A reakciókat objektív módon mm-ben kell megadni (a csalángöb két legnagyobb átmérője vagy bőrindex).
Fül-orr-gégészeti fizikális vizsgálat
A vizsgálat a beteg külsejének megtekintésével kezdődik (gátolt orrlégzésre jellemző arc-, ajak- és szájpadformák, duzzadt szemhéjak, belövellt conjunctiva, a szem alatt kékes árkok észlelése).
Rinoszkópia anterior és posterior során - a rhinitis diagnosztizálásán túlmenően - meg kell állapítani az esetleges egyéb rinológiai betegségeket (pl. orrsövényferdülés, orrpolip, rhinosinusitis, alsó orrkagyló-hipertrófia, rhinitis medicamentosa), anatómiai variációkat (pl. concha bullosa, infundibulum variációi stb.) és szövődményeket. Szükség esetén az orr- és melléküregek endoszkópos vizsgálatát is el kell végezni.
Az allergiás rhinitisre a sápadt, duzzadt nyálkahártya és a serosus vagy mucosus váladék jellemző, de tünetmentes beteg esetében ezek a jelek hiányozhatnak. Hasonló nyálkahártyakép nem csak allergiás náthában szenvedő betegnél látható. Az orrtükri kép nem specifikus az allergiás náthára. Otoszkópia során a középfül, a torok vizsgálatakor pedig a garatnyálkahártya érintettségét kell értékelni.
A rhinitis minden formájában szükséges a fül-orr-gégészeti szakvizsgálat. Megállapított diagnózis és megkezdett kezelés esetén is mielőbbi szakvizsgálat indikált. A cél az, hogy megállapítsuk az esetleges szövődményeket és kísérő betegségeket, illetve azok mértékét és az esetleges teendőket. Bizonyos eltérések a helyi, nazális terápiát akadályozhatják vagy lehetetlenné tehetik.
Kiegészítő vizsgálatok
Allergológiai vizsgálatok
A szérum össz IgE-szintjének meghatározása különböző radio- vagy enzimvizsgálatok révén történik. Egészséges ember össz IgE-szintje a születéstől (0-1 kU/l) a serdülőkor végéig növekszik, ezután lassan csökken, és a második-harmadik évtized után nem változik, állandó szintje alakul ki. Felnőttkorban az össz IgE-szintet 100-150 kU/l felett emelkedettnek tartjuk, de klinikai jelentősége csak a több száz kU/l feletti értékeknek van. Az emelkedett össz IgE-szintnek több oka is lehet. Szezonális allergiás náthában szenvedők több mint 50%-ánál az össz IgE-érték nem emelkedett. A szérum össz IgE-szintjének vizsgálatát rhinitisben nem tartjuk elég specifikusnak, gyakorlati haszna korlátozott.
A szérumspecifikus IgE meghatározása az allergiás légúti betegségben értékes lehetőség, ha a bőrpróba valamilyen okból nem végezhető el.
Módszerek:
- izotópos (radioallergosorbent-teszt = RAST);
- fluoreszcens;
- enzimatikus (ELISA: enzyme-linked immunosorbent assay).
Az in vitro technikák előnye, hogy biztonságos, precíz és standardizált vizsgálatok, nem függnek a bőr reaktivitásától, és gyógyszerszedés sem befolyásolja, szenzitivitásuk és specificitásuk nem alacsonyabb, mint a bőrpróbáké. Egyértelmű hátrányuk, hogy drágák, és az eredményre esetleg heteket kell várni.
Nazális provokációs vizsgálat
Az alsó orrkagyló nyálkahártyájára juttatott antigénnel provokálhatjuk az orrnyálkahártyát, amelyre - az esetek nagy részében - a természetes expozícióhoz hasonló azonnali (korai) választ kapunk, de sok esetben tipikus késői reakciót is regisztrálhatunk. Az eredmény dokumentálása szubjektív (tüsszögési és orrváladékozási cseppszám mérése, orrdugulási tüneti pontszáma), valamint objektív módszerekkel (rinometria) lehet végezni. A provokáció történhet specifikus allergénnel vagy aspecifikus anyaggal (pl. hisztamin). Nem rutinvizsgálat, elsősorban tudományos, ritkábban differenciáldiagnosztikai céllal végezhető. A prick-teszthez viszonyítva nagyobb a szövődményes reakciók veszélye, ezért fokozott óvatosságot igényel.
Orrváladék-vizsgálat
Bakteriológia: a középső orrjáratból vett anyag bakteriológiai vizsgálatának eredménye jól korrelál a sinusokban lévő baktériumokkal, míg az orrból vakon vett kenetek eltérnek ettől.
Orrkenet és citológia: allergiás náthában és nem allergiás eozinofil rhinitisben (NARES) az eozinofil sejtek dominálnak az orrkenetben. Ebből következik, hogy a nazális eozinofília nem specifikus rhinitis allergicára. Bakteriális nátha kenetére a neutrofilek jelenléte jellemző. Az orrváladékból egyéb fontos információ is nyerhető, pl. hisztamin és albumin (fehérje), össz és specifikus IgE, valamint gombaelemek (spórák, fonalak) mennyiségének meghatározásával. Fokozott transsudatio esetén magasabb a fehérjetartalom.
Orrendoszkópia
A fül-orr-gégészeti vizsgálat alatt - ha indikált - sor kerülhet endoszkópos diagnosztikára is, amely lényegesen pontosabb és specifikusabb módszer, mint a hagyományos rinoszkópia. Differenciáldiagnosztikai esetekben az egyéb rinológiai eltérések tisztázásában elengedhetetlen. Merev és fiberoszkópiás módszereket különíthetünk el.
Képalkotó eljárások
Szummációs orrmelléküreg-felvételek
A szummációs orrmelléküreg-felvétel a sinus maxillaris, frontalis és sphenoidalis egyértelmű fedettségének, nyálkahártya-duzzanatának, érintettségének, valamint folyadéknívó, mucokele, ciszta- és csontdestrukció kimutatására alkalmas. Mind álnegatív, mind álpozitív eredmény gyakran előfordul. Rendelése és értékelése fül-orr-gégész szakorvos feladata, nem rutindiagnosztikai eljárás.
Komputertomográfia (CT)
Az orrmelléküreg-betegségek megállapítására legjobban bevált eljárás. A lágy részek és a csontos fal jó elkülönítése révén pontosan mutatja a folyamatok elhelyezkedését és kiterjedését, jól ábrázolhatók a sebészeti szempontból fontos anatómiai képletek.
Mágneses rezonanciavizsgálat (MR)
Ez a technika a csontképleteket nem mutatja, így a gyulladásos melléküreg-betegségek esetében kisebb a diagnosztikus értéke.
Nazális légzésfunkciós vizsgálatok
Nazális csúcsáramlásmérés
Kilégzési csúcsáramlás mérése (NPEF: nasal peak expiratory flow): a vizsgálat során a levegőáramlás legnagyobb sebességét mérik, amellyel a levegőt ki tudja fújni a beteg. A nazális csúcsáramlásmérésnek inspiratorikus formáját is alkalmazzák (NPIF: nasal peak inspiratory flow). Az orrlégzés szűrővizsgálatára és otthoni monitorozására alkalmas módszer.
Rinomanometria
A vizsgálat során a dinamikusan változó orrbemeneti és -garati nyomáskülönbség és az ennek hatására beáramló respirációs levegő áramlási sebességének párhuzamos mérése történik, amelyből a nazális rezisztencia kiszámolható. Anterior és posterior, valamint aktív és passzív módszerek ismeretesek. Objektív, dinamikus eljárás, amelyből a vizsgált orrlégzésre következtethetünk, de alkalmas pl. a provokációs vizsgálat eredményének objektív dokumentálására vagy gyógyszerhatás monitorozására.
Akusztikus rinometria
Statikus eljárás, amelynek segítségével az orrbemenettől való távolság függvényében az orrüreg - a respirációs levegő haladására merőleges síkú - keresztmetszete, valamint térfogata határozható meg. A vizsgálat hanggenerátorral előállított ultrahanggal történik, amelyet egy cső- és orradapter segítségével juttatunk az orrba. A visszavert jeleket mikrofon regisztrálja, az értékeléshez komputeres módszer szükséges. A rinomanometria jó kiegészítője, ahhoz hasonló esetekben alkalmazható.
Mucociliaris funkciós vizsgálatok
Szacharinteszt: a mucociliaris transzporttevékenység sebességének megállapítására szolgáló vizsgálat, amely során azt az időt mérjük, amíg egy részecske az orrüreg hosszán végighalad. Ép csillószőrös működés esetében ez az idő kevesebb mint 30 perc. Károsodott ciliaris működést tapasztalhatunk sinusitis chronicában, rhinitis allergicában, lokálisan alkalmazott gyógyszerek hatására (orrcseppek, helyi érzéstelenítők).
Ciliaris csapásszám mérése: a ciliumok működését fáziskontraszt-mikroszkóp alatt is meg lehet vizsgálni. A csillószőrök csapási frekvenciáját Hz-ben fejezzük ki, az alsó kagylóról vett anyag frekvenciája egészséges egyednél 12-15 Hz.
Elektronmikroszkópos vizsgálat: az elektronmikroszkóp alatt fény derülhet a ciliumok deformitására (pl. primer ciliaris dyskinesis).
Szövettani vizsgálat
Specifikus folyamat vagy daganat gyanúja esetén célirányos szövettani mintavétel és hisztológiai vizsgálat szükséges.
Szaglásvizsgálat
Endonasalis betegségekben romolhat a szaglóképesség, amely általában az akadályozott nazális respirációs levegőáramlás következménye (a szaganyag szaglóhámhoz való eljutása gátolt), de a szaglóhám károsodása is előfordulhat. A szaglásvizsgálatot objektív és szubjektív módszerekkel végezhetjük el.
Objektív:
- szagingerre adott élettani változások vizsgálata;
- szaginger által kiváltott agyi potenciál mérése.
Szubjektív:
- szaglási küszöb mérése;
- szagfelismerés;
- adaptációs teszt.
A mindennapi klinikai gyakorlatban a szubjektív vizsgálatokat alkalmazzuk, legtöbbször a szagfelismerést vizsgáljuk.
Differenciáldiagnózis
Rhinosinusitis
- Akut
- Recidiváló akut
- Krónikus
Orr- és melléküreg-polyposis
Strukturális és mechanikai eltérések
- Orrsövényferdülés
- Orrkagyló-hipertrófia, concha bullosa
- Adenoid vegetáció
- Az ostiomeatalis egység (infundibulum) anatómiai variációi
- Idegen test
- Choanalis atresia
Tumorok
Granulomák
- Wegener
- Középvonali malignus reticulosis (Midline)
- Sarcoidosis
- Egyéb
Liquorfisztula
Egyéb etiológia
- Primer ciliaris dyskinesis
- Egyéb mucociliaris transzport-rendellenesség
- Cisztás fibrosis
- Immundefektusok
A rhinitisek elkülönítő diagnosztikája
| Tünet | Virális | Bakteriális | SAR | PAR | Idiopathiás |
|---|
| Vizes orrfolyás | +++ | - | +++ | ++ | +/++ |
| Sűrű/sárgás orrfolyás | - | +++ | - | - | - |
| Tüsszögés | +++ | + | +++ | ++ | +/- |
| Orrviszketés | + | - | +++ | +/- | +/- |
| Gátolt orrlégzés | ++/+++ | +++ | ++/+++ | +++ | ++/+++ |
| Szemtünetek | + | - | ++/+++ | - | - |
| Láz/elesettség | ++ | +/- | - | - | - |
Differenciáldiagnosztikai algoritmus
A rhinitis kezelése
A kezelésnek több szintje ismeretes, amely magába foglalja a megelőzést, az allergének elkerülését és eltávolítását, a lépcsőzetesség elvén alapuló tüneti-gyógyszeres és immunterápiát, valamint a gondozást. A terápiának és az ajánlásoknak bizonyítékokon alapuló adatokra kell támaszkodniuk. A kezelés általában addig hatékony, ameddig a gyógyszer adagolása történik, és nem szükségszerű, hogy a jól bevált szer esetében tachyphylaxia alakuljon ki. A modern kezelési elveknek a költséghatékonysági mutatókat is figyelembe kell venniük.
Allergénkerülés
Ezzel a módszerrel ritkán érhető el tünetmentesség, mivel az allergénforrás teljes és végleges eltávolítása csak esetenként oldható meg (hobbiállat, foglalkozási allergén, élelmiszer). Ha lehetséges, a környezetrendezési eljárásokat még akkor is tanácsos végrehajtani a lakáson belül, ha hatásuk nem lehet teljes, mert ezek általában javítják a beteg állapotát, és csökkentik a gyógyszeres kezelés iránti igényt. Az atkamentesítést a házipor mennyiségének, illetve a lakáson belüli nedvesség csökkentésével ajánlatos kezdeni, amelynek hatása az acaricidek és az atkamentes ágyneműk alkalmazásával tovább javítható.
A következő eljárások jönnek szóba: a hálószoba berendezése legyen egyszerű, könnyen tisztítható, mosható, szintetikus ágyneműk javasoltak, amelyekre speciális, atkát át nem eresztő huzatot lehet húzni. A kárpitozott bútorok, vaskos takarók, függönyök kerülendők, az ágyneműhuzatokat, függönyöket hetente 60 °C-n kell mosni, a gyermekjátékokat szintén rendszeresen kell mosni vagy egy napra fagyasztóba tenni. A lakás relatív páratartalmának alacsonyan (50% alatt) tartása előnyös, ezért gyakori szellőztetés és a párásítók használatának mellőzése javasolt. Takarításkor kerülendő a függönyök, szőnyegek, kárpitozott bútorok rázása és porolása, rendszeres nedves portörlés javasolt, a padozat legyen felmosható vagy nedvesen takarítható. Hetente kétszer alapos porszívózás (szűrő és eldobható papír porzsák) előnyös. Lehetőleg ne az allergiás beteg takarítson, és takarítás után 2-3 órán keresztül kerülje el a helyiséget vagy viseljen arcmaszkot. Atkaölő kémiai anyagok alkalmazása tovább csökkentheti az atkamennyiséget. Szőrös, tollas állatok lakásban való tartása nem ajánlott, mivel egyrészt az állatok mellett ugrásszerűen nő az atkaszám, másrészt a levált hámsejtek, beszáradt testnedvek a levegőbe kerülve az allergiás egyén légútjaiba juthatnak. A lakásban tartott kedvenc háziállat eltávolítása után az előnyök néha csak hetek, hónapok múlva érzékelhetők.
Ennél sokkal nehezebb a pollen és egyéb, lakáson kívüli allergénexpozíció mértékének csökkentése. A pollenszámot 1989 óta hazánkban is rendszeresen regisztrálják, a mérések adatai a sajtóban hozzáférhetőek. A pollenkalendárium alapján megjósolható, hogy egy adott allergéntermészetű virágpollen koncentrációja melyik hónapban lesz várhatóan magas, így a nyaraláshoz tanácsokat adhatunk az allergiás betegeknek. A beteg pollenszezonjában kerülje a magas pollenszennyezettségű, illetve gyomos helyeket, lehetőleg keveset tartózkodjon a szabadban. Rendszeresen mossa a haját, naponta többször mosson kezet és arcot, viseljen napszemüveget. Magas pollenszám esetén tanácsos csukott ablakok mellett zárt térben tartózkodni, és szűrőberendezést, légkondicionálót alkalmazni. A magas hegyvidéki, illetve a tengerparti levegő jó hatású. A lakáson belüli penészgombaforrásokat fel kell kutatni és megszüntetni, valamint a háziporatka-eliminációnál részletezett környezeti intézkedéseket kell tenni.
Figyelembe kell venni azt is, hogy pollen- és penészgomba-allergén a magevő kisállatok eleségével is a lakásba kerülhet. A profilaktikus óvintézkedéseknek nagyobb jelentősége van gyermekkorú allergiás rhinitiseseknél, mint a felnőtteknél. Kimutatták, hogy öröklött allergiára való hajlam esetén klinikai tünetek csak az allergénnel való jelentős expozíció után nyilvánulnak meg. Lehetséges, hogy a korai allergénkerülés (szekunder prevenció) módosíthatja érzékeny gyermekeknél a betegség lefolyását.
Gyógyszeres kezelés
A farmakoterápia beállítása a betegség etiológiai és kórélettani jellemzőinek figyelembevételével történik, de figyelni kell a rhinitis formáját, időtartamát és súlyosságát is. Szezonális allergiás nátha esetében célszerű a gyógyszerek profilaktikus, azaz a pollenszezonban korai - a tünetek megjelenése előtti - alkalmazása.
Antihisztaminok
A hisztamin szöveti hatásait specifikus, H1-, H2-, H3- és az újabban felfedezett H4-receptorokon fejti ki. Az erek H1-receptorainak ingerlése vasodilatatiót, az érfal permeabilitásának fokozódását, orrfolyást, az orrnyálkahártya érző idegvégződéseinek izgalma viszketést, tüsszögést okoz. A H2-receptorok a gyomorsav-elválasztásban és immunszabályozásban fontosak, a H3-receptorok a légúti kolinerg neurotranszmisszióban és a központi idegrendszer működésében játszanak szerepet.
Az antihisztaminok a H1-receptorokhoz kötődve nem aktiválják azt, hanem a dominálóan hisztaminhatásnak tulajdonított korai allergiás reakció tüneteit enyhítik: csökken a vascularis permeabilitás és a viszketés, ellazul a simaizomzat. Emellett mérsékelik a ciklikus GMP- és prosztaglandintermelést, gátolják a nervus vagus afferens rostjainak aktivációját. Az allergiás reakció késői fázisát, a nyálkahártya-ödémával és következményes orrdugulással járó inflammatiót csak mérsékelten befolyásolják. Az antihisztaminokat hagyományosan nem tekintjük antiasztmatikumoknak. Annak ellenére, hogy a nazális submucosa mirigyein jelentős számú H2-receptor van, a H2-receptor antagonisták nem befolyásolják jelentősen az orrfolyást (Mygind és Naclerio 1993). Az első generációs antihisztaminok (klórfeniramin, difenhidramin, clemastin, hidroxizin) a központi idegrendszeri H1-receptorokra kifejtett erős hatásuk miatt szedálhatnak, amelynek számos oka van: a gyenge H1-szelektivitás, a vér-agy gáton való átjutás képessége (lipofilitás, ionizáció, szérumproteinekhez való kötődés, aktív transzport jelenléte), az agyi receptorokhoz való erős kötődés, esetleg a hisztamin N-metiltranszferáz gátlása. E gyógyszerek többsége antikolinerg és antiszerotonin aktivitású is, így szájszárazságot, az étvágy fokozódását okozzák. Az allergiás rhinitis kezelésében - néhány kivételtől eltekintve, pl. terhesség - ma már nem javalltak. A második generációs H1-receptor antagonisták (azelastin, cetirizin, loratadin, mizolastin) viszonylag lipofóbok, ezért alacsony az idegszöveti penetrációjuk, és elsősorban a perifériás H1-receptorokhoz kötődnek, ellentétben az első generációs antihisztaminokkal. Ezek az antihisztaminok terápiás dózisban nem vagy csak kisebb mértékben jutnak át a vér-agy gáton, de szupraterápiás dózisban adagolva nagyobb mértékben is penetrálhatnak. A nem szedatív jelző helyett helyesebb nem szedatív spektrumú vagy relatíve nem szedáló antihisztaminokról beszélni. A második generációs antihisztaminok közül a cetirizin és a loratadin a korai és késői allergiás reakció során felszabaduló hisztamin gátlásán túlmenően a késői allergiás folyamatban csökkenti az eozinofil és bazofil sejtek migrációját, aktivációját, a prosztaglandin-D2, tromboxán-B3, leukotrién-C4 kiválasztását a nazális szekrétumban, valamint az adhéziós molekulák expresszióját is.
Dózisfüggő szívtoxicitási hatást írtak le a forgalomból már kivont terfenadinnál és astemizolnál, azonban ez a kinidinszerű mellékhatás nem jellemző valamennyi antihisztaminra. A kompetitív elvű rendszer miatt a májban, a citokróm P450-en metabolizálódó gyógyszerek (astemizol, terfenadin, valamint makrolidek [erythromycin] és ketokonazolok) együttes adagolása kapcsán csökkenhet az antihisztamin lebomlása és nőhet a plazma koncentrációja. Utóbbi a kritikus érték fölé növekedhet, ami bizonyos esetekben a szívizomsejt káliumcsatornáinak blokkolásán keresztül repolarizációs zavarokat (QT-idő megnyúlása, aritmia, torsade de pointes) okozhat. Annak ellenére, hogy a loratadin a májban metabolizálódik, a fenti gyógyszerekkel együtt adva - a plazmaszint emelkedése ellenére - nem okozott kardiális mellékhatásokat. Ettől függetlenül a loratadin és a májmetabolizmust csökkentő gyógyszerek egyidejű alkalmazása körültekintést igényel.
Az utóbbi évek fejlesztései nyomán újabb antihisztaminok jelentek meg (desloratadin, fexofenadin, levocetirizin), amelyek az eredeti molekulák metabolitjai vagy enantiomerjei (levocetirizin). E metabolitok megtartották - esetenként meghaladják - eredeti hatékonyságukat, de biztonságosabbak, mert anyagcseréjük során elkerülik a májat, és a vesén (részben az epével) keresztül ürülnek ki a szervezetből. Az új molekulák hatáskezdete gyorsabb, szupraterápiás dózisban is biztonságosak. Az egyik - nagyszámú, randomizált, kontrollált tanulmányokat feldolgozó - I/a típusú métaanalízis szerint a fexofenadin rendelkezik jelenleg a legelőnyösebb nem szedatív spektrummal (Shamsi Z et al.). Más vizsgálatok szerint (Mann RD et al., 43 363 beteg) a fexofenadin, a cetirizin és a loratadin esetében egyaránt alacsony a szedatív mellékhatás eshetősége, amely fexofenadin és loratadin esetében - egymáshoz viszonyítva - nem mutatott szignifikáns különbséget. Ugyancsak jól dokumentáltak e molekulák antiflogisztikus tulajdonságai, és feltételezhető, hogy ezeknek tulajdonítható a több szerző által reprodukálhatóan kimutatható decongestiós hatás. Utóbbi klinikai értékét közepes/súlyos rhinitisben még több szakember vitatja, ez tehát még további kontrollált klinikai vizsgálatot igényel.
Nem szedatív spektrumú antihisztaminok
| Hatóanyag | Gyári név | Átlagos napi adag |
|---|
| Cetirizin | Zyrtec
Parlazin
Cetirizin-ratiopharm | 1x10 mg |
| Desloratadin | Aerius | 1x5 mg |
| Ebastin | Kestin | 1x10 mg |
| Fexofenadin | Telfast | 1x120 mg |
| Levocetirizin | Xyzal | 1x5 mg |
| Loratadin | Claritine
Erolin
Flonidan | 1x10 mg |
| Mizolastin | Mizollen | 1x10 mg |
| Helyi hatású (nazális) antihisztaminok |
| Azelastin | Allergodil | 2x1-1 puff orrba
(0,56 mg) |
| Levocabastin | Livostin | 2x2-2 puff |
A forgalomban lévő, modern második generációs antihisztaminok között vannak szerkezeti, metabolikus és fehérjekötési különbségek, azonban hatékonyságukat, megbízhatóságukat és mellékhatásspektrumukat tekintve nincs köztük alapvető különbség.
A lokálisan alkalmazható H1-antihisztaminok (azelastin, levocabastin) jó antihisztamin- és dokumentált antiallergiás hatással is rendelkeznek, a hatás gyorsan (15 perc) kialakul. Hatásspektrumuk és hatékonyságuk egymással és az orális antihisztaminokkal egyező, mellékhatás a gyakorlatban elhanyagolható. Az orális antihisztaminok előnye, hogy hatásuk a szem- és egyéb nem nazális tünetekre is vonatkoznak, compliance-ük jobb, mint a napi kétszeri adagolást igénylő lokális antihisztaminoké, amelyek hatása azonban gyorsabban alakul ki. Számos orális készítmény tartalmaz első generációs, illetve nem szedatív antihisztamint és orális decongestiv sympathicomimeticumot (kombinációs készítmények). A kombináció előnye a gátolt orrlégzés hatékonyabb befolyásolása és a rhinitis medicamentosa elkerülhetősége.
Hátrányuk, hogy az orális sympathicomimeticumoknál - különösen fiatal- és időskorban - álmatlansággal, idegességgel, tremorral, tachyarrhythmiával, szájszárazsággal stb., valamint az első generációs antihisztaminok mellékhatásaival is számolni kell.
Az antihisztaminok csökkent(het)ik vagy megszüntet(het)ik a korai allergiás bőrreakciót, ezért diagnosztikus bőrpróba előtt legalább 4 nappal adásukat fel kell függeszteni.
Kortikoszteroidok
A kortikoszteroidokat széles körben alkalmazzák a gyulladásos betegségek kezelésében. Farmakológia hatásuk molekuláris mechanizmusai jórészt ismertek: citoplazmahormon-receptorokhoz történő kötődés után a hormonreceptor-komplex a nucleolusba jut, ahol a DNA-molekula specifikus pontjain kötődve befolyásolja a gyulladásos folyamatokra ható proteinek szintézisét. Hatásuk nagyobb részét génexpresszió révén fejtik ki, azt mindkét irányba képesek módosítani (génrepresszió, génaktiváció).
Terápiás hatásuk rhinitisben komplex antiinflammatiós hatásban nyilvánul meg: a nazális mucosa felszíni rétegeiben csökken a gyulladásos sejtes infiltráció, különösen a hízósejtek és eozinofilek száma, a hízósejt mediátorok felszabadulása, mérséklődik a hiperreaktivitás és a vascularis permeabilitás, ennek eredményeként a nyálkahártya-ödéma és nyákszekréció. Allergiás rhinitisben a szteroidok alkalmazása lokális adagolással történik, per os kezelésre vagy más szisztémás alkalmazásra ritkán kerül sor.
A helyileg ható szteroidok terápiás előnyei abból adódnak, hogy a biológiai hormonhatás a szteroidok gyulladáscsökkentő hatásának lokális alkalmazása mellett is kialakul, a szisztémás effektus a szerek szokásos terápiás dózisai mellett elhanyagolható. Az első korszerű helyileg ható szteroid, a beclomethason dipropionat 1973-ban történt bevezetése után a flunisolid, triamcinolon, budesonid, fluticason, majd a mometason vált elérhetővé. A fejlesztés során javultak a lokális hatás tekintetében fontos farmakológiai jellemzők (szteroid receptor binding affinitás, first-pass metabolizmus). A nazális nyálkahártyafelszínről felszívódó gyógyszermennyiség (kb. 30%) a szisztémás keringésbe, a tápcsatornába jutott rész (kb. 70%) pedig a portalis keringésen keresztül a májba kerül, ahol a korszerű vegyületek - budesonid, fluticason, mometason - több mint 90%-a first-pass metabolizmus során inaktiválódik (Brattsand és Axelsson 1997). Egyes szerzők a nazális beclomethason növekedésre kifejtett negatív hatását is közölték, azonban ezen a téren kevés a releváns adat. A nagy dózisú belégzett kortikoszteroidoknak van csak általában biokémiai és laboratóriumi eszközökkel kimutatható szisztémás hatása a hipofízis-mellékvese rendszerre és a csontanyagcserére. Utóbbi elsősorban a rövid távú csontnövekedésre vonatkozik, ami nem befolyásolja a prognosztizált, elérhető testmagasságot, azaz a hosszú távú csontnövekedést, mely inkább a kezeletlen asztmával mutat összefüggést. A belégzett szteroidok jótékony hatása messze túlnő a - nagyobb dózisoknál esetlegesen tapasztalható - szisztémás mellékhatásokon. A három modern nazális szteroidmolekula receptoraffinitásában, hatékonyságában, first-pass eliminációs arányában, a zsíroldékonyságot tükröző szöveti és szérumeloszlási arányában mutatkoznak kisebb különbségek, klinikai hatásosságuk és biztonságosságuk között azonban nem tapasztalható lényeges különbség. Fentieket figyelembe véve óvatosság ajánlott nazális és pulmonalis szteroid, illetve szteroidtartalmú krémek együttes adagolásánál, valamint gyermekek hosszabb távú kezelésénél, amikor a legkisebb hatásos dózis javasolt.
A helyi szteroidok a rhinitis összes tünetét a leghatékonyabb módon csökkentik, ami egyértelmű terápiás előny az antihisztaminokkal szemben (Harding és Heath 1976). Összehasonlító klinikai vizsgálatokban valamennyi tünet mérséklésében eredményesebben alkalmazhatók, mint a dinátrium-kromoglikát (Welsh et al. 1987). A nazális mucosa duzzanata okozta orrdugulás a lokális szteroidkezelés bevezetése után néhány nappal kezd csökkenni, ezen időszakban szükség lehet decongestans orrcsepp alkalmazására a nazális szteroid bejuttatása előtt. Szezonális és perennialis allergiás és a perennialis nem allergiás rhinitisek középsúlyos és súlyos formájában a gyulladáscsökkentő gyógyszeres kezelés alapja.
A lokális szteroidok vizes vagy glikolos oldatok mechanikus porlasztásával vagy száraz por formájában juttathatók az orrba. Magisztrális szteroidos orrcseppek adása korszerűtlen, veszélyes és kontraindikált. Az egyes szerek, illetve eszközök helyes használati módját - amitől a gyógyszer optimális eloszlása várható a nyálkahártyán - a betegeknek meg kell mutatni. A jó lokális hatás feltétele, hogy a gyógyszer minél nagyobb nyálkahártya-felületre kerüljön, ami a nazális bejuttatás módjának függvénye. E tekintetben legelőnyösebbek a gyógyszeroldatot mechanikusan porlasztó eszközök, illetve a turbuhaler (Mygind 1993). A betegoktatás másik fontos pontja annak ismertetése, hogy a helyi szteroidok hatásának felépülése néhány nap, tehát a készítményeknek azonnali - a decongestansokhoz hasonló - hatása nincs. Mellékhatásként nyálkahártya-pörkösödés, szárazságérzet, orrvérzés fordulhatnak elő, a septum perforációja raritásként leírt.
A szisztémás alkalmazásból ismert vegyületek, a betamethason és a dexamethason orrcsepp formájában bejuttatva szintén nagyon hatékonyak a rhinitis kezelésében, de tekintve, hogy felszívódás utáni metabolizmusuk lassú, szisztémás hormonhatással is számolni kell, ezért krónikus kezeléshez nem ajánlottak. Szisztémás szteroidkezelésre akkor kényszerülünk, ha a beteg nagy adagú nazális szteroid- és nem szedáló antihisztamin-készítmény mellett is kínzó tünetekkel küszködik. Ez esetben történjen rövid, 10-14 napos per os szteroidkúra 20-24 mg/nap metilprednizolon vagy prednizolon formájában. Az így elért, javult klinikai állapot rendszerint lokális szteroiddal fenntartható. Folyamatos orális szteroidterápiát ne állítsunk be rhinitises tünetek miatt, minden esetben a kúraszerű alkalmazást kell előnyben részesíteni. Depó szteroidinjekciók (betamethason, metilprednizolon) krónikus kezeléshez - farmakokinetikai tulajdonságaik miatt - ellenjavalltak, a folyamatos hatóanyag-leadás következtében legnagyobb a mellékhatások kialakulásának esélye. Ugyanakkor lökésterápia céljára sem optimálisak, tekintve a kis dózisú, egyenletes hormonfelszívódást. Gyermekkori rhinitisben és terhesség idején szisztémás szteroidot ne alkalmazzunk. Intranasalis szteroidinjekció kontraindikált.
Nazális szteroidok
| Hatóanyag | Gyári név | Átlagos napi dózis
(adagok felnőttkorban) |
|---|
| Beclomethason | Aldecin aeroszol (vivőgázzal) | 4x1-1 befújás (a: 50 μg) |
| Budesonid | Rhinocort Aqua (mech. porlasztóval) | 1-2x1-2 befújás mko. (a: 32 μg) |
| Rhinocort Aqua (mech. porlasztóval) | 1-2x1-2 befújás mko. (a: 50 μg) |
| Rhinocort Aqua (mech. porlasztóval) | 1-2x1-2 befújás mko. (a: 64 μg) |
| Rhinocort Turbuhaler | 1x1-1 beszippantás mko. (a: 100 μg) |
| Fluticason | Flixonase oldat (mech. porlasztóval) | 1-2x1-2 befújás mko. (a: 50 μg) |
| Mometason | Nasonex (mech. porlasztóval) | 1-2x1-2 befújás mko. (a 50 μg) |
Kromoglikátok
A dinátrium-kromoglikát (DNCG) és a nedocromil sodium helyileg ható gyulladáscsökkentő antiallergikum. A gyulladáscsökkentő hatás mechanizmusa nem ismert. IgE-függő allergiás reakciókban gátolja a hisztamin és egyéb mediátor anyag felszabadulását a hízósejtekből (Okuda 1985).
A vegyület a sejtmembrán kötőproteinjéhez kapcsolódik, amely membránszakasz az intracelluláris kalciummozgás szabályozásával áll kapcsolatban (Dixon 1985). Feltételezhető, hogy a gyors kalciumcsatornák blokkolásával éri el a hízósejt-degranulációt gátló hatást. A DNCG az enyhe és közepesen súlyos allergiás náthákban mérsékli az orrviszketést, tüsszögést, orrfolyást, de alig befolyásolja az orrdugulás okozta panaszokat. Farmakokinetikája napi négyszeri alkalmazást tesz szükségessé, ami rontja a beteg compliance-ét. A kizárólag lokális hatás miatt oldatként (Taleum orrspray) vagy por formájában (Intal kapszula insufflatorral) juttatható az orrba. A kapszula napi adagja 4x1 (á 20 mg) mindkét orrfélbe, a Taleum orrspray 4x1-1 befújás (á 2,7 mg). Mellékhatásként a por okozta nyálkahártya-irritáció tüsszögést provokálhat. A DNCG preventív gyulladáscsökkentő hatása gyengébb, mint a lokális szteroidoké, indikációs területe az enyhe fokú allergiás rhinitis. Kromoglikátot tartalmaz az Opticrom, a Stadaglicin és a Taleum szemcsepp is. A nedocromil sodium orrban és szemben helyileg alkalmazva igen hatásos antiallergikum.
Antikolinerg szerek
Az antikolinerg hatású vegyületek - ipratropium-bromid és oxitropium-bromid - a nazális mucosa kolinerg muszkarinreceptorainak gátlása útján hatnak. Mérséklik a nazális szekrétum termelődését, de a nyálkahártya-vasculaturára hatástalanok, az orrdugulást nem befolyásolják (Mygind és Borum 1990). Nincs hatásuk a szenzoros idegvégződéseken, ezért a tüsszögést és orrviszketést sem képesek hatékonyan befolyásolni (Jokinen és Sipila 1983). Terápiás alkalmazása ezért idiopathiás (vazomotoros) rhinitis esetében merül fel, ahol az orrfolyás mérséklése céljából az alkalmazott gyógyszer-kombináció része lehet. Átlagos napi terápiás adagja 4x1 befújás mindkét orrfélbe (á 0,02 mg).
Adrenoreceptor-agonisták (decongestiv, nyálkahártya-lohasztó szerek)
Infekció, allergiás reakció, vazomotoros bénulás kapcsán a prae- és postcapillaris erek (arteriolák, venulák) vasodilatatiója miatt az orrnyálkahártya, ezáltal a barlangos és erectilis testek vérteltsége többszörösére növekedhet, ami klinikailag a gátolt orrlégzés egyik oka. Sympathicomimeticus hatású szerekkel ezen érterületeken vasoconstrictio hozható létre, és ezáltal az orrlégzés jelentős mértékben javítható. E hatás elérhető egyrészt az erek falában található α1- és α2-receptorok direkt ingerlésével, másrészt a szinapszisok noradrenalin (NA)-tartalmának felszabadításával, illetve a NA re-uptake rendszer gátlásával. A postcapillarisan elhelyezkedő α1-receptort stimuláló agonisták (fenilefrin) kevésbé okoznak szöveti ischaemiát, hatásidőtartamuk azonban rövidebb (1-2 óra), a prae- és postcapillaris α2-receptorok agonistái (naphazolin és az imidazolinszármazék oxy- és xylometazolin) az arteriolák és venulák simaizomelemeire egyaránt hatva igen jó és tartós vasoconstrictiót hoznak létre (kb. 6-8 óra). Hasonló hatású anyag a tetryzolin. A klasszikus szernek számító efedrin, valamint a pszeudoefedrin és a fenilpropanolamin a szinaptikus NA-felszabadulás serkentésével fejtik ki szimpatikus hatásukat. Helyileg orrcsepp, orrspray, illetve szemcsepp formájában széles körben alkalmazzák őket, és kombinálhatók antihisztaminnal (fenilefrin + dimentinden m., tetryzolin + antazolin) is. A rhinitis egyéb tüneteire nem hatnak. A lokális nazális decongestansok - infekciózus és egyéb eredetű rhinosinusitis kezelésében is - csak rövid időszakra rendelhetők, ami semmilyen körülmények között sem haladhatja meg a 10-14 napot. A lokális decongestansok bármely csoportjának (α1- és α2-receptor agonisták, NA-liberalizáló szerek) hosszan tartó adagolása (orrcseppabúzus) a rhinitis medicamentosa kialakulásának veszélyét rejti magában, amelyhez még társulhat a benzalkonium-klorid esetleges károsító hatása is. A rebound orrdugulással, addikcióval, toleranciával és nazális hiperreaktivitással jellemezhető rhinitis medicamentosa sokszor igen nehezen kezelhető, és maradandó orrnyálkahártya-károsodással is járhat. Utóbbiak miatt a lokális decongestansok rendelésekor figyelembe kell venni, hogy rövid időszakra szóló, tüneti-adjuváns terápiáról van szó, amelyről a beteget is tájékoztatni kell.
Orálisan is rendelhető a fenilefrin (Neo-Citran, Rhinopront), az efedrin, a pszeudoefedrin (Clarinase, Zyrtec D) és a fenilpropanolamin (Contac, Rhinopront). Az orális szerek hatása gyengébb, mint a lokális decongestansoké, de a káros lokális mellékhatásokra nem kell számítani. Az orális formák általában első generációs antihisztaminnal vannak kombinálva (lásd antihisztaminok), illetve szisztémás sympathicomimeticus hatásuknál fogva mellékhatásokat okozhatnak: nyugtalanság, agitációs állapot, tremor, alvászavar, tachycardia, angina pectoris, vérnyomás-emelkedés, fejfájás és vizelési zavar, ezért nem adható coronariabetegségben, hipertóniában, hyperthyreosisban, glaukómában, diabetes mellitusban, prostatahypertrophiában, pszichiátriai kórképekben, terhességben, valamint kisgyermek- és időskorban. A decongestansok orrlégzést javító hatása kiváló, de mind a lokális, mind a szisztémás adagolás jelentős mellékhatásokkal járhat, valamint a rhinitis többi, meghatározó tünetére az antiallergiás-antiflogisztikus hatás hiányában egyáltalán nincs befolyással. Ezért a decongestansok nem első vonalbeli, adjuváns szerek a rhinitis kezelésében, és bármely forma rendelésekor mérlegelni kell a kizáró tényezőket és a mellékhatások lehetőségét.
Leukotrién-antagonisták
A leukotriének a rhinitis korai és késő fázisának fontos mediátorai, kifejezett vasodilatatiós és érpermeabilitást fokozó tulajdonságuk miatt a gátolt orrlégzés fenntartásában meghatározó szerepet játszanak. A leukotriénantagonisták (LA) a leukotriénreceptorokon fejtik ki antagonista hatásukat (montelukast, pranlukast, zafirlukast). Először az asztmás betegek kezelésében alkalmazták, de bebizonyosodott, hogy a rhinitises tüneteket is enyhítik. Asztmában aszpirinintoleráns betegek additív terápiájával biztató eredményekről számoltak be.
Jelenleg az 5-lipoxigenáz inhibitor antagonista (zileuton), valamint a CysLT (ciszteinil leukotrién) szelektív receptorantagonisták (zafirlukast, montelukast) rhinitisre gyakorolt hatásairól vannak adataink. Már 1990-ben közlemény jelent meg arról, hogy a zileuton javítja a gátolt orrlégzést.
Az ARIA dokumentum szerint - több, bizonyítékokon alapuló adatra támaszkodva - a leukotriénantagonisták a rhinitis és az asztma kezelésében hatékony gyógyszerek. Szezonális allergiás rhinitisben indikáltak, előnyösen befolyásolják a gátolt orrlégzést, de kevésbé csökkentik az orrváladékozást és a tüsszögést. A jelenleg elérhető kontrollált tudományos vizsgálatok szerint AR esetén hatékonyabbak a placebónál, de nem hatékonyabbak az orális antihisztaminoknál, a nazális szteroidoknál, és meglepő módon az antihisztamin + LA kombináció sem hatékonyabb, mint ezek a szerek külön-külön. Más adatok szerint antihisztaminnal együtt adva hatásos, mert a leukotriénantagonisták gátolt orrlégzést javító hatása jól kiegészíti az antihisztamin-kezelés hiányosságát. Egyes állásfoglalások szerint ez a terápiás módszer biztonságos és hatékony, mások szerint inkább additív szerepe lehet (ASA-szindróma, asztma, terápiarezisztens orrdugulás, kezelésre nehezen reagáló sokszervi atópiás beteg, orrpolip).
Rinológiai szempontból feltétlenül további adatok és tapasztalat szükséges a pontos indikációk meghatározásához. Hazánkban - jelenleg - rinológiai indikációkban még nem törzskönyvezték.
Anti-IgE-terápia
Az IgE-molekula központi patogenetikai szerepe feltételezi, hogy az IgE hatásának gátlásával komoly terápiás eredményt lehet elérni. A rekombináns, humanizált, monoklonális IgE-ellenanyagot (omalizumab) az IgE-molekula Cε3 domainjával szemben fejlesztették ki, amely dózisfüggő módon csökkenti a szérum IgE-koncentrációt, és ezzel párhuzamosan javulnak a klinikai paraméterek is. Az antitest az IgE-molukula azon részéhez kötődik, amellyel az IgE-molekula egyébként a nagy affinitású FcεRI receptorhoz kapcsolódik. Az IgE-molekula és a monoklonális antitest komplexet képez, amely megakadályozza, hogy az IgE a FcεRI receptorhoz kötődjön, ezáltal blokkolja a hízósejtek, a bazofilek és az IgE közötti interakciót. A rendelkezésre álló tudományos adatok szerint AR esetén a kezelés hatására (300 mg sc., 3-4x a szezonban) szignifikáns mértékben csökkent az antihisztamin-igény, a szérum- és nazális eozinofilsejt-szám, az IgE-t megkötő sejtek száma, valamint javultak az életminőségi paraméterek. Rhinitis immunterápiájának kiegészítéseként további javulást tudtak kimutatni. Asztmában lényegesen több az eredményes kezelést alátámasztó tudományos adat. Mivel az omalizumab minden szabad IgE-vel komplexet alkot, a poliallergiás betegek kezelésére is használható.
Ígéretes lehetőségnek tűnik az allergiás rhinitis bizonyos eseteinek kezelésében, bár a nemzetközi ajánlásokban egyelőre nem szerepel, drága és hazánkban nincs törzskönyvezve.
Szemcseppek
Az allergiás rhinitis bizonyos eseteiben a vezető tünetek a conjunctiva érintettségével kapcsolatosak, melyek szükségessé tehetik a conjunctiva lokális kezelését. Erre rendszerint akkor kerül sor, ha az orális nem szedáló antihisztaminok - vagy a választott egyéb kezelési formák (lásd még „a rhinitis kezelésének lépcsőzetes elve” fejezetben) - nem enyhítik a panaszokat. A helyileg ható antihisztaminok (emadastin - Emadine, azelastin - Allergodil) hatékonysága gyengébb, mint a szisztémás antihisztamin-készítményeké, de enyhe/közepes panaszok esetén önállóan vagy komplementer kezelésként alkalmazva kiválóan csökkentik a szemviszketést és irritációt. Önmagukban vagy vasoconstrictorral kombinálva (Spersallerg szemcsepp - antazolin chlor. és tetryzolinum chlor.) főként akut tünetek esetén javasoltak. A monokomponensű vasoconstrictorok (Visine - tetryzolinum) csökkentik az irritációt, de a szem kiszáradásához vezetnek. Az allergiás gyulladás megelőzésére a kromoglikát tartalmú szerek (Opticrom, Stadaglicin, Taleum, szemcsepp) ajánlottak. Hatásuk csak rendszeres használat esetén alakul ki, a napi terápiás dózis 4-6x1-1 csepp. Hasonló hatásmechanizmusú az N-acetil-aszpartil-glutamátot (spaglumicum natrium) tartalmazó Naaxia, illetve a lodoxamidtartalmú Alomide szemcsepp.
A conjunctiva allergiás reakciója néha ijesztő mértékű, ödémája olyan súlyos lehet, hogy zselatinszerű képletként emelkedik elő az alsó szemhéjból. Ez esetben indokolt a lokális szteroid alkalmazása (Efflumidex, Flucon, Ultracortenol szemcsepp) rövid kúra formájában. A szteroidszemcseppek krónikus adása lehetséges mellékhatásaik (másodlagos fertőzések, glaukóma, subcapsularis hályog, cornea károsodás) miatt ellenjavallt.
A rhinitis terápiájában alkalmazott gyógyszerek és hatásuk az egyes tünetekre
| Név | Viszketés, tüsszögés | Orrfolyás | Szemtünetek | Orrdugulás | Szaglászavar |
|---|
| Kromoglikátok | + | + | - | + | - |
| Orális antihisztaminok | ++ | ++ | ++ | + | - |
| Nazális antihisztaminok | ++ | ++ | +/- | + | - |
| Vasoconstrictorok | - | - | - | ++++ | +/- |
| Helyi szteroidok | +++ | +++ | ++ | +++ | + |
| Orális szteroidok | +++ | +++ | +++ | ++++ | ++ |
| Ipratropium-bromid | - | ++ | - | - | - |
| Leukotrién-antagonisták | - | + | ++ | ++ | ? |
Immunterápia
A specifikus immunterápia (SIT) az allergiás betegségek kezelésének hatékony, integrált része, amelyben nagy tisztaságú specifikus allergént tartalmazó vakcinát emelkedő adagban, majd megfelelő fenntartó dózisban évekig alkalmaznak a betegség tüneteinek és súlyosságának mérséklése, a gyógyszeres kezelés veszélyeinek és költségeinek csökkentése, valamint az allergiás beteg életminőségének javítása érdekében. A SIT célja specifikus immunológiai tolerancia indukálása az alkalmazott allergénnel szemben. Az allergiás rhinitis hatással lehet az asztmára, gyakran társul a rhinitis asztmával vagy meg is előzheti azt. Az asztma nem tartható jól karban, ha az allergiás rhinitist nem megfelelően kezelik. Ezért alakulhatott ki és érdemel figyelmet az a megközelítés, hogy az IgE közvetítette betegségek szempontjából a felső és alsó légutakat egységként kezeljék („egyesült légutak”, „egységes” légúti betegség), annál is inkább, mivel közös a kiváltó ok (allergén), és közös a gyulladásos folyamat is, mely állandósulhat és megsokszorozódhat az egymásba fonódó mechanizmus miatt. A WHO új kezdeményezése, az ARIA dokumentum 2001-ben az asztma és a rhinitis asszociációját értékelve azt hangsúlyozza, hogy az asztmát, a rhinitist és conjunctivitist egyetlen egységként kezeljék az immunterápia mérlegelésekor, felírásakor. A specifikus immunterápia az egyetlen olyan kezelési eljárás, mely a sokkszervtől függetlenül javíthatja a gyulladást, és az általa okozott immunmoduláció az atópiás kórkép egészére kedvező hatású lehet. Az immunterápia gátolja a bőrön és orron jelentkező allergén kiváltotta késői választ, ugyanakkor a T-lymphocyták beáramlása és az eozinofilek aktiválódása csökken. A Th2 típusú allergiás reakcióról Th1-es típusúra kapcsolás következik be, melynél a T-lymphocyta választ egy INFγ-mRNA expressziónövekedés jellemez, ez gátolhatja a helyi IL-4 indukálta IgE-szintézist és/vagy blokkoló IgG-antitestek termelését segíti elő. Újabb allergénstimulusra a Th1 sejtvonalnak megfelelő citokinek termelődése a normális immunitás és a SIT eredményessége irányába mutat, a Th2 sejtek reaktiválódása pedig az allergiás reakció fellángolásához vezet. Ezért várható kevésbé sikeres SIT előrehaladott állapotban levő poliallergizált, atópiás betegeknél; jobb az eredmény, ha a kezelés a betegség egészen korai fázisában elkezdődik. SIT után a perifériás T-sejt-anergia méh- és darázsméreg-, fűpollen-, háziporatka- és macskaszőr-allergia különböző klinikai kórformáiban (anafilaxia, asztma, rhinitis, conjunctivitis) bizonyított. A kezelés biztonságosságát fokozza rekombináns hipoallergén allergének használata, mivel csökken a mellékhatások (anafilaxia) rizikója, de az immunogenitás megmarad.
A következő allergének jönnek szóba allergiás rhinoconjunctivitis immunterápiájában: fa-, fűpollenek, gyomnövények (elsősorban parlagfű és feketeüröm, kettős szenzibilizációban mindkettő; egyes esetekben útifű), perennialis allergének esetében elsősorban háziporatka-, állatiszőr-, tollallergia esetében csak kivételesen (foglalkozás, emocionális tényezők). A specifikus immunterápia indikációjának részleteit illetően utalunk a Cserháti és mtsai (Gyógyszereink 2004) közleményére. Az IgE közvetítette kórkép diagnózisát korrekt módon kell felállítani, és a tünetek kiváltásában egyértelműen igazolni kell az allergénexpozíciót. Az immunterápia a gyermekek és fiatal felnőttek, kevésbé az idősek kezelési eljárása. Az injekciós formájú, szubkután immunterápia (SCIT) kedvező hatását kettős-vak, kontrollált vizsgálatokban allergiás rhinitisnél világosan kimutatták fűpollenre (Varney 1991; Dolz 1996), parlagfű, nyírfa, üröm, háziporatka (Blainey 1984) és macskaszőr kivonatára. Néhány szerző a tünetek tekintetében felnőtt parlagfűérzékeny betegeknél (Creticos 1996), mások felnőtt atkaérzékeny asztmásoknál negatív eredményt kaptak. Gyermekeknél az atkakivonat hatásos volt asztmában is (Warner 1978). Igen fontos eredménnyel zárult a PAT vizsgálat, mely megállapította, hogy szezonális rhinitises gyermekek SIT kezelése csökkentette a későbbi asztma kockázatát (Moller). Alkalmilag súlyos reakciók jelenhetnek meg az injekciót követően, különösen asztmás betegeknél. A súlyos reakciók elkerülése, a hatásosság növelése érdekében a specifikus immunterápiát helyes, ha specialista indikálja, a szisztémás reakció ellátására felkészült orvos jelenlétében végzik, és az adrenalin- (epinefrin-) injekció azonnal elérhető, ha anafilaxiás reakció jelentkezne. Minden beteget legalább 30 percig meg kell figyelni az injekció beadása után. A betegválogatás nagyon fontos, és a potenciális veszélyek nem múlhatják felül az immunterápia előnyét. Az immunterápia hatása dózisfüggő, alacsony adagok általában hatástalanok. A magasabb dózis növelheti a súlyos szisztémás reakciók lehetőségét, ezért az optimális fenntartó adagot kell alkalmazni. Nem kell súlyos, anafilaxiás mellékhatásokkal számolni a nem parenteralis, lokálisan alkalmazott (orális, nazális, sublingualis) immunterápia (régebben alternatív immunterápia) bevezetésekor. A lokális kezelésnél csak kivételesek a mellékhatások, azok is igen enyhék. A beteg otthon alkalmazza, elmarad az injekciók miatti orvoshoz járás időigénye, fáradsága, költsége; ennek hátránya, hogy a beteget ritkábban lehet ellenőrizni. Az injekciók elmaradása viszont - főleg gyermekeknél - csökkenti a kezelés gyakorlati és pszichés terheit. Mivel a kontrollált vizsgálatok nem tudták kimutatni az orális és bronchialis alkalmazás klinikai hatását, biztonságosságát, ezek adását fokozatosan elhagyták. A nazális SIT csak a rhinitisben hatásos, és különleges alkalmazási technikát igényel, fonáció szükséges hozzá, ez a tüdőbe történő inhaláció kivédését szolgálja (Cserháti 1997). Bár igazolódott, hogy jelentős mennyiségű direkt allergénfelszívódás nincs a sublingualis mucosáról, mégis a sublingualis immunterápia (SLIT) hatásosnak bizonyult számos vizsgálatban, jelenleg ez a legkiterjedtebben használt nem injekciós immunterápia Európában. A mucosalis immunrendszerhez való kapcsolódás és a hatás kifejtése ilyen körülmények között megtörténik. A sublingualis immunterápiában a kumulatív dózis nagyságrendekkel nagyobb, mint az injekciósnál. Sublingualis immunterápia gyermekeknek és felnőttnek is adható (Pajno, Khinch). Az immunterápiás készítmények az utóbbi időben bővültek az immunogén tulajdonságokat megőrző monoid sublingualis készítménnyel. A monoid, éppen azért, mert allergoid (módosított allergén), kevésbé okoz allergiás mellékhatást, mint az eredeti nem módosított allergén, de érintetlenül megőrzi antigén-tulajdonságát. A többi nem injekciós kezeléshez hasonlóan otthon végezhető.
Egyéb kezelési módok
A nem allergiás, illetve az idiopathiás rhinitis kezelésében egyéb kezelési formák is szóba jönnek. A kapszaicin szelektív módon roncsolja az orrnyálkahártya SP-immunoreaktív, C típusú afferens rostjait, mellyel megelőzhető, hogy az axonreflex során felszabaduló P-anyag (SP) kifejtse hatásait az orrnyálkahártyán (Wolf 1988; Stjärne 1992; Hirschberg 1993). A módszer - Wolf szerint alkalmazva alkalmas a „terápiarezisztens” idiopathiás rhinitises esetekben az orrnyálkahártya deszenzibilizálására. A gátolt orrlégzésre kifejtett hatását kritikával kell értékelni, mivel a rendelkezésre álló adatok szerint az eredmények ebben a kezelési formában sem tekinthetők hosszú távúnak. Azokban az esetekben, amikor perzisztáló rhinitisnél a konzervatív kezelés eredménytelen és/vagy egyéb releváns strukturális eltérés akadályozza az eredményes terápiát, sebészi beavatkozás (orrkagylóplasztika, alsó orrkagyló lézervaporizációja vagy elektro-, kriokoaguláció, ESS [endoszkópos sinussebészet], Vidian-neurectomia) is szóba jön. Allergiás rhinitisben a szükséges sebészi beavatkozást szezonon vagy aktív szakon kívül szabad csak elvégezni.
Az allergia kezelésében az első lépés az allergén eltávolítása. Ezt a célt szolgálja az orrüreg izotóniás sóoldattal vagy tengervízkivonattal (Sterimar, Isomar) történő átmosása (orrzuhany). Klinikai tanulmányok igazolják a fiziológiás sóoldattal történő rendszeres orrzuhany jó hatását (Spector 1982). Az aktív, dinamikus mosás célja az allergénrészecskék eltávolítása és ezáltal a tünetek mérséklése, valamint a gyógyszerek mennyiségének csökkentése (Seppey 1995). Az orrüreg öblítésével és átmosásával az egyéb típusú rhinitisekben felhalmozódott kóros váladékot (genny, mucus) és pörköket is eltávolíthatjuk. Kisgyermekkorban e módszerrel hatékonyan távolítható el a le nem szívható vagy orrfúvással ki nem ürülő kóros orrváladék. Komplementer kezelésként meg bizonyos esetekben - jó hatásúak lehetnek a vitaminos orrolajok (pl. Coldastop), amelyek a nazális szteroidok esetenkénti helyi mellékhatásait kompenzálhatják.
A természetes gyógymódok minden formája támogatható, amelyet a Magyar Tudományos Akadémia Orvosi Osztálya elismert, s pontos orvosi diagnózison alapul, ellenőrizhető és törzskönyvezett alkotóelemeket tartalmaz.
A rhinitis kezelésének lépcsőzetes elve
Intermittáló/szezonális allergiás rhinitis
Allergén és irritáló anyagok - elsősorban aktív és passzív dohányzás - elkerülése
I. Enyhe rhinitis
- Orális, nem szedatív H1-antihisztamin a tünetek felléptekor
vagy - helyileg antihisztamin vagy kromoglikát vagy nedocromil orrba, szembe, illetve mindkettőbe
II/a Közepes fokú rhinitis, döntően orrpanaszokkal
- Helyileg szteroid az orrba, naponta
és - helyileg antihisztamin vagy kromoglikát vagy nedocromil a szembe
II/b Közepes fokú rhinitis, döntően szempanaszokkal
- Orális, nem szedatív H1-antihisztamin rendszeresen
vagy - Helyileg antihisztamin vagy kromoglikát vagy nedocromil orrba,
és - szteroid vagy kromoglikát vagy nedocromil helyileg a szembe
III. Súlyos rhinitis
- Szteroid helyileg az orrba és nem szedatív H1-antihisztamin orálisan
vagy - orális szteroid rövid ideig (gyermekeknek nem adható!)
Szezon után az immunterápia mérlegelendő
Szezonális rhinitis esetén a szezonban korán tanácsos megkezdeni a kezelést
Perzisztáló/perennialis allergiás rhinitis
Az allergén vagy irritáló anyagok elkerülése
- Helyileg antihisztamin vagy kromoglikát vagy nedocromil orrba (gyermekkor, enyhe fokozat)
vagy - orális, nem szedatív H1-antihisztamin (gyermekkor, enyhe/közepes fokozat)
vagy - helyileg szteroid az orrba
Nem allergiás rhinitis
I. Kifejezett vizes orrfolyással - Az irritáló anyagok elkerülése
- Helyileg antikolinerg szer (ipratropium bromid) az orrba
II. Döntően orrdugulással - Az irritáló anyagok elkerülése
- Helyileg szteroid az orrba
Betegtájékoztatás
Az allergiás rhinitis kezelésének sikere nagymértékben függ a beteg és kezelőorvosa jó együttműködésétől. A legfontosabb, hogy a beteg bizalmát már a kezelés elején megszerezzük. Időt kell áldozni arra, hogy elmagyarázzuk a rhinitis lényegét, a betegség kialakulásának okát. A beteg kooperációját nagymértékben növeli, ha betegségét és annak kezelését részletesen ismeri. Fontos, hogy még a pollenszezon előtt jusson tudomására, mit kell tennie, hogy tüneteit jól kontrollálja, és életminőségét javítsa. Juniper (1992) tanulmánya igazolja, hogy ha a beteg a pollenszezon előtt megkapja a gyógyszereit, emellett megfelelő oktatásban részesül és írott utasításokkal is ellátjuk, akkor tünetei minimálisak lesznek, és életminősége nem romlik. Jó, ha alapos ismeretekkel rendelkezik a következőkről:
- Hogyan és miért fejlődik ki a rhinitise?
- Mit kell tennie, hogy elkerülje vagy csökkentse az allergén expozícióját?
- Milyen következményekkel kell számolnia, ha „alulkezeli” vagy nem kezeli betegségét?
- Milyen gyógyszeres kezelés szükséges ahhoz, hogy közel tünetmentes legyen?
- Milyen profilaktikus teendői vannak (időben, a szezon előtt elkezdett terápia pollenallergia esetén, perennialis allergia esetén, ha fokozott expozíció elé néz)?
- A terápia lehetséges mellékhatásairól és a gyógyszer-interakciókról.
- A lokális decongestansok túlzott használatának következményeiről.
- Tájékoztatni kell a beteget a készülékek helyes alkalmazásáról.
 |
Mindenekelőtt az orvosi rendelő az a hely, ahol a betegnek ezekhez az ismeretekhez hozzá kell jutnia, azonban a kezelőorvos nem kell egyedül végeznie felvilágosító munkáját, jól képzett asszisztens, a betegklubok, alapítványok segítségét is igénybe veheti. Egyszerűen leírt instrukciókkal lehet megerősíteni a szóban elhangzottakat. A tájékozott beteg jobb együttműködésével a terápia sikeresebbé, a beteg életminősége jobbá válhat.
Speciális vonatkozások
Rhinitis gyermekkorban
A gyermekkori nátha patofiziológiai mechanizmusa, klinikai képe, diagnózisa és kezelési szempontjai látszólag azonosak a felnőttekével, azonban van néhány különbség, mely miatt speciális megfontolásokat figyelembe kell venni (Mygind 1991; Siegel 1993; Van Cauwenberge 1991).
A rhinitis a gyermekkor leggyakoribb betegsége. 2-6 éves kor között a gyermekek évente átlag 6 alkalommal betegszenek meg ún. „megfázásos” (virális) náthában. Minél kisebb a gyermek, a rhinitis (nátha) tünetei annál súlyosabbak lehetnek, a következmények, szövődmények előfordulásával annál inkább számolni kell. Újszülött- és csecsemőkorban a szűk viszonyok és a gyermekek obligát orrlégző volta légzési zavarokhoz vezethet rhinitisnél.
A megbetegedések legtöbbször a téli és tavaszi hónapokban fordulnak elő. Sokan egyszerűen megfázásról beszélnek, és ennek biztosan szerepe is van a rhinitis kialakulásában, az elsődleges mégis a vírusinfekció. Általában rhinovirusok, ritkábban Coxsackie, adeno-, illetve Myxovirusok a felelősek a kórkép kialakulásáért. A vírusfertőzést követheti bakteriális szuperinfekció, ennek jele, hogy az orrváladék purulenssé válik, a közérzet romlik, láz, hőemelkedés lép fel.
Az akut, infekciós rhinitis kezelése gyermekkorban tüneti. Legfontosabb az orrváladék eltávolítása, az „orrhigiéné”, amelynek eszköze csecsemő- és kisdedkorban a porszívóra szerelhető orrszívó. Ezzel kellő nagyságú vákuumot tudunk elérni anélkül, hogy a gyermeknek sérülést okoznánk. Fokozhatjuk a leszívás hatékonyságát különböző depletiót okozó orrcseppek, spray-k használatával (pl. oxymetazolin, xylometazolin), de adagolásukkor gondolni kell a tachyphylaxia jelenségére, valamint az abúzus csillómozgást bénító hatására, ezért általában 4-5 napos kezelés után 2-3 nap szünet iktatandó be. Ezalatt a különböző sós orrcseppek (pl. fiziológiás sóoldat, Sterimar) becseppentése alkalmazható. A fentieken kívül szükség lehet antiflogisztikumokra (paracetamol, amidazofén), valamint C-vitaminra is. Antibiotikumot egyszerű rhinitis esetében nem rendelünk, legfeljebb lokális készítmény jöhet szóba, mint pl. a fusafungin. Szisztémás antibiotikus kezelést csak igazolt felülfertőződés, illetve szövődmény kapcsán adunk: otitis mediában, sinusitisben, bronchitisben. Ugyancsak a szövődmények kezelése során kerülhet sor a különféle nyákoldók, mucoregulansok használatára, elsősorban elhúzódó, száraz, kínzó köhögés miatt. Ilyenkor acetilcisztein-származékokat rendelünk, és adjuváns terápiaként előírjuk a helyiség párásítását. Nem ajánlatos a régebben széles körben alkalmazott „gőzölés”, sok forrázásos baleset oka volt a forró folyadékkal telt edény kiömlése a gyermekre, másrészt a forró gőz okozta reaktív hyperaemia csak fokozta a dugulásérzést az orrban.
A gyermekkori krónikus rhinitis hátterében meg kell keresni az okot. Ezt legtöbbször a megnagyobbodott adenoidban találjuk meg, ennek eltávolításával a panaszok látványosan javulnak vagy megszűnnek. Orrsövényferdüléssel főként újszülöttnél találkozunk: oka a szülőcsatornán való áthaladáskor az orr „megnyomódása”. Ha idejekorán gondolunk rá, és megvizsgáljuk, a rendellenesség egyszerűen „helyre tehető”. Ha az újszülöttnél elnézik, később már csak műtéttel, septumplasztikával lehet a helyzetet javítani, ezt leghamarabb 5-6 éves korban végezhetjük el. Orrpolip ritkán fordul elő gyermekkorban. Ha mégis látjuk, először cisztás fibrosisra kell gondolni, pubertás körüli fiúk egyoldali orrpolipja esetében juvenilis angiofibroma merülhet fel, de néha allergiás alapon is előfordul. Egyoldali krónikus, bűzös orrfolyás orr-idegentestre utalhat, ami egyáltalán nem ritka gyermekkorban. Noha az újszülöttosztályokon kötelező születés után mindkét orr szondázása, találkozhatunk későbbi életkorban is choanalis atresiával. Legegyszerűbben gombos fémszonda óvatos bevezetésével győződhetünk meg a choanák átjárhatóságáról.
Az allergiás betegségek bármely életkorban megjelenhetnek, de az allergiás reakció típusa, megnyilvánulása és lokalizációja a kortól függ, az allergiás rhinitis az „allergiás mars” része. Az élet első hónapjaiban a gastrointestinalis allergián kívül a bőrt érintő atópia, mint pl. az ekcéma jelentkezik, és rendszerint az allergiára való hajlamot jósolja. Az élet első éveiben visszatérő hörghurut, asztmatikus hörghurut, sípoló nehézlégzés jelezheti az allergiás kórképet. Csecsemőkorban és a korai gyermekkorban az ételek a leggyakoribb allergének, az inhalált allergének a kor előrehaladtával válnak jelentőssé. 4 éves korig az IgE-közvetített fül-, orr-, torokbetegség ritka. Az allergiás nátha 4-5 éves kor után válik egyre gyakoribbá, és 0,8-14,9%-os az előfordulása 6-7 évesek körében és 1,4-39,7%-os a 13-14 éveseknél a világ minden földrészére kiterjedő ISAAC vizsgálat szerint. Az allergiás rhinitis legtipikusabb a serdülő- és fiatal felnőttkorban.
Az allergiás gyermeket felismerhetjük az arc jellegzetességei, mint pl. az allergiás szalutálás, az allergiás redő, az infraorbitalis sötét gyűrű alapján. Egyik jel sem patognomikus. Az általános fül-orr-gégészeti vizsgálat elengedhetetlen, idősebb gyermeknél ez magába foglalja a flexibilis vagy rigid rinoszkópiát is. Atópiás betegség gyanúja esetén fiatal életkorban is elvégezhető a bőrpróba, pozitivitása esetén igen hasznos információt nyerhetünk; negativitás esetén, 2-3 éves kor alatt a bőr életkorból adódó, nem megfelelő válaszadó képességét is mérlegelni kell. Az össz IgE normális értéke és a szérum specifikus IgE mennyisége kisgyermekkorban alacsonyabb, mint felnőtteknél. Az allergiás náthás gyermekek felének van csak emelkedett össz IgE-értéke.
A gyermekkori allergiás rhinitis kezelésének alapelve a felnőttekével megegyezik, de a hangsúly kissé eltérő, ügyelni kell a mellékhatások elkerülésére. A korai, megfelelő kezelés nemcsak terápiás hatású, hanem profilaktikus értéke is lehet. A profilaktikus óvintézkedéseknek nagyobb jelentősége van gyermekkorú allergiás náthásoknál, mint a felnőtteknél. Kimutatták, hogy még öröklött allergiára való hajlam esetén is a klinikai tünetek csak az allergénnel való jelentős expozíció után nyilvánulnak meg, ily módon lehetséges, hogy a korai beavatkozás, például az allergénkerülés módosíthatja érzékeny gyermekeknél a betegség lefolyását. Több gyermek vállalása esetén a következő gyermek kilátásaira is kihat egy maradéktalanul végrehajtott allergénmentesítés. Kisgyermekkorban a légúti allergének és irritánsok kerülését gyorsabban lehet biztosítani, mivel tüneteiket nagymértékben a lakáson belüli környezet határozza meg, itt töltik ugyanis idejük nagyobbik részét. A gyermekek nagy emocionális kötődése miatt nehéz a hobbiállat eltávolítását elérni. Atópiás családokban, az előrelátható konfliktusok elkerülése érdekében, mellőzni kell a lakáson belüli szőrös vagy tollas hobbiállat tartását. Az allergiás betegségek viszonylag gyakori előfordulása miatt zárt közösségek helyiségeiben (óvoda, iskola, kollégium) sem helyes az állattartás. A szájon át adható antihisztaminok, különösen az újabb, nem nyugtatóak képezik az allergiás nátha primer kezelését. A fiatal gyermekeknél, a kooperáció hiánya miatt, gyakran nehézségbe ütközik a helyi kezelés alkalmazása. Napi egy- vagy kétszeri alkalmazás előnyösebb, mert odahaza lehet alkalmazni, s nem kell az iskola dolgozóit is bevonni a kezelésbe. A nazálisan adható antihisztaminoknak az a nagy előnye, hogy alig van mellékhatásuk, viszont az alkalmazás helyétől eltérő szerven nem hatnak. A kromoglikát tartalmú orrspray-t régóta használják, bármilyen fiatal gyermeknek is felírható, de kooperációt igényel a használata. A kromoglikát optimális hatásának eléréséhez minimum naponta 4x kell alkalmazni, de napközben gyakran elfelejtik a betegek, ill. szüleik. A nazális kromoglikát kevésbé hatásos, mint a nazális szteroid.
A nazális szteroidok alkalmazásától - a hosszú távú kezelés szisztémás és lokális mellékhatásaitól tartva - többen óvakodnak. Több mint 15 éve használják a helyi szteroidokat, és gyakorlatilag nem közöltek mellékhatást, ezért ezeket az előírt dózisban (ami általában a felnőttek adagjának a fele, napi egyszeri alkalmazásban) ajánlani lehet, különösen akkor, ha az orrdugulás a legkifejezettebb tünet. A modern intranasalis szteroidokból (budesonid, fluticason, momethazon) nagyon kevés szívódik fel. A viszonylag magas bioelérhetőségű betamethazont gyermekeknek nem ajánlják. A lokálisan adható, nagy hatású, szisztémás mellékhatás nélküli szteroidok megjelenése óta az injekciós szteroidok orrba cseppentése idejétmúlt eljárásnak számít. A szisztémás kortikoszteroidoknak nincs helye a gyermekek komplikáció nélküli allergiás náthájának kezelésében! Veszélyes lehet helyi vasoconstrictort adni egy év alatti gyermekeknek, a szerek szűk terápiás és toxikus tartománya miatt, szív-ér rendszeri és központi idegrendszeri tüneteket okozhatnak. A szájon át adható decongestansok is csak óvatosan írhatók fel, alkalmilag központi idegrendszeri hatásuk lehet. A gyermekek allergiás rhinitisének kezelését alapvetően a prevenció irányelvei irányítsák, és a terápia, amennyire csak lehet, a tünetek súlyosságának megfelelő aktivitású és mellékhatás nélküli legyen. A legkisebb allergiás gyermekeknél a fiziológiás orrcsepp vagy spray segít az orr tisztításában evés vagy alvás előtt. A kromoglikát és bizonyos antihisztaminok négyéves életkor alatt is adhatók. A cetirizin 1 éves kortól, a loratadin 2 éves kortól már felírható azon országokban, ahol törzskönyvezték őket; a nazális szteroidok közül a momethazont 3, a fluticasont 4, a budesonidot 5 éves kortól lehet használni gyermekkorban.
Rhinitis időskorban
65 év felett allergiás mechanizmusok igen ritkán okoznak perennialis rhinitist. E betegcsoportban általában nem allergiás hátterűek a rhinitises panaszok. Az ok gyakran az autonóm beidegzés zavara, a muszkarinreceptorok kóros működése stb. Az idősek gyakori orrfolyásának, híg, profúz rhinorrhoeájának oka ismeretlen. Ipratropium-bromid 0,03%-os koncentrációjú vizes oldata (mindkét orrnyílásba 42 mcg naponta háromszor) gyakran hatásos lehet (Mygind és Borum 1990).
Igazi allergiás rhinitis előfordulhat ugyan időskorban, de - mint említettük - ritkán. A kezeléssel kapcsolatban mérlegelni kell, hogy a régebbi, szedatív hatású antihisztaminok gyakrabban okoznak székrekedést, látásromlást időseknél, mint fiatalabbaknál. Az érszűkítők viszont - főként parenteralis adagolás mellett - gyakran idéznek elő cardiovascularis és központi idegrendszeri tüneteket. Így az időskori rhinitisek kezelésekor lehetőleg helyi terápiát (dinátrium-kromoglikát, lokális szteroid, ipatropium-bromid) alkalmazzunk (Malm és Anggärd 1993).
Rhinitis terhességben
A második trimesztertől a szülésig a terhesek 32%-ánál a rhinitis tünetei, főként orrdugulás, orrfolyás előfordulhatnak (Marby 1986). A szülés után ezek a tünetek gyorsan megszűnnek. A terhesség folyamán a seromucinosus mirigyek hiperreaktivitása, a fagocitafunkció növekedése, valamint a vérátáramlás fokozódása figyelhető meg (Toppozada 1982). A rhinitis allergicában szenvedő terhesek orrtünetei jó vagy rossz irányba egyaránt változhatnak (Schatz 1988). Érdekes, hogy purulens sinusitis is gyakrabban fordul elő a terhesek között, mint az átlagos népességben (Sorri 1980). Terhesség alatt in vivo diagnosztikus tesztet nem szabad végezni anafilaxia veszélye miatt, a szérum specifikus IgE vizsgálata javasolt. A terápia során igen óvatosnak kell lennünk. A terhesek rhinitisének kezelésében különös hangsúlyt kap az allergének és irritáló anyagok kerülése. Ezt a célt szolgálja az orrüreg sóoldattal történő mosása (orrzuhany). Általános szabály, hogy a terhesség első trimeszterében - amennyiben lehetséges - semmiféle gyógyszert ne kapjanak a kismamák. Az azt követő időszakban is csak a haszon és a kockázat gondos mérlegelése mellett adható a lehető legkisebb adagban, legrövidebb ideig antiallergikum. Előnyben kell részesíteni a régi, ismert szereket és a helyileg adhatókat. Az amerikai FDA előírása szerint első generációs antihisztaminok, elsősorban chloropyramin (Suprastin) adható az előny/kockázat mérlegelése alapján. A második generációs antihisztaminok alkalmazását - a nem elegendő tapasztalat miatt - több szerző (Blaiss 2003) ellenzi. A legújabb adatok alapján azonban a cetirizin és a loratadin (Moretti ME et al.) is rendelhető terhességben, mivel nem észleltek magzati károsodást vagy kóros terhességet a gyógyszerek adagolásával kapcsolatban. Valamennyi, hazánkban forgalomban levő lokális szteroid adható terhességben az előny/kockázat mérlegelése mellett. Legtöbb ilyen irányú tapasztalat a beclomethason (Aldecin) és a budesonid (Rhinocort Aqua) orrspray-vel van (Mygind 1993; Kallen B. 1999). A szájon keresztül szedett decongestansok vérellátási rendellenességeket okozhatnak a placentában és a foetusban, ezért szedésük terhességben ellenjavallt. Lohasztó orrcseppeket terhességben csak óvatosan szabad használni, és szigorúan be kell tartani az adagolásra vonatkozó előírásokat. Túladagolva szintén placentalis keringési zavart okozhatnak, valamint a terhesek könnyebben hozzá is tudnak szokni a vasoconstrictor tartalmú nazális szerekhez.
Immunterápia elkezdése nem ajánlott a terhesség alatt, a fenntartó kezelés folytatható (Bousquet 1993).
Sportolók rhinitise
Az epidemiológiai felmérésekből ismert, hogy az aktív sportolók között lényegesen gyakoribb a rhinitis allergica előfordulása, mint az átlagos népességben (Weeke 1993; Didier 2003). A fizikai terhelés kezdetén - a felszabaduló noradrenalin hatására - vasoconstrictio, az orr ellenállásának csökkenése figyelhető meg (Cole 1980, 1983; Forsyth 1983). Ezt egy aránylag hosszú ideig tartó orreldugulás követi („rebound effektus”), amely a sportteljesítményre is kihatással lehet, elsősorban a hosszútávfutókat és a kerékpárversenyzőket érinti (Katelaris 2000, 2003). A sportolók orrpanaszainak gyógyszeres kezelésekor két alapelvet kell szem előtt tartani: a gyógyszer nem szerepelhet a doppinglistán, és nem befolyásolhatja hátrányosan a sportteljesítményt.
Doppinglistán szerepelnek az alábbi gyógyszerek:
- Vasoconstrictorok: Béta-fenil-etil-amin származékai (pl. Aktedron, Eferit stb.). Mindegyik vérnyomásemelő hatású, az amfetamin és a metilamfetamin erős pszichostimuláns is. Efedrin (pl. Calciphedrin, Coderit, Coderetta, Nasog. ephedrini stb.), pszeudoefedrin per os és/vagy nazális alkalmazása (pl.: Disophrol) tilos. Számos gyógyszer tartalmaz kombinációban antihisztamint és vasoconstrictort, erre is figyelni kell.
- Szisztémás kortikoszteroidok (pl. Prednisolon, Metypred, Oradexon stb.).
- Lokális szteroidok (pl. Aldecin, Rhinocort, Flixonase stb.) megengedettek, ha a sportoló kezelőorvosa nyilatkozik ennek szükségességéről.
Az alábbi gyógyszereknek hatása lehet a fizikai teljesítményre:
- Az első generációs antihisztaminoknak szedatív és antikolinerg hatásuk van.
- Az immunterápia napokig kellemetlen érzést okozhat a szubkután injekció helyén. Mindezeket figyelembe véve az allergiás rhinitisben szenvedő sportolók ideális kezelése második generációs antihisztaminokkal és lokális kortikoszteroidokkal történjék (Van Cauwenberge 1992). Amennyiben immunterápia mellett döntünk, akkor azt a sportszezon előtt legalább három hónappal el kell kezdeni. Tanácsos, hogy az injekciós kezelések napján a sportoló nagy fizikai terhelést ne végezzen. A sportorvosoknak tudniuk kell arról, hogy a versenyek idején (pl. nyári olimpiai játékok) a magas pollenszám az allergiás nátha exacerbatióját okozhatja, ami jelentősen befolyásolja a sportolók csúcsteljesítményét. Ismerniük kell a sportolók pollenérzékenységét és a verseny helyének aerobiológiai jellemzőit is. A betegség súlyosságának megfelelő kezelést időben el kell kezdeni.
Rhinitis és asztma
A felső és alsó légutak anatómiai, élettani és funkcionális egységet képviselnek. Számos epidemiológiai vizsgálat erősíti meg a rhinitis és az asztma együttes előfordulásának gyakoriságát, azaz a felső és alsó légutak összetartozásának tényét. A European Community Respiratory Health Survey felmérésében (Leynaert B et al.) a nem rhinitises populációban az asztma előfordulási gyakorisága 4% volt, míg a rhinitises betegek körében szignifikánsan nagyobb, 22,5%. Franciaországban 20 000 háztartás szűrésével végzett kérdőíves felmérésben a perennialis rhinitis prevalenciáját 4,1%-nak találták, a betegek 13,4%-ánál egyidejűleg asztma is fennállt (Pariente PD et al.). Az asztma szignifikánsan gyakrabban fordul elő perennialis rhinitisben, mint a betegség szezonális formájában. A krónikus rhinitises betegek egy részénél bronchialis hiperreaktivitás (BHR) demonstrálható, manifeszt asztmás tünetek nélkül, és ez a nem specifikus bronchialis túlérzékenység allergénexpozíció idején (pl. a pollenszezonban) rendszerint növekszik. Rhinitises betegeknél a BHR prediktív értéke az asztma kialakulására vonatkozóan mégis csekély, nincsenek meggyőző adatok arról, hogy kevesebb lenne az asztma későbbi megjelenése a bronchialis hiperreaktivitást nem mutató rhinitises csoportban. Rhinitises betegek követéses vizsgálatában a legtöbb szerző az asztma kialakulásának esélyhányadosát 4-5 közötti értéknek találta, ami azt jelenti, hogy az asztma kialakulásának kockázata a rhinitises populációban 4-5-szöröse az egészséges csoporténak. Az asztmás betegek többségének ugyanakkor egyidejűleg rhinitise is van. Allergiás asztmások 75%-ának, nem allergiás etiológiájú asztma esetében a betegek több mint 80%-ának vannak rhinitises panaszai, amelyek a súlyosabb betegség, az asztma miatt sokszor rejtve maradnak. A rhinitis és az asztma együttes megjelenésének jellegzetes klinikai képével találkozunk az ún. „aszpirinasztmában”, amit szalicil és egyéb nem szteroid gyulladásgátlókkal (NSAID) szemben fennálló túlérzékenység, krónikus perennialis rhinitis, orrpolip és eozinofília jellemez. Általánosan elfogadott, hogy a jelenség fenti készítményeknek az arachidonsav metabolizmusára kifejtett hatásával, fokozott leukotriénképződéssel kapcsolatos. Az idioszinkrázia ebben a betegcsoportban bármikor kialakulhat, a kérdéses szerekkel - szűrés jelleggel - végzett provokációs vizsgálatoknak nincs értelme, a kapott lelet csak az adott időpontra érvényes (Herjavecz I és mtsai).
A két betegség immunbiológiája, a nazális és bronchialis mucosa gyulladásos elváltozásai is hasonlóak, eozinofil sejtes, hízósejtes és T-sejtes infiltrációval jellemezhetők. Azonosak az involvált proinflammatiós mediátorok (hisztamin, leukotriének), T-sejt citokinek (IL-4, IL-5, IL-13, GM-CSF), kemokinek és adhéziós molekulák. Az eozinofil sejtes infiltráció és a légúti hám elvékonyodása, pusztulása azonban asztmában kifejezettebb, továbbá a betegség hosszú távú prognózisát meghatározó szöveti átépülés, a remodelling asztmában legtöbbször kimutatható, míg az allergiás rhinitisre nem jellemző. Az asztma és a rhinitis együttes megjelenése speciális terápiás szempontokat vet fel, ezt felismerve készült el az ARIA (Allergic Rhinitis and its Impact on Asthma) című nemzetközi szakértői ajánlás, amelynek főbb útmutatásai a következők (16):
- Az asztma kezelésének a nemzetközi asztmaterápiás ajánlást kell követnie.
- Az asztmában és rhinitisben egyaránt hatékony szerek a lokális szteroidok és az antileukotriének.
- Az antihisztaminok rhinitisben hatékonyabbak, mint asztmában.
- Az alfa-adrenerg agonisták csak rhinitisben, a béta-adrenerg agonisták csak asztmában terápiás értékűek.
- A rhinitis optimális kezelése javulást eredményezhet asztmában is.
- A lokális szteroidok nazális és inhalált együttes alkalmazása növeli a szisztémás hatás kockázatát.
A nem gyógyszeres terápia (betegoktatás, allergénelimináció) szempontjai hasonlóak, az immunmodulációt célzó terápiás beavatkozási forma, az allergénvakcinával történő kezelés az allergiás rhinitis és a szezonális asztma esetében jelenthet terápiás alternatívát. A gyógyszeres kezelés mindkét kórkép esetében a betegség klinikai súlyosságának a függvénye. Rhinitisben a helyileg ható szteroidok javasolt átlagos napi terápiás dózisa 100-200 mg (maximális napi adag 400 mg), míg asztmában az átlagos terápiás dózis 400-800 mg (maximális napi adag 1600-2000 mg). Az inhalált szteroidok dózis-hatás görbéje 1000-1200 mg körüli dózisoknál ellapul, az adag további emelését rendszerint nem követi jobb asztmakontroll, ellenben nő a szisztémás hatás kockázata. Amennyiben a rhinitises asztmás beteg nazálisan és inhalálva egyaránt nagy dózisú inhalációs szteroidterápiára szorul, a szisztémásan megjelenő hormonmennyiség összeadódik, és keresnünk kell azokat a gyógyszerterápiás és egyéb lehetőségeket, amelyekkel a fenntartó lokális szteroidadag csökkenthető. Rhinitis esetében ez a környezeti allergén mennyiségének mérséklésére irányuló rendszabályok betartását, illetve a nazális légzést rontó krónikus infekciók, kóros endonasalis elváltozások (pl. polipok) szanálását jelentheti. Asztma esetében az inhalált szteroid mellé adott hosszú hatású béta-2-agonisták (formoterol, salmaterol), illetve az antileukotriénekkel való kombináció ad lehetőséget az inhalációs szteroidadag csökkentésére. Szisztémás antiallergiás hatása alapján a rhinitis és az asztma egyidejű kezelése valósul meg a monoklonális anti-IgE-ellenanyagokkal végzett terápiával. Ilyen készítmény (omalizumab) néhány országban már törzskönyvezett.
Kapcsolódó betegségek
Ismert tény, hogy az alsó és felső légutak anatómiai, élettani és patológiai egységet képeznek, ennek következtében a rhinitis és az asztma együttes előfordulása gyakori. Az allergiás gyulladás azonban nem korlátozódik kizárólag csak a nazális nyálkahártyára. A rhinitis mellett több kórkép együttes előfordulása figyelhető meg, ilyenek a sinusitis, a conjunctivitis, az orrpolip és az otitis media bizonyos formái.
Rhinosinusitis
A sinus maxillarisok, az elülső rostasejtek, valamint a homloküreg a középső orrjáratba nyílnak, az ún. osteomeatalis egységbe, a hátsó rostasejtek és a sinus sphenoidalis pedig a felső orrjáratba, ill. a recessus sphenoethmoidalisba. Bármilyen kóros folyamat, amelyik nyálkahártya-duzzanathoz vezet, lezárhatja a szájadékokat, és megteremtheti a lehetőségét az akut vagy krónikus sinusitis kialakulásának (Rowe-Jones J 1995). Számos tanulmány foglalkozik az allergiás rhinitis és a sinusitis kapcsolatával. Az egyoldali idült orrmelléküreg-gyulladásos betegek 40%-a egyidejűleg bizonyítottan allergiás rhinitisben is szenvedett, míg a kétoldali krónikus sinusitises betegeknél ez az arány 80%-nak bizonyult. Ez azt jelenthetné, hogy az allergének bejutnak a sinusokba, és ott ugyanolyan allergiás gyulladást okoznak, mint az orrnyálkahártyán. (Karlsson G 1994) Amikor radioizotóppal jelölt polleneket jutattak be az orrnyálkahártyára, azokat a sinusokban nem tudták kimutatni (Adkins 1998). A sinusok nyálkahártyájának biopsziás mintáiban azonban aktivált eozinofil sejteket találtak mind az allergiás, mind a nem allergiás egyedeknél. Hízósejtek, makrofágok, neutrofil sejtek ugyancsak emelkedett számban voltak jelen. Ugyanakkor ha összevetették az orrnyálkahártyában és a sinusok nyálkahártyájában az ICAM-1-expressziót perennialis allergiás rhinitises betegek esetében, azt találták, hogy az a sinusokban alacsonyabb (Demoly 1998). Mindezekből következik, hogy bár az allergiás gyulladás eredményezhet ventilációs zavart a melléküregekben, amelyikből akut vagy krónikus sinusitis kialakulhat, az ezzel kapcsolatos vizsgálatok még nem meggyőzőek.
Otitis media
Az allergiás gyulladás indirekt és direkt módon érintheti a középfület.
- Az orrnyálkahártya allergiás gyulladása az Eustach-kürt funkciójának zavarát eredményezheti, amely otitis media catarrhalis chronica serosához vezethet (behúzódott dobhártya mellett savós váladék van a dobüregben).
- A középfül-nyálkahártya maga is lehet target szövete az allergiás folyamatnak, fenntartva egy rekurráló, ill. folyamatos otitis media allergicát (serosus váladék elődomborodó v. normális állású dobhártya mellett). Számos tanulmányban atópiás gyermekek körében lényegesen gyakoribbnak találták a savós középfülfolyamatok előfordulását nem atópiásokhoz viszonyítva (Reisman 1975; Berstein 1993; Ruokonen 1981). Számos vizsgálatot végeztek (állatkísérleteket és humán megfigyeléseket egyaránt), hogy megfigyeljék, az allergiás gyulladás megjelenik-e a középfül nyálkahártyáján, azonban eddig csak azt tudták bizonyítani, hogy tubafunkció-zavar állt elő, és ez képezte a középfülfolyamatok közös etiológiáját (Mogi 1992; Tomonaga 1988).
Orr- és melléküregpolip
A század elején az orrpolipok jelenlétét még szorosan összekapcsolták a légúti allergiás állapotokkal. Ez a teória azután az 1970-es évektől kezdve lassan megváltozott, s kezdték az allergia szerepét az orrpolip patogenezisében minimálisnak vagy teljesen elhanyagolhatónak tekinteni. E témakörben meglehetősen nagy számban jelentek meg közlemények. A polyposisos betegek között a pozitív bőrteszt elfordulását valamivel gyakoribbnak találták, mint az átlag populációban (Keith 1995). Nem találtak különbséget az allergiás és nem allergiás egyedekből származó polipok között, amikor az eozinofil, ill. a hízósejtek számát vizsgálták (Ruhno 1990). Jelentős különbséget észleltek ugyanakkor a sejtek által expresszált citokinek vonatkozásában (Hamilos 1995). Az allergiás egyedekből származó polipszövetekben szignifikánsan magasabb volt az mRNA-t expresszáló sejtek denzitása GM-CSF-re, IL-3-ra, IL-4-re és IL-5-re, a nem allergiás egyedek mintáiban pedig a GM-CSF-re, IL-3-ra és IFN-γ-ra mRNA-t expresszáló sejtek denzitása volt magasabb. Small és mtsai (1985) allergénspecifikus IgE-t találtak olyan betegekből származó orrpolipokban is, akiknél mind a szérum RAST vizsgálata, mind a bőrteszt negatív volt, alátámasztva ezzel azt a feltevést, hogy lokális IgE-antitestképződés és lokális allergiás reakció eredményezhet lokális allergiás gyulladást. Mindezen adatok ellenére a kapcsolat a nazális polyposis és az allergia között még nem tekinthető bizonyítottnak. Az viszont tény, ha az orrpolipos betegeken concomittáló allergiás rhinitis vagy asztma is jelen van, az allergén elkerülése, illetve egy sikeres immunterápia jelentősen javíthatja a beteg állapotát.
Irodalom
- AAAAI, ACAAI: Practical parameters for allergen immunotherapy. J Allergy Clin Immunol 1996;98:1-11.
- Aberg M, Hesselmar B, Aberg B, Eriksson B: Increase of asthma, allergic rhinitis and eczema in Swedish schoolchildren between 1979 and 1991. Clin Exp Allergy 1995;25:815-819.
- Abramson M, Puy R, Weiner J: Allergen immunotherapy for asthma. Cochrane Database Syst Rev. 4: CD001186. (2003)
- Adkins TN, Goodgold HM, Hendershott L, Slavin RG: Does inhaled pollen enter the sinus cavities? Ann Allergy Clin Immunol 1998;81:181-4.
- Adkinson NF, Eggleston PA, Eney D, et al.: A controlled trial of immunotherapy for asthma in allergic children. N Engl J Med 1997;336:324-31.
- Ammar-Kohdja A: Influence des contraceptifs oraux sur la muqueuse nasale. Rev Lar Otol Rhinol 1971;92:40-42.
- Bachert C, Ganzer U (eds.): Die nasale Hyperreaktivität. Die allergische Rhinitis und ihre Differentialdiagnosen - Konsensusbericht zur Pathophysiologie, Klassifikation, Diagnose und Therapie. Laryngo-Rhino-Otol. 1997;76:65-76.
- Bachert C, Hauser U, Prem B, Rudack C, Ganzer U: Proinflammatory cytokines in allergic rhinitis. Eur Arch Otorhinolaryngol (Suppl 1) 1995;252:44-49.
- Balogh K, Augusztinovics M, Koppány J és mtsai: Az allergiás rhinitis prevalenciája Budapesten és Pest megyében 2002-ben. Allergologia és Klinikai Immunológia 2003;6:23-29.
- Batts A, Marriot C, Martin G, Bond S: The effect of some preservatives used in nasal preparations on mucociliary clearance. J Pharm Pharmacol 1989; 1:156-159.
- Bentley AM: Immunohistology of the nasal mucosa in seasonal allergic rhinitis: increase in activated eosinophils and epithelial mast cells. J Allergy Clin Immunol 1992;89:877-883.
- Berstein JM: The role of IgE-mediated hypersensitivity an the development of otitis media with effusion: a review. Otolarygol Head Neck Surg 1993;109:611-20.
- Bittera I, Gyurkovits K: A gyermekkori rhinitis allergica epidemiológiai és kórtörténeti adatainak elemzése. Gyermekgyógyászat 1990;41:401-407.
- Blainey AD, Phillips MJ, Ollier S, Davies RJ: Hyposensitisation with a tyrosine adsorbed extract of Dermatophagoides pteronyssinus in adults with perennial rhinitis. Allergy 1984;39:521-28.
- Blaisdell IH: The use of estrogenic substances in atrophic rhinitis. Laryngoscope 1938;48:699-719.
- Bousquet J, Michel F-B: Immunotherapy. In: Mygind N, Naclerio RM. eds. Allergic and non-allergic rhinitis. Clinical aspects. Copenhagen, Munksgaard, 1993:137-48.
- Bousquet J, Van Cauwenberge P, Khaltaev N et al.: ARIA Workshop Group. Allergic Rhinitis and its Impact on asthma. J Allergy Clin Immunol 2001;108(Suppl 5):147-334.
- Brattsand R, Axelsson BI: Basis of airway selectivity of inhaled glucocorticoids. Inhaled Glucocorticoids in Asthma. In: Lenfant C ed. Lung Biology in Health and Disease. Marcel Dekker. 1997;97:351.
- Broder I, Higgins MW, Mathews KP, Keller JB: Epidemiology of asthma and allergic rhinitis in a total community: Tecumseh, Michigan. J Allergy Clin Immunol 1974;54:100.
- Canonica GW: Clinical implications of minimal persistent inflammation. EAACI Meeting, Rhodes, 1997.
- Chalon J, Loew DAY, Orkin LR: Tracheobronchial cytologic changes during the menstrual cycle. J Am Med Assoc 1971;218:1928-1931.
- Charpin D, Vervloet D, Charpin J: Epidemiology of asthma in western Europe. Allergy 1988;43:481-492.
- Cole P, Fastag O, Forsyth R: Variability in nasal resistance measurement. J Otolaryngol 1980;9:309-315.
- Cole P, Haight JSJ, Cooper PW, Kassel EE: A computed tomographic study of nasal mucosa: effects of vasoactive substances. J Otolaryngol 1983;12:58-60.
- Colloff MJ, Ayres J, Carswell F, et al.: The control of allergens of dust mites and domestic pets: a position paper. Clin Exp Allergy 1992;22 (Suppl. 2.):1-28.
- Connell JT: Quantitative intranasal pollen changes. III. The priming effect in allergic rhinitis. J Allergy 1969;50:43-44.
- Coste A, Rateau JG, Bernaudin JF, Peynegre R, Escudier E: Nasal polyposis pathogenesis: a flow cytometric and immunohistochemical study of epithelial cell proliferation. Acta Otolaryngol (Stockh) 1996;116:755-61.
- Creticos PS, Reed CE, Norman PS et al.: Ragweed immunotherapy in adult asthma. N Engl J Med 1996;334:501-50.
- Croner S, Kjelmann N-IM, Eriksson B, Roth A: IgE screening in 1701 newborn infants and the development of atopic disease during infancy. Arch Dis Child 1982;57:364-368.
- Cserháti E, Mezei G: Nasal immunotherapy in pollen-sensitive children Allergy 1997;52(Suppl. 33):40-44.
- Cserháti E, Adonyi M, Barkai L, Bittera I, Borsodi K, Gyurkovits K, Kósa L, Mezei Gy, Nagy B, Novák Z, Petrássy K: A gyermekkori specifikus allergén immunterápia (allergén vakcináció). Módszertani ajánlás. Gyógyszereink, 2004 (közlésre elfogadva).
- Demoly P, Sahla M, Cambell AM, Bousquet J, Crampette L: ICAM-1 expression in upper respiratory mucosa in differentially related to eosinophil and neutrophil innflammation according to the allergic status. Clin Exp Allergy 1998;731-8.
- Devalia JL, Bayram H, Rusznak C, Calderón M, Sapsford RJ, Abdelaziz MA, Wang J, Davies RJ: Mechanisms of pollution-induced airway disease: in vitro studies in the upper and lower airways. Eur J Allergy Clin Immunol 1997;52 (suppl 38):45-51.
- Didier A, Mazieres J, Kouevijin et al.: Sport and atopy. Rev. Mal. Respir. 2003;20:5, 727-34.
- Dixon M, Jackson DM, Richards IM: The action of sodium cromoglycate on c-fibre endings in the dog lung. Br J Pharmacol 1980;70:11.
- Dolz I, Martinez-Cocera C, Bartolome JM, Cimarra M: A double -blind placebo controlled study of immunotherapy with grass-pollen extract Alutard SQ during a 3-year period with initial rush immunotherapy Allergy 1996;51:489-500.
- Durham SR, Sun Ying, Varney VA: Cytokine messenger RNA expression for IL-3, IL-4, IL-5, and granulocyte/macrophage-colony stimulating factor in the nasal mucosa after local allergen provocation: relationship to tissue eosinophilia. J Immunol 1992;148:2390-94.
- Farkas H, Hirschberg A, Krasznai M, Szabó I, Liktor B, Sziklai I, Pánczél Gy, Kun Zs, Bitay Zs, Naményi M, Vinkler I, Zibotics H, Harsányi E, Molnár GE, Vincze Á, Fényi Á, Rónai Z: Desloratadin hatékonyságának és tolerálhatóságának multicentrikus vizsgálata szezonális allergiás rhinitisben. Orv Hetil 2003;144(21):1021-1024.
- Fleming DM., Crombie DL: Prevalence of asthma and hay fever in England and Wales. Br Med J 1987;294:279-283.
- Forsyth RD, Cole P, Shephard RJ: Exercise and nasal patency. J Appl Physiol 1983;55:860-865.
- Graf P: Overuse of oxy- and xylometazoline nasal sprays. Thesis. Stockholm, 1994. Graf P, Juto JE: Decongestion effect and rebound swelling of the nasal mucosa during 4-week use of oxymetazoline. ORL 1994;56:157-160.
- Hamilos DL, Leung DYM, Wood R, Cunningham L, Bean DK, Yasruel Z, Schotman E, Hamid Q. Evidence for distinct cytokin expression in allergic versus non-allergic chronic sinusitis. J Allergy Clin Immunol 1995;96:537-544.
- Harding SM, Heath S: Intranasal steroid aerosol in perennial rhinitis: comparison with an antihisztamine compound. Clin Allergy 1976;6:369.
- Herjavecz I, Böszörményi-Nagy Gy: Provocation tests with aspirin and food additives in patients with non-allergic asthma. Proceedings of the International Union of Physiological Sciences. XIV. 1980, 470.
- Hirschberg A (szerk.): Rhinitis. Egyeztetett hazai állásfoglalás és ajánlás a rhinitis diagnosztikájához és kezeléséhez. LAM 1998;8(Suppl 1):6-31.
- Hirschberg A: Rhinoconjunctivitis allergica. Medicus Anonymus 1999; Melléklet 7(5):13-16.
- Hirschberg A: A rhinitis allergica kezelési algoritmusa napjainkban. Gyógyszereink 2000;50:101-109.
- Hirschberg A (szerk.): Rhinitis. Egyeztetett hazai állásfoglalás és ajánlás a rhinitis diagnosztikájához és kezeléséhez 2001; AstraZeneca Kft. Budapest.
- Hirschberg A: Tudományos értékelés a XVIII. Nemzetközi Allergológiai és Klinikai Immunológiai kongresszusról. LAM 2003;13(7):572-574.
- Jacobs RL: Non-allergic chronic rhinitis syndromes. Immunol Allergy Clin North Am 1987;7:93.
- Jokinen K, Sipilä P: Intranasal ipratropium in the treatment of vasomotor rhinitis. Rhinology 1983;21:341.
- Kadocsa E: Az allergiás eredetű nátha prevalenciájának meghatározása Szegeden (1993).ˇFül-orr-gégegyógyászat 1994;39:182-188.
- Katelaris CH, Carrozzi FM, Burke TV et al.: A springtime olimpics demands special consideration for allergic ethlets. J. Allergy Clin. Immunol. 2000;106:2, 260-6.
- Karlsson G, Holmberg K: Does allergic rhinitis predisposes to sinusitis? Acta Otolaryngol Suppl 1994;515:26-8; discussion 9.
- Keith PK, Conway, Evans S, Edney P, Jennigs B, Andersson B, Dolovich J: A doubleblind comparison of intranasal budesonide dry powder vs placebo in nasal polyposis. J Allrgy Clin Immunol 1995;95:204 (Abstract).
- Khinch MS, Poulsen LK, Carat F, André C, Hansen AB, Malling HJ: Clinical efficacy of sublingual and subcutaneous birch pollen allergen-specific immunotherapy: a randomized, placebo-controlled, double-blind, double-dummy study. Allergy 2004;5945-50.
- Kjellman N-IM: Prevention of allergy-myth or reality? In: Godard Ph, Bousquet J, Michel FB: Advances in allergology and clinical immunology 1992;401-414. (Carnforth: The Parthenon Publishing Group)
- Leynaert B, Bousquet J, Neukirch C. et al.: Perennial rhinitis: An independent risk factor for asthma in nonatopic subjects: Results from the European Community Respiratory Health Survey. J Allergy Clin Immunol 1999:301-4.
- Lund VJ et al.: International Consensus Report on the Diagnosis and Management of Rhinitis. Eur J Allergy Clin Immunol (Suppl) 1994;49:5-34.
- Mackay I: Rhinitis Mechanisms and management. Royal Society of Medicine Services Limited, London 1989.
- Malling HJ, Weeke B: EAACI Position Paper. Immunotherapy Allergy 1993;48 (Suppl. 14):1-35.
- Malm L, Anggärd A: Vasoconstrictor. In: Mygind N, Naclerio RM, eds. Allergic and non-allergic rhinitis. Clinical aspects. Copenhagen: Munksgaard, 1993:95-100.
- Mann RD, Pearce GL, Dunn N, Shakir S: Sedation with „non-sedating” antihistamines: four prescription-event monitoring studies in general practice. BMJ 2000;320:1184-1187.
- Marby RL: Rhinitis of pregnancy. Southern Med J 1986;79:965-71.
- Mc Fadden Jr. ER: Physiological and pathological interaction between the upper and lower airways and bronchial asthma. In: Mygind N, Pipkorn H, Dahl R eds.: Rhinitis and Asthma: similarities and differences. Copenhagen, Munksgaard, 1990;139.
- Mezei G, Magyar P, Cserháti E, Márk Z: A double-blind, placebo-controlled parallel study to assess the efficacy of preseasonal sublingual ragweed (Ambrosia artemisiifolia) specific immunotherapy. Notizario allergologico 1996;15(Suppl):40-45.
- Mezei Gy, Cserháti E, Kelemen J, Lendvay M, Póder Gy: A gyermekkori szénanátha. Gyermekgyógyászat 1986;37:443-449.
- Mezei Gy, Járainé Komlódi M, Medzihradszky Zs, Cserháti E: Szezonális allergiás rhinitis és pollenszám (ötéves felmérés Budapesten). Orv Hetil 1995;136:1721-1724.
- Mezei Gy, Cserháti E, Pusztai A: Atkaölő szer hatása a háziporra és a házipor-allergiások tüneteire. Orv Hetil 1994;135:969-72.
- Mezei Gy: Anamnesztikus adatok és összehasonlító légzésfunkciós vizsgálatok a gyermek szénanáthájában. Kandidátusi értekezés, 1987.
- Mogi G. Tomonaga K, Watanabe T, Chaen T: The role of type I allergy in secretory otitis media and mast cells in the middle ear mucosa. Acta Otolaryngol Suppl 1992;493:155-63.
- Mohun M: Incidence of vasomotor rhinitis during pregnancy. Arch. Otolaryngol. 1943;37:699-709.
- Moller C, Dreborg S, Ferdousi HA, Halken S, Host A, Jacobsen L, Koivikko A, Koller DY, Niggemann B, Norberg LA, Urbanek R, Valovirta E, Wahn U: Pollen immunotherapy reduces the development of asthma in children with seasonal rhinoconjunctivitis (the PAT-study). J Allergy Clin Immunol. 109:251-256. (2002)
- Moretti ME, Caprara D, Coutinho CJ, Bar-Oz B, Berkovitch M, Addis A, Jovanovski E, Schüler-Faccini L, Koren G: Fetal safety of lortadine use int he first trimester of pregnancy: A multicenter study. J Allergy Clin Immunol 2003;111:479-83.
- Mortimer H., Wright RP., Collip JB: The effect of the administration of oestrogenic hormones on the nasal mucosa of the monkey. Can. Med. Assoc. J. 1936;35:503-513.
- Mygind N, Borum P: Anticholinerg treatment of watery rhinorrhoea. Am J Rhinol 1990;4:1-5.
- Mygind N, Dahl R, Pedersen S, Thestrup-Pedersen K: Essential Allergy. Second edition Blackwell Science, London, 1996.
- Mygind N, Naclerio RM (eds): Allergic and Non-allergic Rhinitis. Copenhagen, Munksgaard, 1993.
- Mygind N, Pedersen M, Nielsen MH: Morphology of the upper airway epithelium. In: Proctor DF, Andersen I eds: The nose: upper airway physiology and the athmospheric enviroment. Amsterdam, Elsevier 1982.
- Mygind N, Pipkorn H, Dahl R eds.: Rhinitis and Asthma: Similarities and Differences. Copenhagen, Munksgaard, 1990;256-57.
- Mygind N, Weeke B: Allergic and Vasomotor Rhinitis. Copenhagen, Munksgaard, 1985.
- Mygind N: Glucocorticoids and rhinitis. Allergy 1993;48:476.
- Mygind N: Treatment of nasal allergy in children. In: Van Cauwenberge P ed.: Immunological and allergological item in pediatric otorhinolaryngology Amsterdam, Kugler Publications, 1991;1-3.
- Naclerio RM, Proud D, Togias AG: Inflammatory mediators in late antigen induced rhinitis. N Engl J Med 1985;313:65-70.
- Okuda M, Ohnishi M, Ohtsuka H: The effect of cromolyn sodium on the nasal mast cell. Ann Allergy 1985;55:721.
- Ortolani C, Ispano M, Pastorello E, Bigi A, Ansaloni R: The oral allergy syndrome. Ann Allergy 1988;61:47-52.
- Osguthorpe D, Reed S: Neonatal respiratory distress from rhinitis medicamentosa. Laryngoscope 1987;97:829-831.
- Pajno GB, Vita D, Parmiani S, Caminiti L, La Grutta S, Barberio G: Impact of sublingual immunotherapy on seasonal asthma and skin reactivity in children allergic to Parietaria pollen treated with inhaled fluticasone propionate. Clin Exp Allergy 33 1641. (2003.)
- Pariente PD, LePen C, Los F, et al.: Quality-of-life outcomes and the use of antihistamines in a French national population-based sample of patients with perennial rhinitis. Pharmacooeconomics 1997;12:585-95.
- Peddersen PA, Weeke ER: Allergic rhinitis in Dannish General Practice. Allergy 1981;36:375-379.
- Position statement on nasal polyps. Rhinology 1994;32:126.
- Ramsdale EH, Morris MM, Roberts RS, Hargreave FE: Asymptomatic bronchial hyperresponsiveness in rhinitis. J Allergy Clin Immunol 1985;75:573.
- Reisman RE, Berstein J: Allergy and secretory otitis media: clinical and immunologic study Pediatric Clin North Am1975;22:251-7.
- Rimpela AH, Savonius B, Rimpela MK, Haahtela T: Asthma and allergic rhinitis among adolescents in 1977-1991. Scand J Soc Med 1995;23:60-65.
- Rowe-Johnes J., Mackay I.: Management of sinusitis. Sinusitis and rhinitis, or rhinosinusitis? BMJ 1995;310-670.
- Ruhno J, Howie K, Anderson M, Andersson B, Vanzieleghem M, Hitch D, Lapp P, Denburg J, Dolovich J. The increased number of epithelial mast cells in nasal polyps and adjacent turbinates is not allergy-dependent. Allergy 1990;45:370-374.
- Ruokonen J, Holopainen E, Palva T, Backman A: Secretory otitis media and allergy With special reference to the cytotoxic leukocyte test. Allergy 1981;36:59-68.
- Schatz M, Zeigler RS: Diagnosis and management of rhinitis during pregnancy. Allergy Proc 1988;9:545-54.
- Schiff M: The „Pill” in Otolaryngology. Transactions of the American Academy of Ophtalmology and Otolaryngology 1968;72:76-84.
- Seppey M, Krayenbuhl M, Simmon D, Buvelot J-M, Pelloni R: Benefits and prospects of rhinomer in the treatment of nasosinusal pathologies. ORL Highlights 1995;2:20-24.
- Settipane RJ, Hagy GV, Settipane GR: Long-term risk factors for developing asthma and allergic rhinitis: a 23-year follow-up study of college students. Allergy-Proc 1994;15:21-25.
- Shamsi Z, Hindmarch Z: Sedation and Antihistamines: A Review of Inter-Drug Differences using Proportional Impairment Ratios. Hum Psychopharmacol 2000;15:3-30.
- Sibbald B, Rink E: Epidemiology of seasonal and perennial rhinitis: clinical presentation and medical history. Thorax 1991;59:17-21.
- Sibbald B: Epidemiology of allergic rhinitis. In: Burr ML ed.: Epidemiology of clinical allergy. Monographs in allergy. Basel, Karger, 1993;61-79.
- Siegel SC: Rhinitis in children In: Mygind N, Naclerio RM eds. Allergic and non-allergic rhinitis. Clinical aspects. Copenhagen: Munksgaard 1993;174-83.
- Small P, Barrett D, Frenkiel S, Rodhon L, Cohen C, Black M. Local specific IgE production in mnasal polyps associated with negative skintests and serum RAST. Ann Allergy 1985;55:736-739.
- Smith IM: Epidemiology and natural history of asthma, allergic rhinitis and allergic dermatitis. In: Middleton E, Reed CE, Ellis EF eds. Allergy: principles and practice. 2nd ed. St Louis, CV Mosby, 1983;771-804.
- Sorri M, Hartikainen-Sorri AL, Karja J: Rhinitis during pregnancy. Rhinology 1980;18:83-86.
- Stachan D., Sibbald B., Veiland S. et al.: Worldwide variations in prevalence of symptoms of allergic rhinoconjunctivitis in children: the International Study of Asthma and Allergies in Childhood (ISAAC). Pediatr. Allergy Immunol 1997;8:161-176.
- Stjärne P, Lundblad L, Änggard A, Lundberg JM: Local capsaicin treatment of the nasal mucosa reduces symptoms in patients with nonallergic nasal hyperreactivity. Am J Rhinol 1992;5:145-151.
- Tomonaga K, Kurono Y, Mogi G: The role of nasal allergy inotitis media with effusion: a clinical study. Acta Otolaryngol 1988;458 (suppl):41-47.
- Toppozada H, et al.: The human respiratory nasal mucosa in pregnancy. An electron microscopic and histochemical study. J Laryngol Otol 1982;96:613-26.
- Van Cauwenberge P et al.: EAACI Consensus statement on the treatment of allergic rhinitis. Allergy 2000;55:116-134.
- Van Cauwenberge P: Recent development of anti-allergic drugs. Rhinology 1992;(Suppl. 14.):67-71.
- Varney VA, Gaga M, Frew AJ, Aber VR, Kay AB, Durham S: Usefulness of immunotherapy in patients with severe summer hay fever uncontrolled by antiallergic drugs. BMJ 1991;302:265-69.
- Vóna I: Immunotherapy for House Dust Allergy. Clinical Otolaryngology 22:52-56. (1997)
- Warner JO, Price JF, Soothill JF, Hey EN: Controlled trial of hyposensitization to Dermatophagoides pteronyssinus in children with asthma. Lancet 1978;2:913-15.
- Watson-Williams E: Endocrines and the nose. J Laryngol Otol 1952;66:29-38.
- Weeke ER: Epidemiology of hay fever and perennial allergic rhinitis. Monogr. Allergy 1987;21:1-20.
- Weeke ER: Epidemiology of allergic and non-allergic hypersensitivity. „The world of allergies”. Brussels, 1993; Abstr. 24pp.
- Weeke ER: Epidemiology of allergic diseases in children. Rhinology 1992;13(Suppl):5-12.
- Welsh PW, Stricker WE, Chu-Pin C et al.: Efficacy of beclomethason nasal solution, fluticasone and cromolyn in relieving symptoms of ragweed allergy. Mayo Clin Proc 1987;62:125.
- Wolf G: Neue Aspekte zur Pathogenese und Therapie der hyperreflektorischen Rhinopathie. Laryng Rhinol Otol 1988;67:438-445.
- Wüthrich B, Schindler C, Leuenberger P, Ackermann U: Prevalence of atopy and pollinosis in the adult population of Switzerland. Int Arch Allergy Immunol 1995;100:149-156.
- Wüthrich B, Schyder UW, Henauer SA, Heller A: Häufigkeit der Pollinosis in der Schweiz. Ergebnisse einer representativen demoskopischen Umfrage unter Berücksichtigung anderer allergischer Erkrankungen. Schweiz Med Wschr 1986;116:909-917.
Az irányelvről további információk kérhetők:
Fül-orr-gégészeti Szakmai Kollégium
dr. Z. Szabó László
Országos Gyógyintézeti Központ
Budapest, Szabolcs u. 33-35.;
E-mail: zszabo@hiete.hu | Tüdőgyógyászati Szakmai Kollégium
dr. Böszörményi Nagy György
Országos Korányi TBC és Pulmonológiai Intézet
Budapest, Pihenő út 1.
E-mail: bngy@koranyi.hu |
Az irányelvet szerkesztette: dr. Hirschberg Andor
Az irányelvet írták: dr. Böszörményi Nagy György, dr. Herjavecz Irén, dr. Hirschberg Andor, dr. Kadocsa Edit, dr. Katona Gábor, dr. Mezei Györgyi, dr. Tóta Julianna, dr. Vóna Ida, dr. Z. Szabó László





