|
|
 A pulmonalis hipertónia diagnózisa és kezelése Kardiológiai Szakmai Kollégium • 2004 Írta: Karlóczai Kristóf Definíció Pulmonalis artériás hipertóniáról akkor beszélünk, ha a pulmonalis átlagnyomás 25 Hgmm-nél és a pulmonalis vascularis ellenállás 3 Wood-egységnél magasabbra emelkedik (PAPm>25 Hgmm és PVR> 3WU), miközben a PCW<15 Hgmm marad. A háttérben az a jól ismert élettani jelenség húzódik meg, hogy a PAPsy normális esetben terhelésre sem emelkedik 40 Hgmm fölé, mert a véráramlás fokozódásakor új tüdőterületeknek a véráramlásba való bekapcsolódásával a pulmonalis rezisztencia csaknem konstans marad. PH esetén ez a platóképződés megszűnik, és a nyomásértékek fokozatosan kóros tartományba emelkednek. Ha a pulmonalis hipertónia csak terhelésre manifesztálódik, rejtett vagy szubklinikus PH-ról beszélünk. Epidemiológia, lefolyás Sokfajta pulmonalis hipertóniát ismerünk (lásd később), ezek közül az idiopathiás forma ritka betegség, de mégis ennek előfordulását regisztrálják és hasonlítják össze területenként. Incidenciája 1-2/1 M. A fizikai terhelhetőség fokozatos beszűkülésével jár, a diagnózis utáni várható élettartam 2,8 év. A nők mintegy kétszer gyakrabban érintettek, a betegség rendszerint fiatalkorban jelentkezik (nőknél 20-30 év, férfiaknál 30-40 év) (2). A más betegségekhez társuló formák incidenciája a szűrési stratégiáktól függ. Patológia Elsősorban intimaproliferáció, mediahipertrófia és adventitiaproliferáció utal az artériák betegségére. A különféle formákban nem biztos, hogy azonos a patofiziológia. Három faktor okozhat fokozott PVR-t: vasoconstrictio, a tüdőér falának remodellálódása és az in situ trombózisok. A vasoconstrictio csak igen ritkán oka a betegségnek. Feltételezett mechanizmus: - A keringő vasoconstrictor anyagok intracellulárisan felszaporodnak (tromboxán, szerotonin);
- endothelin felszaporodása;
- endotheliumfüggő vasodilatatorok csökkenése (PGI2, NO, EDHF [Endothelium-Derived Hyperpolarizing Factor]);
- csökkent Ca-sequestratio a sarcoplasmás reticulumban;
- K-kiáramlás csökken, Ca-beáramlás nő;
- Na-Ca ionpumpa csökken;
- Az aktin és a miozin Ca-érzékenysége nő;
- a prosztaciklin-szintetáz kiválasztása csökken;
- BMPR2 gén mutációja gyakori (familiáris forma), de ebben környezeti és szomatikus hatások is szerepet játszanak;
- az angiopoetin kiválasztása nő, ekkor az aktivitás mértéke arányos a PAH súlyosságával.
Klinikailag manifeszt pulmonalis hipertóniában a PAPm átlagos értéke 60 Hgmm, a PVRI átlagban 20 WU. Rövidítések jegyzéke | 6MWD: | 6 perces járóterhelés során megtett távolság | | 6MWT: | 6 perces járóterhelés | | ACA: | anti centromer antitest | | AcT: | akcelerációs idő | | AKH: | Allgemeines Krankenhaus (Bécs) | | ANA: | antinukleáris antitest | | ANP: | agyi natriureticus peptid | | APm: | arteria pulmonalis középnyomás | | APsy: | pulmonalis szisztolés nyomás | | BK: | bal kamra | | BMPR2: | bone morphogenetic protein receptor, type II (serine/threonine kinase) | | BNP: | pitvari natriureticus peptid | | CCB: | kalciumcsatorna-blokkoló | | CI: | cardiac index (szívindex) | | COPD: | krónikus obstruktív légúti betegség | | CREST: | calcinosis cutis, Raynaud-szindróma, oesophagusmotilitasi zavar, scleroderma, teleangiectasiák | | DLCO: | szén-monoxid diffúziós kapacitás | | DLTX: | kétoldali tüdőtranszplantáció | | dsDNA: | double-stranded DNA (DNS kettős spirál) | | EDHF: | endothelium-derived hyperpolarizing factor | | ENA: | extractable nuclear antigens (extrahálható nuclearis antigének elleni antitest) | | ERA: | endothelin receptor antagonista | | ET: | Endothelin | | FEV1: | forszírozott kilégzési térfogat | | HIV: | humán immundeficiencia vírus | | HRCT: | nagyfelbontású komputertomográfia | | HUH: | hasi ultrahang | | ILD: | interszticiális tüdőbetegség | | IPAH: | idiopathiás pulmonalis hipertónia | | IVS: | interventricularis septum | | JK: | jobb kamra | | JP: | jobb pitvar | | NIH: | National Institute of Health | | NO: | nitrogén-monoxid | | OSA: | obstruktív alvási apnoe | | PaCO2: | szén-dioxid parciális nyomása | | PaO2: | oxigén parciális nyomása | | PAPm: | pulmonalis artériás átlagnyomás | | PAPsy: | pulmonalis artériás szisztolés nyomás | | PCW: | pulmonalis kapilláris éknyomás | | PDE5: | foszfodiészteráz-5 gátló | | PE: | pulmonalis embolia | | PGI2: | prosztaglandin I2 | | Pm-Scl: | polymyositis/scleroderma antigén | | PPHN: | újszülöttkori primer pulmonalis hipertenzió | | PVOD: | venoocclusiv pulmonalis betegség | | PVR: | pulmonalis vascularis rezisztencia | | RNP: | extractable nuclear antigens | | RVET: | jobb kamrai ejekciós idő | | SLE: | szisztémás lupus erythematosus | | SLTX: | egyoldali tüdőtranszplantáció | | SSS: | Stiff skin syndrome (scleroderma) | | TEE: | transoesophagealis echokardiográfia | | TnT: | troponin T | | TR: | tricuspidalis regurgitatio | | TTE: | transthoracalis echokardiográfia | | TVI: | transvelocity integral | | VO2: | Oxigénfogyasztás | | VWF: | Von Willebrand-faktor | | WU: | Wood-egység | Felosztás (a WHO 2003-as velencei szimpóziuma alapján) 1. Pulmonalis artériás hipertónia: - idiopathiás PAH (IPAH);
- familiáris PAH;
- más betegségekkel, ill. gyógyszerhatással kapcsolatos PAH:
- kötőszöveti betegségek;
- HIV;
- portalis hipertónia;
- anorexigen szedése (fenfluramin);
- veleszületett szívbetegségek;
- PPHN (újszülöttkori idiopathiás pulmonalis hipertónia);
- PAH venula/kapilláris érintettséggel (PVOD).
2. PH balszívfél-betegséggel: - pitvari, illetve kamrai érintettség;
- valvularis érintettség.
3. PH tüdőbetegségekkel/hypoxiával: - COPD;
- interszticiális tüdőbetegségek;
- alvási apnoe szindróma;
- fejlődési zavarok.
4. Krónikus trombotikus és/vagy embóliás betegségek melletti PH: - proximalis tüdőartériák thromboemboliás obstrukciója;
- distalis tüdőartériák thromboemboliás obstrukciója;
- nem trombotikus tüdőembolisatio.
Diagnosztikus stratégia Klinikai gyanú: - ismeretlen effort dyspnoe, különösen fiataloknál, ha ennek hátterében nincs ismert szív- vagy tüdőbetegség;
- syncope (késői jel);
- angina (késői jel);
- fizikális jelek - nagy gyakorlatot igényel a felismerésük:
- hangos P2;
- tiszta tüdőhangok;
- jobb kamrai eredetű III., ill. IV. hang, TR zöreje;
- emelkedett vena jugularis nyomás;
- ödéma, ascites;
- rendszerint PH-val járó más betegség diagnózisa;
- véletlenszerűen készített EKG vagy mellkasröntgen, ami PH-ra utal.
Felismerés: EKG, mellkasröntgen, TTE - mellkasröntgen (érzékeny, de nem specifikus):
- 90%-ban kóros;
- JK-, JP-megnagyobbodás jelei;
- a proximalis tüdőartériák dilatáltak;
- perifériás érszegénység;
- EKG (érzékeny, de nem specifikus): jobb pitvari, jobb kamrai terhelés, ill. hipertrófia jelei, V1-ben jobbszár-blokk, intrinsicoid deflection kiszélesedése;
- echokardiográfia
echokardiográfiás definíció: - enyhe PH: TR max. seb 2,8-3,4 m/s (PAsy 36-50 Hgmm);
- JK-dilatáció (JP is), hipokinézis, hipertrófia;
- IVS paradox mozgás, D-jel (excentricitási index);
- BK kicsi;
- pericardialis folyadék;
- VCI-dilatáció;
- Doppler:
- JK-ejekció (AcT, RVET);
- BK-ejekció (TVI);
- TR: sebesség, szélesség, área;
- BK-telődés (E, A, E/A, TVI).
A magas érzékenység és fajlagosság ellenére gondolni kell az álpozitív Doppler-vizsgálat (1) és az álnegatív echó (2) lehetőségére. Osztályozás Differenciáldiagnosztikai lépések az alábbiak kizárására: - balszívfél-betegségek (EKG, echó);
- tüdőbetegségek (röntgen, spirometria, vérgáz);
- krónikus thromboemboliás betegségek (tüdőperfúzió, pulmonalis angiográfia);
- kötőszöveti betegségek (immunológiai vizsgálatok).
- COPD esetén a PAH arányos a spirometriával mérhető térfogat-redukcióval, a nyomások csak közepesen emelkedettek.
- Interszticiális tüdőbetegségben lehet igen magas a nyomás.
- Enyhe PH és WHO I. funkcionális állapotban elegendő az autoimmun (CREST) betegségek kizárása, majd kontroll 6 havonta.
- Enyhe PH és WHO III-IV. funkcionális állapotban: jobbszívfél-katéterezés.
- Congenitalis betegség gyanújakor: TEE és kontraszt echó.
- Kötőszöveti betegségek gyanúja esetén: immunológiai vizsgálatok.
- HIV-vizsgálat.
- Portalis hipertóniában: HUH.
- Genetikai vizsgálatok (BMPR2-mutációk) - csak kutatási célokra.
Légzésfunkciók és vérgázvizsgálatok különféle eredetű PH-ban | PAH | COPD | ILD |
|---|
| tüdővolumenek =/↓ | tüdővolumenek ↑ | tüdővolumenek ↓↓ |
|---|
| DLCO ↓ 60-80% | FEV1 ↓ | DLCO ↓↓ |
|---|
| PaO2 =/↓ | DLCO ↓ | PaO2 ↓ |
|---|
| PaCO2 =/↓ | PaO2 ↓ | PaCO2 =/↑ |
|---|
| PaCO2 =/↑ | |
|---|
Funkcionális megítélés, hemodinamika - 6 perces járás terhelés. Olcsó, egyszerű és számos vizsgálat primer végpontjában szereplő vizsgálat, de csak a betegre és az asszisztensre vonatkozó speciális szabályok betartásával reprodukálható. Ideális a 30 m-es jelzett folyosó.
- Cardiopulmonalis terheléses vizsgálatok. Légvételről légvételre méri terhelés közben a spirometriás paramétereken túl a kilégzett levegő parciális oxigén- és szén-dioxid-nyomását. Ezekből számos metabolikus paraméter származtatható (részletesen lásd a Szívtranszplantációs kivizsgálás ajánlásában).
- Swan-Ganz-katéterezés. A pulmonalis keringés nyomás- és áramlásadatait megbízhatóan invazív úton nyerhetjük termodilúciós perctérfogatméréssel. A katétert a vena jugularison át a pulmonalis főágba juttatjuk. Az alapadatokból prognosztikai információt nyerhetünk. Ezen túl igen fontos és terápiás következménye van a vazoreaktivitási vizsgálatnak (lásd később). A módszerrel megbízhatóan tesztelhetünk gyógyszereket és ellenőrizhetjük a hatásuk tartósságát.
Diagnosztikai algoritmus 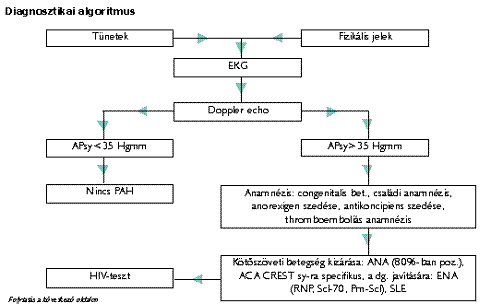
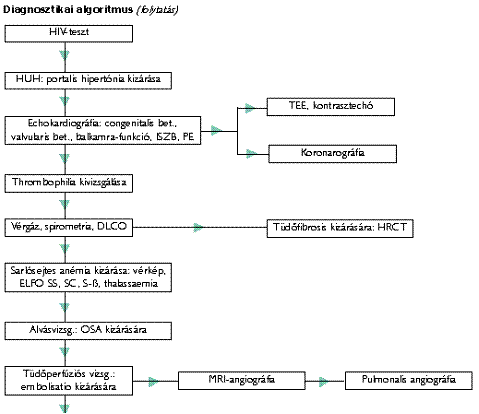
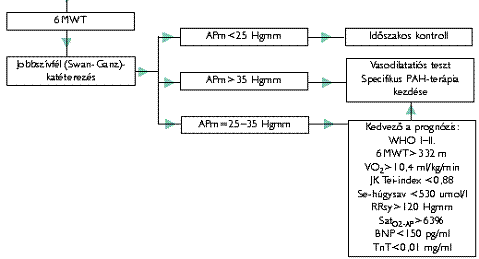
Prognózis meghatározása Nagy jelentőségű, hogy a PAH súlyosságát meghatározzuk az optimális terápia és a megfelelő kiválasztás érdekében (gyógyszerek, septostomia, transzplantáció). Számos vizsgálatnak ismert a prognosztikai értéke, de ezek az idiopathiás formában használhatók, és nem alkalmasak kötőszöveti betegségben, congenitalis szívbetegségben, anorexigenekkel, HIV-fertőzéssel vagy portalis hipertóniával kapcsolatos PAH esetén. Így ezeket a paramétereket csak nagy óvatossággal lehet olyan betegeken alkalmazni, akiknél több tényező, ill. betegség együttesen határozza meg a télélést. A legsúlyosabb prognózisa a kötőszöveti betegségek melletti PAH-nak van, ennél valamivel jobbak az esélyek az idiopathiás formában, míg a congenitalis szívbetegségek mellett a legjobbak kilátások, leglassúbb a progresszió. Az ET prognosztikai faktor: minél magasabb a szintje, annál rosszabb a túlélés. SSS esetén a túlélés erősen függ attól, hogy van-e tüdőmanifesztáció, és különösen attól, hogy van-e PAH, ami mintegy 20%-ban fordul elő. A perctérfogat és a pulmonalis nyomás nem párhuzamosan változik: a preklinikai stádiumban a nyomás fokozatosan emelkedik, aztán stagnál, és a végstádiumban sem a csökkenés, sem a növekedés nem jellemző, ekkor a perctérfogat viszont csökkenni kezd. Terminálisan a nyomásértékek normalizálódnak. A prognózist befolyásolja a funkcionális kapacitás, a terheléses vizsgálat, a Swan-Ganz-katéterezés eredménye, az echokardiográfia, ill. Doppler-adatok és biokémiai markerek. A WHO szerinti funkcionális állapot alapvetően determinálja a prognózist, a IV. funkcionális osztály túlélése sokkal alacsonyabb, mint a II. és a III. osztályé. A 6 perces járóterhelés jól korrelál a klinikai lefolyással. A 332 m-nél kevesebbet teljesítők prognózisa jelentősen rosszabb a hosszabb távot járóknál. Ez párhuzamos a maximális O2-fogyasztással szívelégtelenségben. (1) A betegségben az 1, 3, ill. 5 éves túlélés 68%, 48%, 34% a NIH-regiszter szerint.(2) Az epoprostenol ezt javítja: 85-88%, 63%, illetve 47-55%-ra. (3, 4) Multivariáns analízis szerint az 1 éves túlélést PGI2-kezelés mellett elsősorban a 10,4 ml/kg/min alatti maximális VO2 és a 120 Hgmm alatti terheléses szisztolés vérnyomás határozza meg. Ugyancsak prognosztikai céllal használható a szérum húgysavszintje is: 530 mmol/l érték fölött a prognózis rosszabb. (5) Az invazív hemodinamikai mérések szintén prognosztikai információt nyújtanak: ha a kevert vénás vér O2-szaturációja 63% alatti, a 3 éves túlélés 17%, szemben az e fölötti csoportban talált 55%-kal. Az echokardiográfiás paraméterek közül a pericardialis folyadék, a jobbpitvar-megnagyobbodás, a septum balra helyezettsége és a Tei-index jelzik a jobbszívfél-elégtelenség súlyosságát. (6, 7) Biokémiai markerek PAH esetén: - Endotheliumdiszfunkció: ET-1, PGI2, NO
- Thrombocyták/koaguláció: tromboxán, szerotonin, VWF, D-dimer
- Neurohormonális aktiváció: KA, PRA, AT
- Metabolikus/szöveti perfúziós jel: húgysav
- Szívmyocyták: ANP, BNP, szív-Tn
A kiindulási BNP 150 pg/ml alatti szintje, mely 3 hónap után sem emelkedik 180 pg/ml fölé, szignifikánsan jobb prognózisra utal. (8) Hasonlóan a TnT is prognosztikai marker: 0,01 mg/ml fölötti szintje már fél év után is szignifikánsan alacsonyabb túlélésre utal. (9) Tüdőbiopszia sem a diagnosztikához, sem a prognosztikai besoroláshoz nem javasolt, veszélye meghaladja a leletből nyerhető előnyöket. Terápiás algoritmus Az utóbbi 20 évben javultak a terápiás eredmények, ami a betegek sokkal kedvezőbb életkilátásaiban mutatkozik meg. A 80-as években még a hagyományos kezelést egyedül az antikoagulálás jelentette. 1981 óta érhető el a szív-tüdő transzplantáció. Nagy dózisú CCB-kezelést 1992 óta alkalmazunk. 1996-ban került be a klinikai gyakorlatba a folyamatos iv. PgI2-kezelés. (10) 2000-től számíthatjuk a legújabb korszakot, amelyben az ERA (bosentan, ambrisentan), a prosztanoidok (treprostinil, beraprost, iloprost) és a PDE-5 gátlók (sildenafil) játsszák a fő szerepet, de az epoprostenolkezelésnek ma is van létjogosultsága. (11) Újabb kezelési lehetőségek - Stabil prosztaciklinanalógok:
- iloprost (inh.);
- treprostinil (sc.);
- beraprost (orális).
- Más szerek:
- tromboxán A2 gátló (terbogrel);
- endothelin 1 gátló (bosentan, sitaxentan, ambrisentan);
- foszfodiészteráz gátló (sildenafil);
- nitrogén-oxid, L-arginin.
A legnagyobb terápiás sikereket a kombinációs kezelésekkel lehet elérni. A betegek számára lényeges kényelmi szempont, ha orális vagy inhalációs kezelésekkel, ill. ezek kombinációjával sikerül az invazív adagolással megegyező vagy annál hatásosabb eredményt elérni. Ajánlott a gyógyszeres kezelés idejében való elkezdése, így a prognózis javul és a transzplantáció is elkerülhető.. A nagy összegű kezelések költségeit e betegeknek egyedileg kell biztosítani. PAH kezelésében randomizált, kontrollált vizsgálatokkal igazolt szerek | Kezelés | Alkalmazás módja | Fő hátrány | RCT-vizsgálatok száma | Az evidencia erőssége | Törzskönyvezés |
|---|
| EPO | iv. (folyamatos) | szepszis kockázata nő | 3 | A | USA, Kanada,Európa, Japán |
|---|
| Treprostinil | sc. (folyamatos) | helyi fájdalom | 2 | B | USA |
|---|
| Iloprost | inhaláció (6-8x/nap) | rövid hatás | 1 | B | Európa |
|---|
| Beraprost | p. os (napi 4x) | flush, fejfájás | 2 | B | Japán |
|---|
| Bosentan | p. os (napi 2x) | májenzim-emelkedés | 2 | A | USA, Kanada,Európa |
|---|
| Sitaxsentan | p. os (napi 1x) | májenzim-emelkedés | 1 | B | - |
|---|
| Ambrisentan | p. os (napi 1x) | májenzim-emelkedés | 1* | - | - |
|---|
| Sildenafil | p. os (napi 3x) | látási/színlátási zavarok | 1* | C | - |
|---|
| L-arginin | p. os (napi 3x) | gastrointestinalis intolerancia | 1* | - | - |
|---|
*Folyamatban újabb RCT. PAH kezelésében szóba jövő, de randomizált, kontrollált vizsgálatokkal nem igazolt szerek, ill. eljárások | Kezelés | Adagolás módja | Fő hátránya | Vizsgálatok száma | Betegpopuláció | Evidencia foka |
|---|
| CCB | orális | perifériás ödéma | 5 | IPAH | C |
|---|
| Antikoagulálás | orális | vérzés | 3 | IPAH | C |
|---|
| Szupportív szerek (O2, digoxin, diuretikum) | inhalálás, orális | - | - | - | C |
|---|
| Atrioseptostomia | | beavatkozás kockázata | 4 | IPAH | C |
|---|
| Transzplantáció | | vérzés | 5 | IPAH | C |
|---|
Antikoagulálás PAH-ban (12) Szövettani vizsgálatok trombotikus laesiót mutatnak a kis artériákban. Emellett az endotheldiszfunkció hiperkoagulabilitást okoz. A low output, a vénás stasis, az ülő-fekvő életmód és a lassult tüdővéráramlás miatt a vénás thromboembolia kockázata eleve nagy. Mindezek alapján az antikoagulálás minden betegnél javasolt, holott ennek kedvező hatásáról nem rendelkezünk megfelelő minőségű evidenciával. A Syncumar (warfarin) adagját az INR 2-3 közötti értékéig javasolt feltitrálni. A kezeléstől feltehetően a túlélés javul. Kalciumcsatorna-gátlók PAH-ban A betegeknek csak kis része tartósan responder. Akinél a vasodilatatortesztre a hemodinamikai paraméterek akutan nem javulnak, a hosszú távú kezelésre sem fognak javulni. Az akut teszt CCB segítségével nem javasolt, veszélyes (főleg a non-responderek körében) (13, 14), halálos szövődmények ismertek. Akut vasodilatatiós teszt (15) | Szer | Adagolás módja | Dózis | Felezési idő |
|---|
| Adenozin | iv. | 20-200 ng/kg/min | 5-10 s |
|---|
| Epopros-tenol | iv. | 2-24 ng/kg/min | 3 min |
|---|
| NO | inh. | 10-80 ppm | 15-30 s |
|---|
Responder definíciója A korábbi minimum 20% helyett ma a PAPm jelentős (legalább 10 Hgmm-es, legalább a 40 Hgmm-es értékre történő) csökkenését tekintjük pozitív tesztnek, ha a perctérfogat változatlan vagy növekszik. ΔPAPm ↓ ≥10 Hgmm
PAPm<40 Hgmm
PVR ↓ ≥20%
CO → ↑ Valódi responder: ha hónapok után is kedvező a kezelés hatása (klinikailag és hemodinamikailag) és nem szükséges prosztanoidok és/vagy ERA adása. Egy nagy vizsgálat alapján a betegek 87,4%-a (487/557) non-responder, és csak 12,6%-a (70/557) responder. Közülük is csupán 6,6% a hosszú távú valódi responder (37/557), míg a többieknél a hosszú távon CCB-kezelés sikertelen (33/557) (16). A vasodilatatorteszt során a CCB hosszú távú eredményességét jelzi, ha a PAPm<37 Hgmm, a DPAPm>31%, a PVR<6,7 WU, míg a DPVR>39%. Terápiás algoritmus 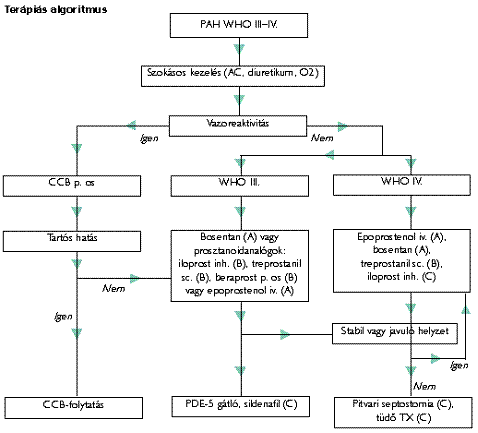
Kezelési algoritmus - Csak WHO III. és IV. stádiumú betegekre korlátozódik, mert WHO I-II. stádiumúakra túl kevés adat áll rendelkezésre. A legtöbb adat IPAH-ra és SSS-hez, ill. anorexigenekhez kapcsolódó PH-ra vonatkozik. Az eredmények más betegcsoportokra való kiterjesztésekor óvatosság szükséges.
- WHO III-IV. betegeket PAH-ra specializálódott köz-pontokba, gyakorlott szakemberekhez kell küldeni.
- Olyan gyógyszerek kerültek be az algoritmusba, amelyek vagy legalább egy országban PAH-ra törzskönyvezettek, vagy más indikációra már rendelkezésre állnak.
- A pozitív akut teszt azt jelenti, hogy a pulmonalis nyomás csaknem normalizálódik, PAPm<40 Hgmm, D>10 Hgmm, miközben a CO normális vagy emelkedett.
- Tartós CCB-hatásról akkor beszélünk, ha több hónapos kezelés után a beteg WHO I. vagy II. stádiumba kerül és marad.
- A legtöbb szakértő véleménye megegyezik abban, hogy az instabil, IV. stádiumú betegeknél az iv epoprostenolkezelést kell előnyben részesíteni.
- III. stádiumú betegeknél az első szer lehet ERA vagy prosztanoidanalóg, de az iv. epoprostenol is megfelelő lehet. Újabban PDE-5 gátló elsőnek történt alkalmazásáról és igen kedvező eredményekről is beszámoltak. (17)
Tüdőtranszplantáció indikációja PAH-ban A gyógyszeres kezelések eredményeképpen az utóbbi évtizedben felére csökkent az IPAH miatti tüdőtranszplantáció száma. (18) A mai gyakorlatban az optimális kezelés melletti non-responderek tekintendők transzplantációs jelölteknek. Nem helyes, ha a gyógyszeres kezelés és a különböző kombinációk addig elhúzódnak, amíg a manifeszt jobbszívfél-elégtelenség miatt a műtéti esélyek már jelentősen romlanak, a posztoperatív időben elhúzódó respiráltatást és ECMO-kezelést igényelve, és az sem, ha a gyógyszeres kezelés helyett, esetleg költségvetési megfontolásból kerül sor a műtétre. Ajánlatos a súlyos betegeket kivizsgálás után várólistára helyezni és a kezelést egyidejűleg elkezdeni, majd szignifikáns javulás, WHO II. stádium elérése esetén levenni őket a listáról. A Nemzetközi Szív- és Tüdőtranszplantációs Társaság adatai szerint (18) a transzplantációs eredmények az IPAH miatti műtéteknél rosszabbak, mint a más indikációjú csoportok esetén. Ezért ilyen betegeket a tüdőtranszplantációs centrumok közül is csak olyanokba szabad küldeni, ahol ennél a betegcsoportnál kellő jártassággal rendelkeznek. Szív-tüdő, SLTX, DLTX eredménye nem különbözik, de a beteg számára nem egyforma terhelést jelent. Így a gyakorlatban a DLTX és a SLTX jön szóba. A tüdőtranszplantációs listázás indikációjának összefoglalása - WHO III. betegnél, ha a 6MWD>332 m: gyógyszeres kezelés javasolt, transzplantációs központba 3 hónapos sikertelen kezelés esetén küldendő.
- WHO IV. betegnél, ha a 6MWD>332 m: kivizsgálás, majd azonnal listára helyezés, gyógyszeres kezelés elkezdése, 3 hónap után jelentős (II. osztályú) javulás után listáról való levétel. Romlás esetén pitvari septostomia jön szóba bridge-műtétként.
- Hemodinamikailag rossz prognózisra utal, ha a jobb pitvari nyomás >15 Hgmm, ha a CI<2 l/min/m2, és ha a vénás oxigénszaturáció <63%.
A tüdőtranszplantáció után a bécsi központban (AKH) az 5 éves túlélés @70%, a műtétre az átlagos várakozási idő 2-6 hónap. Ahol hosszú a várakozási idő (2 év), a várólista mortalitása az 50%-ot is eléri. Pitvari septostomia (19) Palliatív beavatkozás, mely a túlélést javítja, így a beteg nagyobb eséllyel ki tudja várni, amíg a transzplantációra sor kerül. Pulmonalis endarterectomia Krónikus thromboemboliás betegség miatti pulmonalis hipertónia esetén a javasolt terápiás eljárás a pulmonalis endarterectomia (korábban ugyanezt a műtétet thrombendarterectomiának hívtuk, de ez már valójában nem az eredeti thrombust, hanem a helyén szervült kocsonyás öntvényt távolítja el). (20) A nehéz műtét súlyos distalis és proximalis formában egyaránt elvégezhető. Az eljárás igen sikeres, óriási életminőség-javulást eredményezhet. Szűrés PAH-ra nagy kockázatú csoportoknál: - scleroderma (CREST);
- familiáris PAH. E betegeknél 1-3 évente Doppler-echokardiográfia javasolt.
Irodalom - Miyamoto S, Nagaya N, Satoh T, Kyotani S, Sakamaki F, Fujita M, Nakanishi N, Miyatake K. Clinical correlates and prognostic significance of six-minute walk test in patients with primary pulmonary hypertension. Comparison with cardiopulmonary exercise testing. Am J Respir Crit Care Med. 2000 Feb;161(2 Pt 1):487-92.
- D'Alonzo GE, Barst RJ, Ayres SM, Bergofsky EH, Brundage BH, Detre KM, Fishman AP, Goldring RM, Groves BM, Kernis JT, et al. Survival in patients with primary pulmonary hypertension. Results from a national prospective registry. Ann Intern Med. 1991 Sep 1;115(5):343-9.
- Sitbon O, Humbert M, Nunes H, Parent F, Garcia G, Herve P, Rainisio M, Simonneau G. Long-term intravenous epoprostenol infusion in primary pulmonary hypertension: prognostic factors and survival. J Am Coll Cardiol. 2002 Aug 21;40(4):780-8.
- McLaughlin VV, Shillington A, Rich S. Survival in primary pulmonary hypertension: the impact of epoprostenol therapy. Circulation. 2002 Sep 17;106(12):1477-82.
- Wensel R, Opitz CF, Anker SD, Winkler J, Hoffken G, Kleber FX, Sharma R, Hummel M, Hetzer R, Ewert R. Assessment of survival in patients with primary pulmonary hypertension: importance of cardiopulmonary exercise testing. Circulation. 2002 Jul 16;106(3):319-24.
- Raymond RJ, Hinderliter AL, Willis PW, Ralph D, Caldwell EJ, Williams W, Ettinger NA, Hill NS, Summer WR, de Boisblanc B, Schwartz T, Koch G, Clayton LM, Jobsis MM, Crow JW, Long W. Echocardiographic predictors of adverse outcomes in primary pulmonary hypertension. J Am Coll Cardiol. 2002 Apr 3;39(7):1214-9.
- Tei C, Dujardin KS, Hodge DO, Bailey KR, McGoon MD, Tajik AJ, Seward SB Doppler echocardiographic index for assessment of global right ventricular function. J Am Soc Echocardiogr. 1996 Nov-Dec;9(6):838-47.
- Nagaya N, Nishikimi T, Uematsu M, Satoh T, Kyotani S, Sakamaki F, Kakishita M, Fukushima K, Okano Y, Nakanishi N, Miyatake K, Kangawa K. Plasma brain natriuretic peptide as a prognostic indicator in patients with primary pulmonary hypertension. Circulation. 2000 Aug 22;102(8):865-70.
- Torbicki A, Kurzyna M, Kuca P, Fijalkowska A, Sikora J, Florczyk M, Pruszczyk P, Burakowski J, Wawrzynska L. Detectable serum cardiac troponin T as a marker of poor prognosis among patients with chronic precapillary pulmonary hypertension. Circulation. 2003 Aug 19;108(7):844-8. Epub 2003 Aug 04.
- Barst RJ, Rubin LJ, Long WA, McGoon MD, Rich S, Badesch DB, Groves BM, Tapson VF, Bourge RC, Brundage BH, et al. A comparison of continuous intravenous epoprostenol (prostacyclin) with conventional therapy for primary pulmonary hypertension. The Primary Pulmonary Hypertension Study Group. N Engl J Med. 1996 Feb 1;334(5):296-302.
- Sitbon O, Humbert M, Nunes H, Parent F, Garcia G, Herve P, Rainisio M, Simonneau G. Long-term intravenous epoprostenol infusion in primary pulmonary hypertension: prognostic factors and survival. J Am Coll Cardiol. 2002 Aug 21;40(4):780-8.
- Fuster V, Steele PM, Edwards WD, Gersh BJ, McGoon MD, Frye RL. Primary pulmonary hypertension: natural history and the importance of thrombosis. Circulation. 1984 Oct;70(4):580-7.
- Farber HW, Karlinsky JB, Faling LJ. Fatal outcome following nifedipine for pulmonary hypertension. Chest. 1983 Apr;83(4):708-9.
- Partanen J, Nieminen MS, Luomanmaki K. Death in a patient with primary pulmonary hypertension after 20 mg of nifedipine. N Engl J Med. 1993 Sep 9;329(11):812; author reply 812-3.
- Sitbon O, Humbert M, Jagot JL, Taravella O, Fartoukh M, Parent F, Herve P, Simonneau G. Inhaled nitric oxide as a screening agent for safely identifying responders to oral calcium-channel blockers in primary pulmonary hypertension. Eur Respir J. 1998 Aug;12(2):265-70.
- Sitbon et al: ATS meeting 2003.
- Michelakis ED, Tymchak W, Noga M, Webster L, Wu XC, Lien D, Wang SH, Modry D, Archer SL. Long-term treatment with oral sildenafil is safe and improves functional capacity and hemodynamics in patients with pulmonary arterial hypertension. Circulation. 2003 Oct 28;108(17):2066-9. Epub 2003 Oct 20.
- Boucek MM, Edwards LB, Keck BM, Trulock EP, Taylor DO, Mohacsi PJ, Hertz MI. The Registry of the International Society for Heart and Lung Transplantation: Sixth Official Pediatric Report--2003. J Heart Lung Transplant. 2003 Jun;22(6):636-52
- Sandoval J, Rothman A, Pulido T. Atrial septostomy for pulmonary hypertension. Clin Chest Med. 2001 Sep;22(3):547-60. Review.
- Jamieson SW, Kapelanski DP, Sakakibara N, Manecke GR, Thistlethwaite PA, Kerr KM, Channick RN, Fedullo PF, Auger WR. Pulmonary endarterectomy: experience and lessons learned in 1,500 cases. Ann Thorac Surg. 2003 Nov;76(5):1457-62; discussion 1462-4.
- European Society of Cardiology guidelines on primary pulmonary hypertension. ESC congress Vienna, 2003
- Vachiery JL, Brimioulle S, Crasset V, Naeije R. False-positive diagnosis of pulmonary hypertension by Doppler echocardiography. Eur Respir J. 1998 Dec;12(6):1476-8
- McQuillan BM, Picard MH, Leavitt M, Weyman AE. Clinical correlates and reference intervals for pulmonary artery systolic pressure among echocardiographically normal subjects. Circulation. 2001 Dec 4;104(23):2797-802.
- Collados MT, Velazquez B, Borbolla JR, Sandoval J, Masso F, Montano LF, Guarner V. Endothelin-1 and functional tissue factor: a possible relationship with severity in primary pulmonary hypertension. Heart Vessels. 2003 Mar;18(1):12-7.
- Rich S, McLaughlin VV. Endothelin receptor blockers in cardiovascular disease. Circulation. 2003 Nov 4;108(18):2184-90.
- Rondelet B, Van Beneden R, Kerbaul F, Motte S, Fesler P, McEntee K, Brimioulle S, Ketelslegers JM, Naeije R. Expression of the serotonin 1b receptor in experimental pulmonary hypertension. Eur Respir J. 2003 Sep;22(3):408--12.
- Paramothayan NS, Lasserson TJ, Wells AU, Walters EH. Prostacyclin for pulmonary hypertension. Cochrane Database Syst Rev. 2003;(2):CD002994
|
|
|

|
|





